ভৌত বিজ্ঞান (Physical Science) হলো প্রাকৃতিক বিজ্ঞানের সেই শাখা যা অ-জীব বা জড় জগতের বস্তু, শক্তি, গঠন এবং তাদের পারস্পরিক মিথস্ক্রিয়া নিয়ে অধ্যয়ন করে । এটি মূলত পদার্থবিজ্ঞান, রসায়ন, জ্যোতির্বিদ্যা এবং পৃথিবী বিজ্ঞানের সমন্বয়ে গঠিত, যা আমাদের চারপাশের ভৌত জগতকে বিশ্লেষণ করে ।
ভৌত বিজ্ঞানের মূল দিকসমূহ:
সংজ্ঞা: জড় পদার্থ (matter) এবং শক্তি (energy) সম্পর্কিত জ্ঞানই ভৌত বিজ্ঞান ।
প্রধান শাখা:
পদার্থবিজ্ঞান (Physics): শক্তি, বল, গতি, তাপ, আলো ও শব্দ নিয়ে আলোচনা করে ।
রসায়ন (Chemistry): পদার্থের গঠন, বৈশিষ্ট্য এবং তাদের পরিবর্তন নিয়ে অধ্যয়ন করে।
জ্যোতির্বিদ্যা (Astronomy): নক্ষত্র, গ্রহ, মহাবিশ্ব ও মহাজাগতিক বস্তু নিয়ে গবেষণা ।
পৃথিবী বিজ্ঞান (Earth Science): ভূতত্ত্ব ও আবহাওয়াবিদ্যা ।
লক্ষ্য: প্রাকৃতিক ঘটনাগুলো কেন এবং কীভাবে ঘটে, তার গাণিতিক ও পর্যবেক্ষণমূলক ব্যাখ্যা প্রদান করা ।
জীববিজ্ঞানের (Biology) বিপরীতে এটি অজৈব বা অ-জীব সিস্টেমের উপর ফোকাস করে ।
# বহুনির্বাচনী প্রশ্ন
পদার্থ (Matter)
যার ভর আছে, যা কোনো স্থান দখল করে অবস্থান করে, তাকে পদার্থ বলা হয়।
বৈশিষ্ট্য | পদার্থ | শক্তি |
| ভর | ভর আছে | ভর নাই |
| স্থান দখল | করে | করে না |
| উদাহরণ | বাতাস, পানি | তাপ, আলোক, বিদ্যুৎ |
# বহুনির্বাচনী প্রশ্ন
পদার্থ ও শক্তি (Matter and Energy) প্রকৃতিতে দুটি ভিন্ন বিষয়ের অস্তিত্ব আমরা বুঝতে পারি একটি জড় বা পদার্থ (matter) এবং অন্যটি হল শক্তি (energy) ।
পদার্থ (Matter) : যা ইন্দ্রিয় গ্রাহ্য, যা কিছুটা স্থান দখল করে, যার ওজন আছে এবং বলপ্রয়োগের সাহায্যে যার স্থির বা গতিশীল অবস্থার পরিবর্তন করা যায়, তাকেই পদার্থ বলে । যেমন চেয়ার, টেবিল, ইট, বালি, খাতা, পেন্সিল ইত্যাদি । পদার্থের নির্দিষ্ট পরিমাণকে বস্তু বলে । যেমন প্লাস্টিক দিয়ে জলের বালতি, মগ তৈরি করা হয় সুতরাং জলের বালতি, মগ হল বস্তু কিন্তু এগুলির উপাদান প্লাস্টিক হল পদার্থ অর্থাৎ বস্তু যে উপাদানে তৈরি হয় তাকে জড় বা পদার্থ বলে । পৃথিবীতে জড়বস্তু এবং সজীব বস্তু এই দুই ধরনের বস্তু আমরা দেখতে পাই ।
ভর এবং ভার বা ওজন : বস্তুর ভার বা ওজন নির্ণয় : ভরের নিত্যতা সূত্র বা পদার্থের অবিনাশিতা সূত্র : শক্তির বিভিন্ন রূপ : শক্তির নিত্যতা সূত্র : শক্তির রূপান্তর : সূর্যই পৃথিবীর শক্তির প্রধান উৎস
# বহুনির্বাচনী প্রশ্ন
পদার্থের অবস্থাভেদ
States of Matter
পদার্থ সাধারণত ৩টি অবস্থায় থাকতে পারে। যথা: কঠিন, তরল এবং বায়বীয়
| কঠিন পদার্থ | কঠিন পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার এবং দৃঢ়তা আছে। এর অণুসমূহ পরস্পরের অতি সন্নিকটে অবস্থান করে। যেমন: বালু, পাথর, লবণ ইত্যাদি। |
| তরল পদার্থ | তরল পদার্থের নির্দিষ্ট আয়তন আছে কিন্তু নির্দিষ্ট আকার নেই। তরল পদার্থের অণুসমূহ পরস্পরের সন্নিকটে থাকে, তবে তাদের মধ্যকার আকর্ষণ কঠিন পদার্থের মত প্রবল নয়। উদাহরণ: পানি, পেট্রোল, কেরোসিন, ভোজ্য তেল প্রভৃতি। |
| গ্যাসীয় পদার্থ | গ্যাসীয় পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার নেই। গ্যাসীয় পদার্থের অণুসমূহের দূরত্ব অনেক বেশি, তাই আকর্ষণ শক্তি অনেক কম। ফলে তারা প্রায় সম্পূর্ণ মুক্তভাবে চলাচল করে। উদাহরণ: নাইট্রোজেন, অক্সিজেন, মিথেন ইত্যাদি। |
তাপ পদার্থের তিন অবস্থায় রূপান্তরের প্রধান কারণ। পানি একমাত্র পদার্থ যা প্রকৃতিতে কঠিন (বরফ), তরল (পানি) এবং বায়বীয় (জলীয় বাষ্প) তিন অবস্থাতেই পাওয়া যায়।
কঠিন | তরল | বায়বীয় |
| মেরু অঞ্চল বা পর্বত শীর্ষের বরফ | নদী, সমুদ্রের পানি | বায়ুর জলীয় বাষ্প |
# বহুনির্বাচনী প্রশ্ন
গলনাংক (Melting point)
যে তাপমাত্রায় কঠিন হতে তরল পদার্থের সৃষ্টি হয়, তাকে সে পদার্থের গলনাংক বলে। পানির গলনাংক ০° সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
০ ডিগ্রি
৯৯-৯৮ ডিগ্রি
৪ ডিগ্রি
১০০ ডিগ্রি
স্ফুটনাংক (Boiling Point)
যে তাপমাত্রায় কোন তরল পদার্থ ফুটতে থাকে, তাকে সে পদার্থের স্ফুটনাংক বলে। পানির স্ফুটনাংক ১০০ ডিগ্রী সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
ঠিক থাকে
কম হয়
বেশি হয়
কোনোটিই নয়
ঊর্ধ্বপাতন (Sublimation)
কোনো কোনো ক্ষেত্রে কঠিন পদার্থকে উত্তপ্ত করলে তা তরলে রূপান্তরিত না হয়ে সরাসরি বাষ্পে রূপান্তরিত হয়, তাকে ঊর্ধ্বপাতন বলা হয়। যেমন: কপূর, গন্ধক, আয়োডিন, ন্যাপথালিন, অ্যামোনিয়াম ক্লোরাইড, কার্বন ডাই অক্সাইড, আর্সেনিক, বেনজোয়িক এসিড ইত্যাদি।
পদার্থের শ্রেণিবিভাগ:
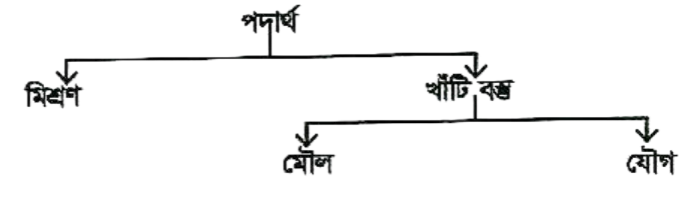
মিশ্রণ (Mixture)
দুই বা ততোধিক পদার্থকে যে কোন অনুপাতে একত্রে মিশালে যদি তারা নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে, তবে উক্ত সমাবেশকে মিশ্রণ বলা হয়। বায়ু একটি মিশ্র পদার্থ কারণ বায়ুতে উপাদান মৌলসমূহ যেমন: নাইট্রোজেন, অক্সিজেন, কার্বন-ডাই-অক্সাইড ইত্যাদি নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে।
খাঁটি বস্তু (Pure substance)
মৌল বা মৌলিক পদার্থ (Elements)
| সবচেয়ে হালকা মৌল | হাইড্রোজেন (H) |
| সবচেয়ে হালকা মৌলিক গ্যাস | হাইড্রোজেন (H) |
| সবচেয়ে ভারী মৌলিক গ্যাস | রেডন (Rn) |
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করে অন্য কোন সহজ বস্তুতে রূপান্তরিত করা যায় না, তাকে মৌল বা মৌলিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন, নাইট্রোজেন, অক্সিজেন, সোনা, তামা, লোহা ইত্যাদি। পৃথিবীতে বর্তমানে মৌলিক পদার্থের সংখ্যা ১১৮। এদের মধ্যে ৯৮টি মৌল প্রকৃতিতে পাওয়া যায়। কৃত্রিম উপায়ে প্রাপ্ত মৌলিক পদার্থের সংখ্যা ২০।
যৌগ বা যৌগিক পদার্থ (Compound)
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করলে দুই বা ততোধিক মৌলিক পদার্থ পাওয়া যায়, তাকে যৌগ বা যৌগিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন ও অক্সিজেন এ দুইটি মৌল নির্দিষ্ট ভর অনুপাতে পরস্পর যুক্ত হয়ে পানি উৎপন্ন করে। অতএব পানি একটি যৌগিক পদার্থ।
# বহুনির্বাচনী প্রশ্ন
পদার্থের পরিবর্তন (Changes in matter)
পদার্থের পরিবর্তন দুই ধরনের। যথা: ভৌত বা অবস্থানগত পরিবর্তন এবং রাসায়নিক পরিবর্তন।
# বহুনির্বাচনী প্রশ্ন
ভৌত বা অবস্থানগত পরিবর্তন (Physical Change)
যে পরিবর্তনের ফলে পদার্থের শুধু বাহ্যিক আকার বা অবস্থার পরিবর্তন হয় কিন্তু নতুন কোনো পদার্থে পরিণত হয় না, তাকে ভৌত বা অবস্থানগত পরিবর্তন বলে।
ভৌত পরিবর্তনের উদাহরণ :
➺ পানিকে ঠাণ্ডা করে বরফে এবং তাপ দিয়ে জলীয় বাষ্পে পরিণত করা।
➺ একটি লোহার টুকরাকে চুম্বক দ্বারা ঘর্ষণ করে চুম্বকে পরিণত করা।
➺ তাপ দিয়ে মোম গলানো।
# বহুনির্বাচনী প্রশ্ন
স্টার্ট
সেলুলোজ
গ্লুকোজ
প্লাইকোজেন
রাসায়নিক পরিবর্তন : যে পরিবর্তনের ফলে এক বা একাধিক বস্তু প্রত্যেকে তার নিজস্ব সত্তা হারিয়ে সম্পূর্ণ নতুন ধর্ম বিশিষ্ট এক বা একাধিক নতুন বস্তুতে পরিণত হয়, তাকে রাসায়নিক পরিবর্তন বলে।
রাসায়নিক পরিবর্তনের উদাহরণ :
➺ লোহায় মরিচা ধরা। মরিচা (Rust) হলো আর্দ্র ফেরিক অক্সাইড (Fe2O3. nH2O)। লোহায় মরিচা ধরার জন্য পানি এবং অক্সিজেন প্রয়োজন।
➺ দুধকে ছানায় পরিণত করা
➺ চাল সিদ্ধ করলে ভাতে পরিণত হয়।
➺ দিয়াশলাইয়ের কাঠি জ্বালানো
# বহুনির্বাচনী প্রশ্ন
পদার্থের গঠন মূলত ক্ষুদ্রতম কণা, যেমন—পরমাণু ও অণু দ্বারা গঠিত, যা স্থান দখল করে এবং যার ভর আছে । পরমাণুর কেন্দ্রে প্রোটন ও নিউট্রন (নিউক্লিয়াস) এবং বাইরে ইলেকট্রন থাকে । এছাড়া, কোয়ার্ক ও লেপটন নামক অবিভাজ্য মৌলিক কণা দিয়েও পদার্থ গঠিত হতে পারে । পরমাণুসমূহ একত্রে অণু তৈরি করে এবং আন্তঃআণবিক বন্ধনের মাধ্যমে কঠিন, তরল বা গ্যাসীয় অবস্থায় থাকে ।
# বহুনির্বাচনী প্রশ্ন
ডাল্টনের পরমাণুবাদ (Dalton's atomic Theory)
গ্রীক দার্শনিক ডেমোক্রিটাস খ্রিস্টপূর্ব পঞ্চম শতাব্দীতে এ অভিমত প্রকাশ করেন যে, সকল পার্থিব বস্তু ক্ষুদ্র ক্ষুদ্র অবিভাজ্য কণার দ্বারা গঠিত। ডেমোক্রিটাস এ অবিভাজ্য ক্ষুদ্রতম কণার নাম দেন atomos। এ শব্দটি দুটি গ্রিক শব্দ হতে উদ্ভূত। a (অর্থাৎ না) এবং tomos (অর্থাৎ ভাগ করা)। তাই atomos শব্দের অর্থ যা ভাগ করা যায় না। ব্রিটিশ বিজ্ঞানী জন ডাল্টন ১৮০৩ সালে এ মতবাদকে বৈজ্ঞানিক মতবাদ হিসাবে প্রতিষ্ঠা করেন। আধুনিক রসায়নের ভিত্তি হচ্ছে এ পরমাণুবাদ। এ কারণে জন ডাল্টনকে 'আধুনিক রসায়নের জনক' বলা হয়।
পরমাণু (Atoms) | অণু (Molecules) |
| মৌলিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা | মৌলিক বা যৌগিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা। |
| রাসায়নিক প্রক্রিয়ায় সরাসরি অংশগ্রহণ করে। | রাসায়নিক প্রক্রিয়ায় সরাসরি অংশগ্রহণ করে না |
অধিকাংশ মৌলের পরমাণু খুব সক্রিয়। এরা যেমন ভিন্ন পদার্থের সাথে বিক্রিয়া করে যেমন যৌগিক পদার্থের সৃষ্টি করে, তেমনি একই পদার্থের সাথে মিলিত হয়ে মৌলিক পদার্থের অণু সৃষ্টি করে। মৌলিক গ্যাসের অণুসমূহ দ্বিপরমাণুক। যেমন- অক্সিজেন (O2), হাইড্রোজেন (H2) প্রভৃতি। নিষ্ক্রিয় গ্যাস [হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Cr), জেনন (Xe), রেডন (Rn)]-এর অণুসমূহ এক পরমাণুক।
পারমাণবিক ভর ও আণবিক ভর (Atomic mass and molecular mass)
পারমাণবিক ভর হচ্ছে একটি সরল রাশি যা একটি পরমাণু একটি কার্বন-১২ পরমাণুর ভরের ১/১২ অংশের তুলনায় কতগুণ ভারী তা প্রকাশ করে। আর আণবিক ভর হলো কোনো পদার্থের একটি অণুর ভর একটি কার্বন ১২ পরমাণুর ভরের ১/১২ অংশের যতগুণ ভারী, সে সংখ্যাকে আণবিক ভর বলা হয়। উদাহরণস্বরূপ, পানির সংকেত H2O। পানির একটি অণুতে ২টি হাইড্রোজেন ও ১টি অক্সিজেন পরমাণু বিদ্যমান।
পানির আণবিক ভর = (হাইড্রোজেনের পারমাণবিক ভর ২) + (অক্সিজেনের পারমাণবিক ভর ১)
= (১ ২) + (১৬ ১) = ২ + ১৬ = ১৮
একইভাবে, অক্সিজেনের সংকেত O2। অক্সিজেনের একটি অণুতে ২টি অক্সিজেন পরমাণু বিদ্যমান। অক্সিজেনের আণবিক ভর = অক্সিজেনের পারমাণবিক ভর ২ = ১৬ ২ = ৩২।
অ্যাভোগেড্রোর সূত্র (Avogadro's Law)
একই তাপমাত্রা ও চাপে সমআয়তন বিশিষ্ট সকল গ্যাসে (মৌলিক ও যৌগিক) সমান সংখ্যক অণু থাকে। কোনো বস্তুর এক মোলে যত সংখ্যক অণু বা পরমাণু থাকে সেই সংখ্যাকে অ্যাভোগেড্রো সংখ্যা বলে। অ্যাভোগেড্রো সংখ্যার মান ৬.০২ ১০২৩। উদাহরণ: এক মোল (অর্থাৎ ১ গ্রাম) হাইড্রোজেনে ৬.০২ ১০২৩ টি হাইড্রোজেন পরমাণু আছে।
মৌলের প্রতীক
কোনো মৌলের ইংরেজি বা ল্যাটিন নামের সংক্ষিপ্ত রূপকে প্রতীক বলে। প্রত্যেকটি মৌলকে সংক্ষেপে প্রকাশ করতে তাদের আলাদা আলাদা প্রতীক ব্যবহার করা হয়। মৌলের প্রতীক লিখতে কিছু নিয়ম অনুসরণ করতে হয়।
মৌল | ল্যাটিন নাম | প্রতীক |
| কপার | Cuprum | Au |
| লেড | Plumbum | Pb |
| সোডিয়াম | Natrium | Na |
| টাংস্টেন | Wolfram | W |
| মারকারি | Hydrurgyrum | Hg |
| আয়রন | Ferrum | Fe |
| পটাশিয়াম | Kalium | K |
| সিলভার | Argentum | Ag |
| টিন | Stannum | Sn |
| এন্টিমনি | Stibium | sb |
| গোল্ড | Aurum | Au |
মৌল | ইংরেজি নাম | প্রতীক |
| হাইড্রোজেন | Hydrogen | H |
| অক্সিজেন | Oxygen | O |
| নাইট্রোজেন | Nitrogen | N |
মৌলের নামকরণ
মৌল | ইংরেজি নাম | প্রতীক |
| কার্বন | Carbon | C |
| ক্লোরিন | Chlorine | Cl |
| ক্যালসিয়াম | Calcium | Ca |
মৌলের নামকরণ (প্রথম অক্ষর এক)।
মৌল | ইংরেজি নাম | প্রতীক |
| কোবাল্ট | Cobalt | Co |
| ক্যাডমিয়াম | Cadmium | Cd |
| ক্রোমিয়াম | Chromium | Cr |
a) মৌলের ইংরেজি নামের প্রথম অক্ষর দিয়ে প্রতীক লেখা হয় এবং তা ইংরেজি বর্ণমালার বড় হাতের অক্ষর দিয়ে প্রকাশ করা হয়।
(b) যদি দুই বা দুইয়ের অধিক মৌলের ইংরেজি নামের প্রথম অক্ষর একই হয় তবে একটি মৌলকে নামের প্রথম অক্ষর (ইংরেজি বর্ণমালার বড় হাতের) দিয়ে প্রকাশ করা হয়। অন্যগুলোর ক্ষেত্রে প্রতীকটি দুই অক্ষরে লেখা হয়। নামের প্রথম অক্ষরটি ইংরেজি বর্ণমালার বড় হাতের অক্ষর এবং নামের অন্য একটি অক্ষর ছোট হাতের অক্ষর দিয়ে লেখা হয়।
(c) কিছু মৌলের প্রতীক তাদের ল্যাটিন নাম থেকে নেওয়া হয়েছে।
# বহুনির্বাচনী প্রশ্ন
অণু হলো পদার্থের ক্ষুদ্রতম কণা যাতে পদার্থের সকল গুণাগুণ বিদ্যমান থাকে, যা দুই বা ততোধিক পরমাণুর সমবায়ে গঠিত ।
আর অণুর সংকেত (Chemical Formula) হলো প্রতীকের সাহায্যে অণুর উপাদান ও গঠন সংক্ষিপ্তভাবে প্রকাশের পদ্ধতি, যা মৌল ও যৌগের সংকেত হিসেবে ব্যবহৃত হয় (যেমন: পানির অণু ।
# বহুনির্বাচনী প্রশ্ন
2 : 2 : 2
1 : 2 : 1
2 : 2 : 1
1 : 3 : 1
দুই বা ততোধিক মৌলের একাধিক পরমাণু এক সাথে যুক্ত হয়ে যদি একটি মাত্র পরমাণুর মতো আচরণ করে তবে তাকে যৌগমূলক বলে। যৌগমূলকসমূহের যোজনী একটি পরমাণুর মতো হয়ে থাকে। যেমন একটি যৌগমূলক, যার যোজনী ২।
যৌগমূলক ধনাত্মক কিংবা ঋণাত্মক আধানবিশিষ্ট হতে পারে। এদের আধান সংখ্যাই মূলত এদের যোজনী নির্দেশ করে। যেমন: একটি N পরমাণুর সাথে তিনটি H পরমাণু ও একটি H+ যুক্ত হয়ে অ্যামোনিয়াম (NH +) আয়ন নামক যৌগমূলকের সৃষ্টি করে। এর আধান সংখ্যা হলো +1 (এক)। সূতরাং এর যোজনীও 1 (এক)। আধান বা চার্জ ধনাত্মক বা ঋণাত্মক হতে পারে কিন্তু যোজনী শুধু একটি সংখ্যা এর কোনো ধনাত্মক চিহ্ন বা ঋণাত্মক চিহ্ন নেই।
# বহুনির্বাচনী প্রশ্ন
মৌলিক পদার্থের যে ক্ষুদ্রতম কণার মধ্যে মৌলটির সমস্ত ধর্ম উপস্থিত থাকে এবং যা রাসয়ানিক বিক্রিয়ায় অংশগ্রহণ করে তাকে মৌলিক পদার্থটির পরমাণু বলে। সমস্ত কঠিন, তরল, গ্যাস এবং আয়ন -এর গঠনের মূলে রয়েছে নিস্তরিত বা আধানগ্রস্ত পরমাণু। পরমাণুর আকার খুবই ক্ষুদ্র; সাধারনত এরা দৈর্ঘ্যে ১০০ পিকোমিটার (১ মিটারের ১০,০০০,০০০,০০০ ভাগের ১ ভাগ)।
পরমাণুর মাত্রা এই ক্ষুদ্রাকার হওয়ার কারণেই এর আচরনের বৈশিষ্টতা প্রথাগত পদার্থবিদ্যার সূত্র দিয়ে ব্যাখ্যা করা যায় না।
# বহুনির্বাচনী প্রশ্ন
মৌলিক কণিকা (Fundamental Particles)
যে সব সূক্ষ্ম কণিকা দ্বারা পরমাণু গঠিত, তাদেরকে মৌলিক কণিকা বলে। পরমাণুতে তিন ধরনের মৌলিক কণিকা থাকে। যথা- ইলেকট্রন, প্রোটন এবং নিউট্রন।
| ইলেকট্রন | পরমাণুর ক্ষুদ্রতম কণিকা ইলেকট্রন |  |
| প্রকৃত ভর । প্রতীক e- | ||
| চার্জ বা আধান: ঋণাত্মক ( কুলম্ব) | ||
| প্রোটন | একটি হাইড্রোজেন পরমাণু থেকে একটি ইলেকট্রন সরিয়ে নিয়ে যা থাকে তা একটি প্রোটন। এই কারণে প্রোটনের সংকেত । |  |
| প্রকৃত ভর ।প্রতীক P | ||
| চার্জ বা আধান: ধনাত্মক (কুলম্ব) | ||
| নিউট্রন | নিউট্রনের কোনো আধান নাই। Neutral হওয়ার কারণেই এর এই নামকরণ করা হয়েছে। |  |
| প্রকৃত ভর । প্রতীক n |
# বহুনির্বাচনী প্রশ্ন
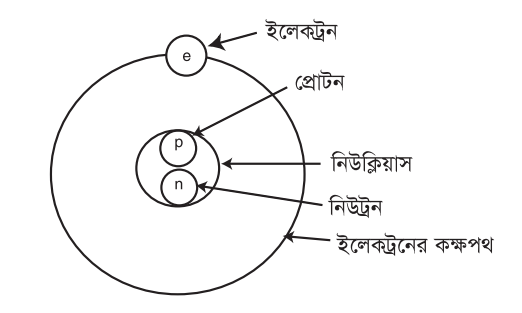
পরমাণুর গঠন (Structure of Atoms)
পরমাণুর একটি কেন্দ্র আছে, যার নাম নিউক্লিয়াস (Necleus)। এই নিউক্লিয়াসে প্রোটন ও নিউট্রন অবস্থান করে। সুতরাং পরমাণুর সকল ধনাত্মক আধান এবং প্রায় সম্পূর্ণ ভরই নিউক্লিয়াসে কেন্দ্রীভূত। ইলেকট্রন নিউক্লিয়াসের বাহিরে থাকে এবং তার চারদিকে ভ্রমণ করে। পরমাণু বৈদ্যুতিক নিরপেক্ষ, কারণ একটি পরমাণুতে যতটি প্রোটন আছে, ততটি ইলকট্রনও আছে। অবশ্য পরমাণু হতে সহজেই ইলেকট্রন বের করে আনা যায় এবং বাহির হতে অতিরিক্ত ইলেকট্রন যোগও করা যায়। তখন আর বিদ্যুৎ নিরপেক্ষ পরমাণু থাকে না, আধানযুক্ত আয়নের সৃষ্টি হয়। ঘর্ষণ, তাপ, রাসায়নিক প্রভৃতি প্রক্রিয়ায় সহজেই পরমাণু থেকে ইলেকট্রন নির্গত হয়।
# বহুনির্বাচনী প্রশ্ন
পরমাণুর ইলেকট্রন বিন্যাস (Electronic configuration of atoms)
পরমাণুতে ইলেকট্রনগুলো যেভাবে সজ্জিত বা বিন্যস্ত থাকে তাই ঐ পরমাণুর ইলেকট্রন বিন্যাস। পরমাণুর প্রতিটি শক্তিস্তরে সর্বোচ্চ ইলেকট্রনের সংখ্যা 2n2।
প্রথম শক্তিস্তরে (n=1) সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা =2n2 = 212 = 2 .
দ্বিতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 22 = 8
তৃতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 32 = 18
চতুর্থ শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 42 = 32

# বহুনির্বাচনী প্রশ্ন
পারমাণবিক সংখ্যা (Atomic Number)
নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাকে মৌলের পারমাণবিক সংখ্যা বলা হয়। একে Z দ্বারা প্রকাশ করা হয়। যে কোনো মৌলের স্বাতন্ত্র্য এই সংখ্যার উপর নির্ভর করে। এটি যে কোনো মৌলের মৌলিক ধর্ম। যেমন- কার্বনের পরমাণুতে ৬টি প্রোটন আছে। সুতরাং কার্বনের পারমাণবিক সংখ্যা ৬।
# বহুনির্বাচনী প্রশ্ন
ভর সংখ্যা বা নিউক্লিয়ন সংখ্যা (Mass Number)
নিউক্লিয়াসে অবস্থিত প্রোটন ও নিউট্রনের মোট সংখ্যাকে একটি পরমাণুর ভর সংখ্যা বলা হয়। ভর সংখ্যাকে A দ্বারা প্রকাশ করা হয়। কোনো পরমাণুর অন্তর্গত প্রোটন ও নিউট্রনের মোট সংখ্যাকে ভর সংখ্যা বলা হয়। ভর সংখ্যা A, প্রোটন সংখ্যা P এবং নিউট্রন সংখ্যা N হলে, পরমাণুর ভর সংখ্যা A = P + N। সোডিয়ামের একটি পরমাণুতে প্রোটন আছে ১১টি, নিউট্রন আছে ১২টি। সুতরাং সোডিয়ামের এই পরমাণুর ভর সংখ্যা ২৩।
কতিপয় গুরুত্বপূর্ণ মৌলের পারমাণবিক সংখ্যা ও ভর সংখ্যা
মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা | মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা |
| হাইড্রোজেন | ১ | ১ | সিলিকন | ১৪ | ২৮ |
| হিলিয়াম | ২ | ৪ | ক্যালসিয়াম | ২০ | ৪০.০৮ |
| কার্বন | ৬ | ১২ | আর্সেনিক | ৩৩ | ৭৫ |
| সোডিয়াম | ১১ | ২৩ | পারদ | ৮০ | ২০০.৬ |
| ম্যাগনেসিয়াম | ১২ | ২৪ | ইউরেনিয়াম | ৯২ | ২৩৮ |
পর্যায় সারণীর জনক মেন্ডেলিফ। মেন্ডেলিফের পর্যায় সারণীর ভিত্তি ছিল পারমাণবিক ভর। আধুনিক পর্যায় সারণীর ভিত্তি পারমাণবিক সংখ্যা। আধুনিক পর্যায় সারণীতে ৭ টি পর্যায় পর্যায় এবং ৯টি গ্রুপ রয়েছে।
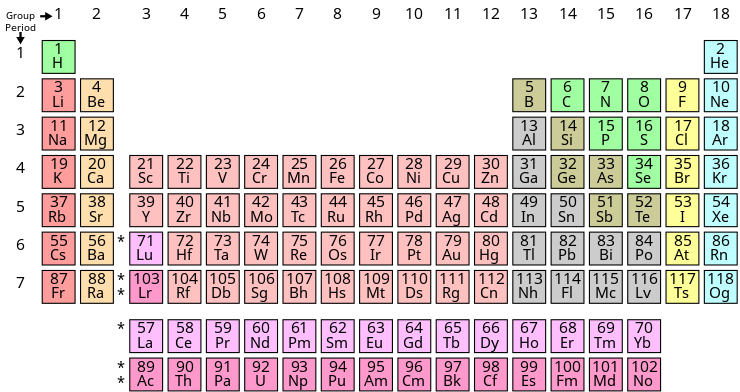
ক্ষার ধাতু (Alkali metal)
যে সকল ধাতু পানির সঙ্গে সরাসরি বিক্রিয়া করে তীব্র ক্ষার গঠন করে, তাকে ক্ষার ধাতু বলে। ক্ষার ধাতুগুলোর নাম লিথিয়াম, সোডিয়াম, পটাসিয়াম, রুবিডিয়াম এবং সিজিয়াম। পর্যায় সারণিতে ক্ষার ধাতুগুলোর অবস্থান IA গ্রুপে।
মৃৎক্ষার ধাতু (Mrtksara metal)
যে সকল ধাতু ভূ-ত্বকের মৃত্তিকার উপাদানরূপে পাওয়া যায় এবং পানির সঙ্গে বিক্রিয়া করে ক্ষারক গঠন করে, তাকে মৃৎক্ষার ধাতু বলে। উদাহরণ: ক্যালসিয়াম, ম্যাগনেসিয়াম। পর্যায় সারণিতে মৃৎক্ষার ধাতুগুলোর অবস্থান IIA গ্রুপে।
নিষ্ক্রিয় গ্যাস (Noble gas)
পর্যায় সারণির শূন্য গ্রুপের মৌলসমূহ রাসায়নিকভাবে নিষ্ক্রিয় এবং কক্ষ তাপমাত্রায় গ্যাসীয়। এদের নিষ্ক্রিয় গ্যাস বলে। নিষ্ক্রিয় গ্যাস ৬টি, যথা- হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Kr), জেনন (Xe) এবং রেডন (Rn)। নিষ্ক্রিয় গ্যাসসমূহের সর্ববহিঃস্থ স্তরে ৮টি ইলেকট্রন থাকে (ব্যতিক্রম: হিলিয়াম)।
হিলিয়ামের সর্ববহিঃস্থ স্তরে ২টি ইলেকট্রন থাকে। মৌলিক গ্যাস' (হাইড্রোজেন (H2), অক্সিজেন (O2)] এর অণুসমূহ দ্বিপরমাণুক। কিন্তু নিষ্ক্রিয় গ্যাসের অণুসমূহ এক পরমাণুক। যেমন: হিলিয়াম (He), নিয়ন (Ne)। মৌলিক গ্যাস র্যাডন সর্বাপেক্ষা ভারি। রেডন তেজস্ক্রিয় মৌল। বিজ্ঞানী ডর্ন ১৯০০ সালে রেডিয়ামের তেজস্ক্রিয় বিভাজন হতে রেডন আবিষ্কার করেন। সূর্যে মৌলিক পদার্থের মধ্যে হিলিয়াম (He) এর পরিমাণ সবচেয়ে বেশি।
ব্যবহার
- বেলুনে এবং ডুবুরিদের জন্য হাইড্রোজেনের পরিবর্তে হিলিয়াম ব্যবহার করা। হাইড্রোজেন হিলিয়াম অপেক্ষা হালকা হলেও হাইড্রোজেন দাহ্য পক্ষান্তরে হিলিয়াম নিষ্ক্রিয়।
- সাধারণ বৈদ্যুতিক বাল্বের ভিতরে সাধারণত নাইট্রোজেন গ্যাস ব্যবহার করা হয়। কিন্তু টিউব লাইটে সাধারণত নিয়ন, আর্গন প্রভৃতি গ্যাস ব্যবহৃত হয়।
- ফটোগ্রাফিক ফ্লাশ লাইটে জেনন গ্যাস ব্যবহৃত হয়।
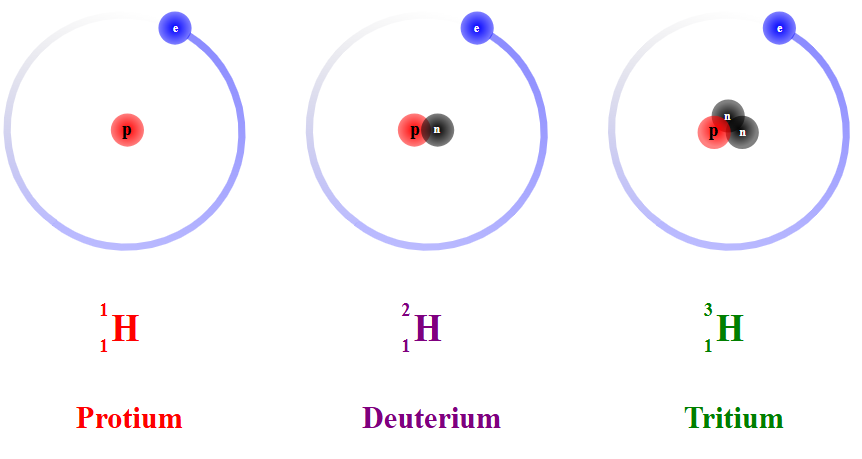
আইসোটোপ
যে সকল পরমাণুর পারমাণবিক সংখ্যা সমান কিন্তু ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। অন্যভাবে বলা যায়, এটমিক সংখ্যা একই হওয়া সত্ত্বেও নিউক্লিয়াসের নিউট্রন সংখ্যা বেশি হওয়ার ফলে ভরসংখ্যা বেড়ে যায়, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। যেমন: হাইড্রোজেনের আইসোটোপগুলো হলো প্রোটিয়াম (1H1), ডিউটেরিয়াম (2H1) ও ট্রিটিয়াম (3H1)। হাইড্রোজেন, ডিউটেরিয়াম এবং ট্রিটিয়াম তিনটিরই পারমাণবিক সংখ্যা 1 কিন্তু ভর সংখ্যা যথাক্রমে 1, 2 এবং 3। লক্ষণীয়, হাইড্রোজেন পরমাণুতে কোনো নিউট্রন থাকে না। ইউরেনিয়ামের তিনটি আইসোটোপ (234U92), (235U92), (238U92) । পারমাণবিক চুল্লীতে বহুল ব্যবহৃত আইসোটোপ (235U92)|
# বহুনির্বাচনী প্রশ্ন
50%
99.3%
0%
69.3%
60Co
32p
65Zn
131 I
আইসোটোন (Isotone)
যে সকল পরমাণুর নিউট্রন সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ও ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোন বলে। যেমন: সিলিকন (30Si14), ফসফরাস (31P15) এবং সালফার (32S16) পরস্পরের
আইসোটোন কারণ
সিলিকনের নিউট্রন সংখ্যা = 30 - 14 = 16
ফসফরাসের নিউট্রন সংখ্যা = 31 - 15 = 16
সালফারের নিউট্রন সংখ্যা = 32 - 16 = 16
কিন্তু এ সকল মৌলের প্রোটন সংখ্যা এবং ভর সংখ্যা ভিন্ন।
# বহুনির্বাচনী প্রশ্ন
আইসোটোপ
আইসোটোন
আইসোবার
আইসোমার
যে সকল পরমাণুর ভর সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোবার বলা হয়। যেমন: কপার (64Cu29) এবং জিংক (64Zn30) পরস্পরের আইসোবার কারণ উভয়ের ভরসংখ্যা 64 কিন্তু প্রোটন সংখ্যা যথাক্রমে 29 এবং 30।
প্রস্তর যুগের পর আসে ধাতুর ব্যবহারের যুগ। খ্রিষ্টপূর্ব ৩৫০০ অব্দের পর পাথরের পর তামার ব্যবহার শুরু হয়। লোহার আবিষ্কার হয় খ্রিষ্টপূর্ব ১৫০০ অব্দে।
# বহুনির্বাচনী প্রশ্ন
ধাতু (Metal)
যে সকল পদার্থ দেখতে চকচকে, তাপ ও বিদ্যুৎ সুপরিবাহী, আঘাত করলে টুনটুন শব্দ হয়, ঘাতসহ প্রসারণশীল ও নমনীয় তাদেরকে ধাতু বলে। এদের পরমাণু ইলেকট্রন ত্যাগ করে ক্যাটায়ন উৎপন্ন করে। উদাহরণ: লিথিয়াম, সোডিয়াম, পটাসিয়াম, ক্যালসিয়াম, ম্যাগনেসিয়াম, অ্যালুমিনিয়াম, দস্তা (Zinc), সোনা, রূপা, তামা (Cupper), প্লাটিনাম, পারদ (Mercury), টাংস্টেন প্রভৃতি।
বৈশিষ্ট্য | ধাতু | বৈশিষ্ট্য | ধাতু |
| সবচেয়ে হালকা ধাতু | লিথিয়াম (Li) | সবচেয়ে সক্রিয় ধাতু | পটাসিয়াম (K) |
| সবচেয়ে ভারী ধাতু | প্লাটিনাম (Pt) | সবচেয়ে তাড়াতাড়ি ক্ষয়প্রাপ্ত হয় | দস্তা (Zn) |
| সবচেয়ে মূল্যবান ধাতু | তার বানানো সহজতর | তামা (Cu) | |
| সর্বোচ্চ গলনাঙ্কের ধাতু | টাংস্টেন | সর্বনিম্ন গলনাঙ্কের ধাতু | পারদ (Hg) |
# বহুনির্বাচনী প্রশ্ন
সোডিয়াম (আধুনিক ল্যাটিন ভাষায় ন্যাট্রিয়াম) একটি মৌলিক পদার্থ যার প্রতীক Na এবং পারমাণবিক সংখ্যা ১১। এটি পর্যায় সারণীর তৃতীয় পর্যায়ে, প্রথম শ্রেণীতে অবস্থিত, যার কারণে এটি ক্ষার ধাতু হিসাবে পরিগণিত। তীব্র সক্রিয়তার কারণে একে প্রকৃতিতে আলাদাভাবে পাওয়া যায় না, সোডালাইট, ফেল্ডস্পার, রকসল্ট ইত্যাদি খনিজ রূপে পাওয়া যায়। মহাবিশ্বে এর উৎপত্তি হয় নক্ষত্রে, ৬০০ মেগাকেলভিন তাপমাত্রায় কার্বন দহন প্রক্রিয়ার মাধ্যমে যখন দুটি কার্বন পরমাণুর মধ্যে ফিউশান ঘটে।
# বহুনির্বাচনী প্রশ্ন
পটাশিয়াম হলো একটি রাসায়নিক উপাদান যা K প্রতীক দ্বারা প্রকাশ করা হয় ( নিও-ল্যাটিন ক্যালিয়াম থেকে ) এবং এর পারমাণবিক সংখ্যা ১৯ ৷ পটাশিয়াম হলো একটি রুপালি-সাদা ধাতু যা একটি ছুরির মাধ্যমে সামান্য শক্তি দিয়ে কাটার জন্য যথেষ্ট নরম।
# বহুনির্বাচনী প্রশ্ন
অ্যালুমিনিয়াম একটি মৌলিক পদার্থ যার প্রতীক Al এবং পারমাণবিক সংখ্যা ১৩। এটি বোরন গ্রুপের সদস্য যার রং ধূসর সাদা; গঠনে কোমল, অচৌম্বকীয় এবং যথেষ্ট সংকোচন-প্রসারণক্ষম। ভর অনুপাতে ভূ-পৃষ্ঠের ৮ শতাংশ অ্যালুমিনিয়াম। অক্সিজেন ও সিলিকনের পর ভূ-পৃষ্ঠের মৌল হিসেবে এর অবস্থান ৩য়, যদিও ভূপৃষ্ঠের গভীরে নগন্য মাত্রায় বিদ্যমান। এর প্রধান আকরিক হল বক্সাইট। রাসায়নিকভাবে অ্যালুমিনিয়াম খুবই সক্রিয় বলে তীব্র বিজারনীয় পরিবেশ ছাড়া একে বিশুদ্ধ অবস্থায় পাওয়া যায় না। একারণে ২৭০ ধরনের ভিন্ন পদার্থে এর উপস্থিতি রয়েছে।
এটি বেশ হালকা ও দীর্ঘদিন ব্যবহারে অক্ষয়িষ্ণু। একারণে এর বহুবিধ ব্যবহার লক্ষ্য করা যায়। মহাকাশীয় যন্ত্রপাতি, যানবাহন ও নির্মানকাজে (জানালার কাঠামো, আংটা ইত্যাদি) অ্যালুমিনিয়াম ও এর সংকর ধাতুসমূহের বহুল ব্যবহার লক্ষনীয়। এর অক্সাইড ও সালফেটসমূহ সবচেয়ে বেশি ব্যবহৃত যৌগ। কোন জীবন্ত প্রাণী তাদের জৈবিক কার্যাবলিতে অ্যালুমিনিয়ামের লবণ ব্যবহার না করলেও মাটিতে প্রচুর পরিমাণে থাকায় উদ্ভিদসমূহে তাদের ভূমিকা রয়েছে।উদ্ভিদে এর ক্রিয়াবলি নিয়ে উপর্যুপরি গবেষণা চলছে।

# বহুনির্বাচনী প্রশ্ন
ক্যালশিয়াম হচ্ছে Ca প্রতীকযুক্ত একটি মৌলিক পদার্থ, যার পারমাণবিক সংখ্যা ২০। ক্যালসিয়াম একটি ক্ষারীয় ধাতব পদার্থ। এজন্য ক্যালসিয়াম বেশ সক্রিয় ধাতু, যা বায়ুর সংস্পর্শে আসার পরে গাঢ় অক্সাইড-নাইট্রাইড স্তর গঠন করে। এর গাঠনিক ও রাসায়নিক বৈশিষ্ট্যগুলির অধিকাংশই মিলে যায় এর চেয়ে কিছু ভারি ও সদৃশ মৌল স্ট্রনশিয়াম এবং বেরিয়ামের সাথে। পরিমাণের দিক থেকে এটি পৃথিবীর ভূত্বকের উপাদানগুলোর ভেতরে পঞ্চম অবস্থানে আছে। একইসাথে প্রাচুর্যের দিক থেকে পৃথিবীতে প্রাপ্ত ধাতুসমূহের ভেতরে এটি তৃতীয় অবস্থানে আছে, অর্থাৎ লোহা এবং অ্যালুমিনিয়ামের পরই এর অবস্থান। পৃথিবীতে সর্বাধিক পরিমাণে পাওয়া যায় এমন ক্যালসিয়াম যৌগটি হলো ক্যালসিয়াম কার্বোনেট, যা চুনাপাথর নামে পরিচিত। এটি সমুদ্রে প্রাপ্ত জীবাশ্মের অবশিষ্টাংশে পাওয়া যায়, যে জীবাশ্মগুলো সৃষ্ট হয়েছিলো সমুদ্র সৃষ্টির প্রারম্ভিক সময়ে। এর পাশাপাশি জিপসাম, অ্যানহাইড্রাইট, ফ্লোরাইট এবং অ্যাপাটাইট ক্যালসিয়ামের উৎস। ক্যালসিয়াম নামটি লাতিন শব্দ Calx Lime থেকে এসেছে। তৎকালে চুনাপাথরকে উত্তপ্ত করলে এটি পাওয়া যেত।

# বহুনির্বাচনী প্রশ্ন
দস্তা বা জিংক হলো একটি মৌলিক পদার্থ, যার প্রতীক Zn এবং পারমাণবিক সংখ্যা ৩০। এর পারমাণবিক ভর ৬৫.৩৮ (সাধারণ কাজে ৬৫ ব্যবহার করা হয়)। এটি পর্যায় সারণীর চতুর্থ পর্যায়ে, দ্বাদশ গ্রুপে অবস্থিত। এটি একটি ডি-ব্লক মৌল হলেও এর d-অরবিটাল পূর্ণ থাকায় এটি সাধারণত অবস্থান্তর ধাতু হিসেবে বিবেচিত হয়না। গ্যালভানাইজিং করতে প্রচুর পরিমাণে জিঙ্ক ব্যবহৃত হয়।
জিংক বর্ণালী
পিতল, বিভিন্ন অনুপাতে তামা এবং দস্তার মিশ্রণ, খ্রিস্টপূর্ব তৃতীয় সহস্রাব্দের আগে এজিয়ান, ইরাক, সংযুক্ত আরব আমিরাত, কাল্মেকিয়া, তুর্কমেনিস্তান ও জর্জিয়ায় এবং দ্বিতীয় সহস্রাব্দে পশ্চিম ভারত, উজবেকিস্তান, ইরান, সিরিয়া, ইরাক এবং প্যালেস্তাইনে ব্যবহৃত হয়েছে।

# বহুনির্বাচনী প্রশ্ন
লোহা বা লৌহ একটি ধাতব মৌলিক পদার্থ। এর রাসায়নিক চিহ্ন Fe, পারমাণবিক সংখ্যা ২৬, পারমাণবিক ভর ৫৫.৮৫, যোজ্যতা ২ ও ৩। লোহার ঘনত্ব ৭.৮৫ গ্রাম/সিসি অর্থাৎ জলের থেকে ৭.৮৫ গুণ ভারি। এর গলনাঙ্ক ১৫৩৮° সেলসিয়াস এবং স্ফুটনাঙ্ক ২৮৬২° সেলসিয়াস। লোহাকে প্রকৃতিতে মুক্ত অবস্থায় পাওয়া যায় না। আকরিক থেকে লোহা নিষ্কাশন করা হয়। লোহার প্রধান আকরিকগুলি হলো, হেমাটাইট (Hematite, Fe2O3), ম্যাগনেটাইট (Magnetite, Fe3O4), আয়রন পাইরাইটিস (Iron Pyrites, FeS2) ও সিডারাইট (Siderite,FeCO3), লিমোনাইট (Fe2O3.3H2O)। পৃথিবীর বিভিন্ন স্থানে প্রচুর লোহার আকরিক পাওয়া যায়। ভূ-ত্বকে লোহার পরিমাণ শতকরা ৪.১২ ভাগ।

# বহুনির্বাচনী প্রশ্ন
পারদ (Mercury)
সর্বাপেক্ষা নিম্ন গলনাঙ্কবিশিষ্ট ধাতু পারদ। এটি স্বাভাবিক তাপমাত্রায় তরল অবস্থায় থাকে। তরল পদার্থগুলোর মধ্যে পারদ সর্বাপেক্ষা ভারী। পারদের প্রতীক Hg । থার্মোমিটারে পারদ রহুলভাবে ব্যবহৃত হয় কারণ অল্প তাপে পারদের আয়তন অনেক বেশি বৃদ্ধি পায়। ফলে তাপমাত্রার সহজে সূক্ষ্মভাবে মাপা যায়।
জেনে রাখা ভাল
১. সোডিয়াম পোড়ালে উজ্জ্বল হলুদ বর্ণের শিখা উৎপন্ন হয়।
২. বৈদ্যুতিক বাল্বের ফিলামেন্টে টাংস্টেন ব্যবহৃত হয়।
৩. বিশুদ্ধ সোনা ২৪ ক্যারেট।
# বহুনির্বাচনী প্রশ্ন
দুই বা ততোধিক ধাতু পরস্পরের সাথে মিশে যে সমসত্ব বা অসমসত্ব মিশ্রণ উৎপন্ন করে, সেই কঠিন ধাতব পদার্থকে সংকর ধাতু (Alloy) বলে। যেমন: কাঁসা হলো কপার ও টিনের সংকর ধাতু।
সংকর ধাতু | মিশ্রণ |
| ঢালাই লোহা বা কাস্ট আয়রন | লোহার সাথে ২-৪.৫৬% কার্বন থাকে। একে পিগ আয়রনও বলে। |
| ইস্পাত (Steel) | লোহার সাথে সুনিয়ন্ত্রিত পরিমাণ কার্বন থাকে। এতে কার্বনের শতকরা পরিমাণ ০.১৫ - ১.৫%। |
| স্টেইনলেস স্টিল Stainless Stell | লোহা (Fe)- ৭৩% + ক্রোমিয়াম (Cr) ১৮% + নিকেল (Ni)- ৮% + কার্বন (C)- ১% |
| ব্রোঞ্জ (Bronze) | ৯০% তামা + ১০% টিন |
| পিতল (Brass) | তামা ৮০% + দস্তা (জিঙ্ক) - ২০% |
| গান মেটাল | তামা ৮৮% + ১০% টিন+ দস্তা (জিঙ্ক) - ২% |
| ডুরালামিন | অ্যালুমিনিয়ামের সাথে মেশানো হয় কপার, ম্যাগনেসিয়াম এবং ম্যাঙ্গানিজ। |
| নাইক্রোম | নিকেল-৬০% + আয়রন-২৫% + ক্রোমিয়াম-১৫% |
| বৈদ্যুতিক ইস্ত্রি এবং হিটারে নাইক্রোম তার ব্যবহার করা হয়। | |
| টাইপ মেটাল | সীসা ৭৫% + অ্যান্টিমনি ২০% + টিন ৫% |
# বহুনির্বাচনী প্রশ্ন
টিন
লোহা
রূপা
দস্তা
বহুরূপতা
প্রকৃতিতে একই মৌলের বিভিন্ন ভৌত রূপে অবস্থান করার প্রবণতাকে বহুরূপতা বলে। কার্বন, ফসফরাস, সিলিকন, সালফার, জার্মেনিয়াম, নাইট্রোজেন, অক্সিজেন, টিন, বোরন ইত্যাদি মৌল বহুরূপতা প্রদর্শণ করে।
ক্যাটেনেশন
একই মৌলের পরমাণুসমূহের মধ্যে বন্ধন সৃষ্টির মাধ্যমে বিভিন্ন দৈর্ঘ্যের শিকল গঠনের ধর্মকে ক্যাটেনেশন বলা হয়। ক্যাটেনেশন ধর্ম দ্বারা কার্বন পরমাণুসমূহ নিজেদের মধ্যে একক বন্ধন, দ্বিবন্ধন বা ত্রিবন্ধন দ্বারা বিভিন্ন দৈর্ঘ্যের কার্বন পরমাণু শিকল ও বলয় গঠন করে বিভিন্ন জৈব যৌগ সৃষ্টি করতে পারে। এজন্য জৈব যৌগের সংখ্যা ২০ লক্ষাধিক। অজৈব যৌগের মধ্যে শুধুমাত্র সিলিকনে কিছুটা ক্যাটেনেশন দেখা যায়।
কার্বন (কার্বনের বহুমুখী ব্যবহার)
কার্বন অধাতু এবং বিজারক। কাঠ ও কয়লা প্রধানত কার্বন। আবার, হীরক এবং গ্রাফাইট হলো কার্বনের দুটি রূপভেদ। প্রকৃতিতে প্রাপ্ত সবচেয়ে কঠিন পদার্থ হীরক। হীরক কাঁচ কাটতে ব্যবহৃত হয়। হীরক বিদ্যুৎ অপরিবাহী কারণ এতে কোনো মুক্ত ইলেকট্রন থাকে না। গ্রাফাইট অধাতু হলেও তাপ ও বিদ্যুৎ পরিবহনে সক্ষম। বিভিন্ন গ্রেডের (2B, HB, 2H, HH) উড পেন্সিলের 'সীস' হিসেবে গ্রাফাইট ব্যবহৃত হয়। এছাড়াও সোডিয়াম ধাতুর নিষ্কাশনে গ্রাফাইট অ্যানোড হিসেবে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
চিনি
নিয়ন
লবণ
পানি
অধাতু সাধারণত ভঙ্গুর, তাপ ও বিদ্যুৎ অপরিবাহী এবং আঘাত করলে কোনো শব্দ উৎপন্ন করে না। এগুলো চকচকে হয় না, কম গলনাঙ্ক ও স্ফুটনাঙ্কবিশিষ্ট, এবং কঠিন, তরল বা গ্যাসীয় অবস্থায় থাকতে পারে । এরা ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে (অ্যানায়ন) পরিণত হয় এবং তাদের অক্সাইডগুলো সাধারণত অম্লীয় প্রকৃতির হয়।
# বহুনির্বাচনী প্রশ্ন
কার্বন (কার্বনের বহুমুখী ব্যবহার)
কার্বন অধাতু এবং বিজারক। কাঠ ও কয়লা প্রধানত কার্বন। আবার, হীরক এবং গ্রাফাইট হলো কার্বনের দুটি রূপভেদ। প্রকৃতিতে প্রাপ্ত সবচেয়ে কঠিন পদার্থ হীরক। হীরক কাঁচ কাটতে ব্যবহৃত হয়। হীরক বিদ্যুৎ অপরিবাহী কারণ এতে কোনো মুক্ত ইলেকট্রন থাকে না। গ্রাফাইট অধাতু হলেও তাপ ও বিদ্যুৎ পরিবহনে সক্ষম। বিভিন্ন গ্রেডের (2B, HB, 2H, HH) উড পেন্সিলের 'সীস' হিসেবে গ্রাফাইট ব্যবহৃত হয়। এছাড়াও সোডিয়াম ধাতুর নিষ্কাশনে গ্রাফাইট অ্যানোড হিসেবে ব্যবহৃত হয়।
কার্বন ডাই অক্সাইড (CO2)
কার্বন ডাই অক্সাইড একটি এসিডধর্মী গ্যাস। পানিতে কার্বন ডাই অক্সাইডের দ্রবণকে সোডা ওয়াটার বলে। কার্বন ডাই অক্সাইড গ্যাসকে অত্যধিক চাপে তরল করে সোডা ওয়াটার তৈরি করা হয়। আবার হিমায়িত কঠিন কার্বন ডাই অক্সাইডকে শুষ্ক বরফ (Dry Ice) বলা হয়। অগ্নি নির্বাপক সিলিন্ডারে তরল কার্বন ডাই-অক্সাইড ব্যবহার করা হয়। রাসায়নিক অগ্নি নির্বাপক অগ্নিতে অক্সিজেন সরবরাহে প্রতিবন্ধকতা সৃষ্টি করে।
| গ্যাস | নিজে জ্বলে | অন্যকে জ্বলতে সাহায্য করে |
| কার্বন ডাই অক্সাইড | x | x |
| হাইড্রোজেন | ✓ | x |
| অক্সিজেন | x | ✓ |
কার্বন মনোক্সাইড (CO)
গাড়ি থেকে নির্গত কালো ধোঁয়ায় বিষাক্ত কার্বন মনোক্সাইড গ্যাস থাকে। কার্বন মনোক্সাইড হিমোগ্লোবিনের অক্সিজেন পরিবহন ক্ষমতা হ্রাস করে।
গ্যাস | রাসায়নিক নাম | সংকেত |
| ওয়াটার গ্যাস | কার্বন মনোক্সাইড ও হাইড্রোজেন গ্যাস | CO + H2 |
| প্রোডিউসার গ্যাস | কার্বন মনোক্সাইড ও নাইট্রোজেন গ্যাস | 2CO + N2 |
# বহুনির্বাচনী প্রশ্ন
সোডিয়াম
এলুমিনিয়াম
ক্যালসিয়াম
কার্বন
অক্সিজেন (O)
বৃটিশ যাজক যোসেফ প্রিস্টলি সর্বপ্রথম ১৭৭৪ খ্রিস্টাব্দে অক্সিজেন আবিষ্কার করেন। অক্সিজেনের একটি বিশেষ ধর্ম হল ইহা নিজে জ্বলেনা কিন্তু অন্যকে জ্বলতে সাহায্য করে। যে পানিতে কঠিন বস্তু (লবণ) বেশি দ্রবীভূত থাকে সে পানিতে অক্সিজেনের পরিমাণ কম। যেমন: সমুদ্রের পানিতে কঠিন বস্তু (লবণ) দ্রবীভূত থাকে কিন্তু নদীর পানিতে থাকে না। ফলে সমুদ্রের পানি, ভূগর্ভস্থ পানির তুলনায় নদীর পানিতে অক্সিজেনের পরিমাণ বেশি। হাসপাতালে ব্যবহৃত অক্সিজেনে অক্সিজেনের পরিমাণ শতকরা ৯৩ ভাগ। বায়ুমণ্ডলে অক্সিজেনের পরিমাণ ২১.০১%। ওজোন (O3) অক্সিজেনের একটি রূপভেদ। বায়ুমণ্ডলে ওজোনের পরিমাণ ০.০০০১%, ওজোনের রং গাঢ় নীল।
# বহুনির্বাচনী প্রশ্ন
অক্সিজেন
কার্বনডাইঅক্সাইড
নাইট্রোজেন
হাইড্রোজেন
সাদা
হলুদ
ধূসর
বর্ণহীন
নাইট্রোজেন (N)
আকাশে বিদ্যুৎ ক্ষরণের ফলে নাইট্রোজেনের অক্সাইডসমূহ তৈরি হয়, যা পানির সাথে মিশে নাইট্রিক এসিড উৎপন্ন করে। এ নাইট্রিক এসিড বৃষ্টির পানির সাথে মিশে মাটিতে পতিত হয় এবং জমির ক্ষারীয় উপাদানের সাথে বিক্রিয়া করে নাইট্রেট লবণ উৎপন্ন করে। উদ্ভিদ এ নাইট্রেট গ্রহণ করে তাকে প্রোটিনে রূপান্তরিত করে, যা প্রাণিসকল গ্রহণ করে। উদ্ভিদ ও প্রাণির জীবন অবসানের পর পচন ক্রিয়ায় প্রোটিনের কিছু অংশ নাইট্রোজেন গ্যাসে পরিণত হয়। এভাবে প্রকৃতিতে "নাইট্রোজেন চক্র" চলে।
# বহুনির্বাচনী প্রশ্ন
ফসফরাস (P)
ফসফরাসের দুটি রূপভেদ আছে। যথা- লোহিত ফসফরাস ও শ্বেত ফসফরাস। শ্বেত ফসফরাস বেশি সক্রিয়। শ্বেত ফসফরাসের গন্ধ রসুনের মত। দিয়াশলাইয়ের কাঠির মাথায় লোহিত ফসফরাস ব্যবহৃত হয়। দিয়াশলাইয়ের বক্সের দু-ধারে কাগজের উপর যে বারুদ থাকে তা আসলে কাঁচচূর্ণ মিশ্রিত ফসফরাস। ফসফরাস পেন্টাক্সাইড (P2O5) নিরুদক হিসেবে ব্যবহৃত হয়। গ্যাস মাস্কের প্রধান উপাদান ফসফরাস পেন্টাক্সাইড।
# বহুনির্বাচনী প্রশ্ন
সিলিকন (Si)
সিলিকার রাসায়নিক নাম সিলিকন ডাই অক্সাইড (SiO2)। সিলিকার বিশুদ্ধ রূপ কোয়ার্টজ। কোয়ার্টজ ঘড়িতে সিলিকা ব্যাপকভাবে ব্যবহৃত হয়। কাচ তৈরির প্রধান কাঁচামাল হলো বালি। বালির প্রধান উপাদান হলো সিলিকা। কাচ রাসায়নিকভাবে অত্যন্ত নিষ্ক্রিয়। কাঁচ বহুদিন রোদে বা পানিতে থাকলে নষ্ট, ক্ষয় বা বৃদ্ধি হয় না।
হ্যালোজেন শব্দের অর্থ 'সামুদ্রিক লবণ উৎপাদক'। হ্যালোজেন বলতে ফ্লোরিন (F2), ক্লোরিন (Cl2), ব্রোমিন (Br2) এবং আয়োডিন (I2) এ চারটি মৌলকেই বোঝায়। সামুদ্রিক শৈবালে আয়োডিন পাওয়া যায়। পান করা পানির সাথে ক্লোরিন মিশানো হয় কারণ ক্লোরিন পানিতে থাকা ক্ষতিকর ব্যাক্টেরিয়া ধ্বংস করে। হ্যালোজেন এসিড শক্তির ক্রম: HI > HBr > HCI > HF পর্যায় সারণিতে হ্যালোজেনগুলোর VIIA গ্রুপে অবস্থান করে।
নিষ্ক্রিয় গ্যাস (Noble Gas): পর্যায় সারণির শূন্য গ্রুপের মৌলসমূহ রাসায়নিকভাবে নিষ্ক্রিয় এবং কক্ষ তাপমাত্রায় গ্যাসীয়। এদের নিষ্ক্রিয় গ্যাস বলে। নিষ্ক্রিয় গ্যাস ৭টি যথা- হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Kr), জেনন (Xe) এবং রেডন (Rn) এবং ওগানেসন । নিষ্ক্রিয় গ্যাসমূহের সর্ববহিঃস্থ স্তরে ৮টি ইলেকট্রন থাকে। ব্যতিক্রম হিলিয়াম। হিলিয়ামের সর্ববহিঃস্থ স্তরে ২টি ইলেকট্রন থাকে। সূর্যে মৌলিক পদার্থের মধ্যে হিলিয়াম (He) এর পরিমাণ সবচেয়ে বেশি। রেডন তেজষ্ক্রিয় মৌল। বিজ্ঞানী ডর্ন ১৯০০ সালে রেডিয়ামের তেজষ্ক্রিয় বিভাজন হতে রেডন আবিষ্কার করেন।
নিষ্ক্রিয় গ্যাসের সংখ্যা সাত। এগুলো হল: হিলিয়াম, নিয়ন, আর্গন, ক্রিপ্টন, জেনন, র্যাডন এবং ওগানেসন। একে নোবেল গ্যাস বলা হয় ।
ব্যবহার
(১) হাইড্রোজেন হিলিয়াম অপেক্ষা হালকা হলেও হাইড্রোজেন দাহ্য পক্ষান্তরে হিলিয়াম নিষ্ক্রিয়। এজন্য বেলুনে এবং ডুবুরিদের জন্য হাইড্রোজেনের পরিবর্তে হিলিয়াম ব্যবহার করা হয়।
(২) ফটোগ্রাফিক ফ্লাশ লাইটে জেনন গ্যাস ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
সালফিউরিক এসিড (H2SO4)
সালফিউরিক এসিডের একটি অণুতে মোট ৭টি (২টি হাইড্রোজেন, ১টি সালফার, ৪টি অক্সিজেন) পরমাণু থাকে। ১০০% বিশুদ্ধ সালফিউরিক এসিডকে সালফান এবং ধূমায়মান সালফিউরিক এসিডকে ওলিয়াম (H2S2O7) বলে। সালফিউরিক এসিড রাসায়নিক পদার্থসমূহের রাজা বলা হয় কারণ প্রায় প্রত্যেক শিল্পে কোনো না কোনো স্তরে H2SO4 এসিড ব্যবহৃত হয়।
হাইড্রোজেন সালফাইড (H2S)
হাইড্রোজেন সালফাইড বর্ণহীন, পঁচা ডিমের গন্ধযুক্ত একটি গ্যাস। এটি পানিতে খুব সামান্য পরিমাণে দ্রবীভূত হয়। ১৭৭৭ সালে সুইডিশ রসায়নবিদ কার্ল উইলহেম শিলি হাইড্রোজেন সালফাইড আবিষ্কার করেন।
নাইট্রিক এসিড (HNO3)
স্বর্ণ থেকে খাদ বের করতে নাইট্রিক এসিড ব্যবহার করা হয়। এক মোল গাঢ় নাইট্রিক এসিড (HNO3) এবং তিন মোল গাঢ় হাইডোক্লোরিক এসিডের (HCI) মিশ্রণকে অ্যাকোয়া রেজিয়া বা রাজ-অম্ল বলে। স্বর্ণ, প্লাটিনাম প্রভৃতি অভিজাত ধাতুসমূহ যে কোনো গাঢ়তার হাইড্রোক্লোরিক এসিড বা নাইট্রিক এসিডে দ্রবীভূত হয় না, কিন্তু এরা অ্যাকোয়া রেজিয়া বা রাজ অম্লে দ্রবীভূত হয়। 96-98% ঘনমাত্রার নাইট্রিক এসিডে অধিক নাইট্রোজেন ডাই অক্সাইড (NO2) দ্রবীভূত থাকে। NO2 গ্যাস বের হয়ে বায়ুতে ধোয়া উৎপন্ন করে। তাই এই ঘনমাত্রার নাইট্রিক এসিডকে ধূমায়মান নাইট্রিক এসিড বলে।
নাইট্রোজেন অক্সাইড
নাইট্রাস অক্সাইড (N2O) এর মৃদু মিষ্টি গন্ধ আছে। নিশ্বাসের সাথে এটি অল্প পরিমাণ গ্রহণ করলে হাসির উদ্রেক করে। এজন্য একে লাফিং গ্যাস বলে। মৃদু চেতনানাশকরূপে N₂O ব্যবহার করা হয়।
এসিড বৃষ্টি (Acid Rain)
শিল্প সমৃদ্ধ এলাকায় সাধারণত এসিড বৃষ্টি দেখা যায়। বায়ুতে শিল্প কারখানা হতে নির্গত সালফার ডাই অক্সাইড (প্রধানত), নাইট্রোজেনের বিভিন্ন অক্সাইড এবং সালফিউরিক এসিড বাষ্প বেশি থাকলে বৃষ্টির সময় ঐ এসিড বাষ্প পানির সাথে যুক্ত হয়ে এসিড বৃষ্টির সৃষ্টি করে। এসিড বৃষ্টির ফলে পরিবেশের ব্যাপক ক্ষতি হয়।
যেসব যৌগ জলীয় দ্রবণে আংশিক বা সম্পূর্ণরূপে বিয়োজিত হয়ে হাইড্রোজেন আয়ন (H+) উৎপন্ন করে তাকে এসিড বলে।
উদাহরণ- সালফিউরিক এসিড, সাইট্রিক এসিড, কার্বলিক এসিড।
যে সকল ক্ষারক পানিতে দ্রবীভূত হয় তাকে ক্ষার বলে।
যেমনঃ ক্যালসিয়াম হাইড্রোক্সাইড [Ca(OH)2], সোডিয়াম হাইড্রোক্সাইড [NaOH]
এসিড ও ক্ষারকের বিক্রিয়ায় যে নিরপেক্ষ পদার্থ উৎপন্ন হয় তাকে লবন বলে।
উদাহরণ- সোডিয়াম ক্লোরাইড [NaCl], ক্যালসিয়াম ক্লোরাইড [CaCl2]
# বহুনির্বাচনী প্রশ্ন
0.4 g
4 g
0.8 g
10 g
এসিড (Acid)
যদি কোনো যৌগের অণুতে এক বা একাধিক প্রতিস্থাপনীয় হাইড্রোজেন পরমাণু থাকে এবং ঐ প্রতিস্থাপনীয় হাইড্রোজেন পরমাণু কোনো ধাতু বা ধাতুর ন্যায় ক্রিয়াশীল কোনো যৌগমূলক দ্বারা আংশিক বা সম্পূর্ণরূপে প্রতিস্থাপিত করা যায় এবং যা ক্ষারকের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে, তাকে অম্ল (Acid) বলে। অন্যভাবে বলা যায়, যে যৌগ বা আয়ন অন্য পদার্থকে প্রোটন দান করতে পারে, তাকে অম্ল (Acid) বলে। এসিডের স্বাদ টক। উদাহরণ: সালফিউরিক এসিড (H2SO4), নাইট্রিক এসিড (HNO3) ইত্যাদি।
# বহুনির্বাচনী প্রশ্ন
ক্ষারক ও ক্ষার (Base & Alkali)
ধাতুর অক্সাইড ও হাইড্রোক্সাইডকে ক্ষারক বলে। অন্যভাবে বলা যায়, যে যৌগ বা আয়ন অম্ল হতে প্রোটন গ্রহণ করতে পারে, তাই ক্ষারক। উদাহরণ: সোডিয়াম হাইড্রোক্সাইড (NaOH), ম্যাগনেশিয়াম হাইড্রোক্সাইড (MgOH)। অধিকাংশ ক্ষারকই পানিতে দ্রবীভূত হয় না। যে সকল ক্ষারক পানিতে দ্রবীভূত হয়, তাকে ক্ষার বলে। উদাহরণ: সোডিয়াম হাইড্রোক্সাইড (NaOH). পটাসিয়াম হাইড্রোক্সাইড (KOH) ইত্যাদি।
| PH | দ্রবণ |
| =7 | নিরপেক্ষ |
| <7 | অম্লীয় |
| >7 | ক্ষারীয় |
PH
কোনো দ্রবণের হাইড্রোজেন আয়নের (H+) মোলার ঘনমাত্রার ঋণাত্মক লগারিদমকে ঐ দ্রবণের PH বলে অর্থ্যাৎ PH = -log[H+] । PH হলো এসিডীয় মাত্রা, ক্ষারকীয় মাত্রা এবং নিরপেক্ষতা নিদের্শক। PH স্কেলের রেঞ্জ ০-১৪।
বিভিন্ন পদার্থের PH এর মান
পদার্থ | PH এর মান | পদার্থ | PH এর মান |
| বিশুদ্ধ পানি | ৭ | চোখের পানি | ৪.৮০~৭.৫০ |
| মানুষের রক্ত | ৭.৩৫- ৭.৪৫ | মূত্র | ৪.৮০~৭.৫০ |
বাফার
যে দ্রবণ নিজস্ব PH স্থির রাখার ক্ষমতা রাখে, তাকে বাফার দ্রবণ বলে। হেন্ডারসন সমীকরণের দ্বারা বাফারের PH এর মান গণনা করা হয়।
নির্দেশক
যে সব যৌগ নিজেদের বর্ণ পরিবর্তনের কোন দ্রবণ অম্লীয় বা ক্ষারীয় তা নির্দেশ করে, তাদের নির্দেশক বলে।
| নির্দেশক | অম্লীয় মাধ্যমে বর্ণ | ক্ষারীয় মাধ্যমে বর্ণ |
| লিটমাস | লাল | নীল |
| ব্রোমোফেনল | হলুদ | নীল |
| মিথাইল অরেঞ্জ | লাল | হলুদ |
# বহুনির্বাচনী প্রশ্ন
১৬%
২০%
২৫%
৩০%
লবণ (Salt)
"লবণ" শব্দটি সাধারণত রসায়নে একটি আয়নিক যৌগ বা খাদ্য লবণ (যেমন সোডিয়াম ক্লোরাইড) কে বোঝায়। রসায়নে, লবণ হল অ্যাসিড এবং ক্ষারকের মধ্যে বিক্রিয়ার ফলে উৎপন্ন একটি পদার্থ। খাদ্য লবণ, যা টেবিল লবণ নামেও পরিচিত, এটি সোডিয়াম ক্লোরাইড (NaCl)। এটি খাবারকে লবণাক্ত করতে এবং খাদ্য সংরক্ষণে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
পানির খরতা
যে পানি সাবানের সাথে সহজে ফেনা উৎপন্ন করে না, অনেক সাবান খরচ করার পর ফেনা উৎপন্ন করে, তাকে খর পানি বলে। খর পানিতে সাবান ফেনা না দিলেও ডিটারজেন্ট উত্তম ফেনা দেয়। পানির খরতা দুই প্রকার। যথা: অস্থায়ী খরতা এবং স্থায়ী খরতা।
খরতা | কারণ |
| অস্থায়ী | ক্যালসিয়াম বা ম্যাগনেসিয়ামের বাইকার্বনেট (HCO3-) লবণ |
| স্থায়ী | ক্যালসিয়াম বা ম্যাগনেসিয়ামের সালফেট (SO4-) বা ক্লোরাইড (Cl-) লবণ |
দূরীকরণ পদ্ধতি | বৈশিষ্ট্য |
| ফুটানো | শুধু অস্থায়ী খরতা দূর করা যায়। |
| পারমুটিট পদ্ধতি | স্থায়ী ও অস্থায়ী খরতা দূর করা যায়। |
| সোডা পদ্ধতি | স্থায়ী ও অস্থায়ী উভয় প্রকার খরতা কাপড় কাচা সোডা (Na2 CO3) এর সাহায্যে দূর করা যায়। |
খর পানি ব্যবহার করলে কারখানার বয়লারে, মোটর গাড়ির শীতক প্রকোষ্ঠে ও কেতলীর তলায় অদ্রবণীয় ও তাপ অপরিবাহী ক্যালসিয়াম কার্বনেট, ক্যালসিয়াম সালফেট প্রভৃতি লবণের আবরণ পড়ে। বয়লারের গায়ে অদ্রবণীয় লবণের স্তর পড়ার কারণে বয়লারের তাপ পরিবাহিতা কমে যায়। ফলে জ্বালানি অপচয় ঘটে।
মৃদু পানি (Soft Water)
যে পানি সাবানের সাথে সহজে ফেনা উৎপন্ন করে, তাকে মৃদু পানি বলে। প্রাকৃতিক উৎসগুলোর মধ্যে বৃষ্টি থেকে সবচেয়ে বেশি মৃদু পানি পাওয়া যায়।
# বহুনির্বাচনী প্রশ্ন
অডিওমিটার
অডিওফোন
ফ্যাদোমিটার
হাইড্রোফোন
একই থাকে
কমে
প্রথমে বাড়ে পরে কমে
বাড়ে
রাসায়নিক বিক্রিয়া (Chemical Actions)
যদি কোনো পরিবর্তনের ফলে কোনো পদার্থ তার নিজের ধর্ম ও বৈশিষ্ট্য হারিয়ে নতুন ধর্ম লাভ করে সেই পরিবর্তনকে রাসায়নিক পরিবর্তন বলে। যে প্রক্রিয়ায় রাসায়নিক পরিবর্তন ঘটে সেই প্রক্রিয়াকে রাসায়নিক বিক্রিয়া বলে। রাসায়নিক বিক্রিয়াকে সংক্ষেপে উপস্থাপন করার জন্য যে সমীকরণ ব্যবহার করা হয় সেই সমীকরণকে রাসায়নিক সমীকরণ বলা হয়।
রাসায়নিক সমীকরণকে প্রকাশ করার জন্য প্রতীক, সংকেত এবং নানা রকম চিহ্ন ব্যবহার করা হয়।
যে সকল পদার্থ নিয়ে রাসায়নিক বিক্রিয়া শুরু করা হয় সেই সকল পদার্থকে বলা হয় বিক্রিয়ক। বিক্রিয়ার ফলে নতুন ধর্ম বিশিষ্ট যে সকল পদার্থ উৎপন্ন হয় সেই সকল পদার্থকে উৎপাদ বলা হয়।
রাসায়নিক বিক্রিয়াকে রাসায়নিক সমীকরণ আকারে লেখার জন্য কতোগুলো নিয়ম মানা হয় সেগুলো হচ্ছে:
1. গণিতে যেমন সমীকরণের মাঝে একটি সমান চিহ্ন (=) ব্যবহার করা হয় তেমনি কোনো বিক্রিয়ার বিক্রিয়ক বাম পাশে এবং উৎপাদ ডান পাশে লিখে তাদের মাঝে একটি সমান চিহ্ন (=) বা তীর চিহ্ন (→) বসাতে হয়।
2. বিক্রিয়কসমূহ এবং উৎপাদসমূহকে রাসায়নিক প্রতীক বা সংকেতের মাধমে লেখা হয়। বিক্রিয়ায় একাধিক বিক্রিয়ক থাকলে বিক্রিয়কসমূহের মাঝে যোগ চিহ্ন দিতে হয়। এবং একাধিক উৎপাদ থাকলে উৎপাদসমূহের মাঝে যোগ চিহ্ন দিতে হয়।
3. যে প্রক্রিয়ায় সমীকরণের বাম পাশের বিভিন্ন মৌলের পরমাণুর সংখ্যা এবং ডান পাশের ঐ একই মৌলের পরস্পর সংখ্যা সমান করা হয়। সেই প্রক্রিয়াকে রাসায়নিক সমীকরণের সমতা বলা হয়।
2H2 + O2→ 2H2O
2H2 + O2 = 2H2O
4. কখনো কখনো বিক্রিয়ার সমতা না করেও বিক্রিয়া দেখানো হয়, তখন সমান চিহ্ন (=) না দিয়ে তীর চিহ্ন (→) ব্যবহার করতে হয়।
H2 + O2 → H2O
5. অনেক সময় বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা উল্লেখ করেও রাসায়নিক সমীকরণ লেখা হয়। বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা পদার্থের ডান পাশে প্রথম বন্ধনীর মধ্যে প্রকাশ করা হয় । এক্ষেত্রে কোনো পদার্থ কঠিন হলে তার ইংরেজি নাম (Solid) এর প্রথম বর্ণ (s) লিখতে হয়, কোনো পদার্থ তরল (liquid) হলে তার ইংরেজি নামের প্রথম বর্ণ লিখতে হয়, কোনো পদার্থ গ্যাসীয় তার ইংরেজি নাম (gas) এর প্রথম বর্ণ (g) লিখতে হয়। কোনো পদার্থ পানিতে দ্রবীভূত হলে সেই দ্রবণকে বলা হয় জলীয় দ্রবণ। জলীয় দ্রবণের ইংরেজি নাম (aquas solution ) এর প্রথম 2টি বর্ণ (aq) লিখতে হয়। উপরের বিক্রিয়ায় হাইড্রোজেন ও অক্সিজেন গ্যাস এবং উৎপন্ন পদার্থ পানি তরল তাই তাকে লিখতে হবে।
2H2(g) + O2(g) → 2H2O(1)
রাসায়নিক সমীকরণ এর উদ্দেশ্য হচ্ছে কোন কোন পদার্থ বিক্রিয়া করে কোন কোন পদার্থ হয়েছে সেটি দেখানো। অনেক সময় সমতা না করেও সেটি দেখানো যেতে পারে।
6. তবে যদি কোনো বিক্রিয়ায় কতটুকু তাপ উৎপন্ন হয় বা কতটুকু তাপ শোষিত হয় তা সমীকরণে দেখাতে হয় তবে সেক্ষেত্রে রাসায়নিক বিক্রিয়ার সমতা করতে হবে এবং বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা (যেমন কঠিন, তরল, গ্যাসীয় অবস্থা, জলীয় অবস্থা ইত্যাদি) লিখতে হবে।
# বহুনির্বাচনী প্রশ্ন
তামা
দস্তা
রূপা
এলুমিনিয়াম
নাপাম
নিউট্রন
হাইড্রোজেন
এটম
একই পদার্থের অসংখ্য অণু বা একাধিক পদার্থের অসংখ্য অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ অণু গঠন করার প্রক্রিয়াকে পলিমারকরণ বলে। এই বিক্রিয়ায় উৎপন্ন বৃহৎ অণুকে পলিমার এবং বিক্রিয়ক অসংখ্য ক্ষুদ্র অণুর প্রত্যেকটিকে মনোমার বলে। একই বিক্রিয়কের অসংখ্য অণু যুক্ত হয়ে পলিমার গঠন করার প্রক্রিয়াকে যুত পলিমারকরণ (Addition Polymerisation) বলে।
যুত পলিমারকরণ বিক্রিয়া-
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুসমূহ পরস্পরের সাথে যুক্ত হওয়ার সময় ক্ষুদ্র ক্ষুদ্র অণু যেমন- ইত্যাদি অপসারণ করে সেই পলিমারকরণ বিক্রিয়াকে ঘনীভবন পলিমারকরণ বলে।
জারণ ও বিজারণ (Oxidation & Reduction)
জারণ (Oxidation)
যে বিক্রিয়ায় কোনো মৌল বা যৌগে তড়িৎ ঋণাত্মাক পরমাণু বা মূলক সংযুক্ত হয় বা তাদের অনুপাত বৃদ্ধি পায় অথবা কোনো তড়িৎ ধনাত্মক পরমাণু বা মূলকের অপসারণ হয় বা তাদের অনুপাত হ্রাস পায়, সেই বিক্রিয়াকে জারণ বলে।
ইলেকট্রনীয় ধারণা: যে বিক্রিয়ায় কোনো রাসায়নিক সত্তা (অণু, পরমাণু, মূলক বা আয়ন) ইলেকট্রন প্রদান করে, তাকে জারণ বলে।
যেমন: Na → Na+ + e- (ইলেকট্রন দান বা জারণ)
বিজারণ (Reduction)
যে বিক্রিয়ার কোনো মৌল বা যৌগে তড়িৎ ধনাত্মক পরমাণু বা মূলক সংযুক্ত হয় বা তাদের অনুপাত বৃদ্ধি পায় অথবা কোনো তড়িৎ ঋণাত্মক পরমাণু বা মূলকের অপসারণ হয় বা তাদের অনুপাত হ্রাস পায়, সেই বিক্রিয়াকে বিজারণ বলে।
ইলেকট্রনীয় ধারণা: যে বিক্রিয়ায় কোন রাসায়নিক সত্তা (অণু, পরমাণু, মূলক বা আয়ন) ইলেকট্রন গ্রহণ করে, তাকে বিজারণ বলে।
যেমন: Cl + e- → Cl- (ইলেকট্রন গ্রহণ বা বিজারণ)
যে বস্তু অন্য কোনো বস্তুর বিজারণ ঘটায় এবং নিজে জারিত হয়, তাকে বিজারক বলে। যেমন: সকল ধাতু, হাইড্রোজেন, কার্বন প্রভৃতি। বিজারক পদার্থ ইলেকট্রন বর্জন করে।
যে বস্তু অন্য কোনো বস্তুর জারণ ঘটায় 'এবং নিজে বিজারিত হয়, তাকে জারক বলা হয়। যেমন: অক্সিজেন, ফ্লোরিন, ক্লোরিন, ব্রোমিন, আয়েডিন, পটাসিয়াম ডাইক্রোমেট, পটাসিয়াম পারম্যাঙ্গানেট, HNO3, উত্তপ্ত গাঢ় H2SO4, পার অক্সাইডসমূহ, পার অক্সি এসিডসমূহ এবং তাদের লবণসমূহ।। জারক পদার্থসমূহ ইলেকট্রন গ্রহণ করে।
# বহুনির্বাচনী প্রশ্ন
তড়িৎ কোষ (Electric Cell)
যে যন্ত্রের সাহায্যে রাসায়নিক শক্তি থেকে নিরবিচ্ছিন্নভাবে তড়িৎ শক্তি পাওয়া যায় তাকে তড়িৎ কোষ বলে। তড়িৎ কোষ দুই প্রকার। যথা:
(ক) তড়িৎ রাসায়নিক কোষ বা গ্যালভানিক সেল: যে কোষে রাসায়নিক বিক্রিয়া হতে বিদ্যুৎ উৎপন্ন হয়, তাকে তড়িৎ রাসায়নিক কোষ বলে। তড়িৎ রাসায়নিক কোষ আলেকসান্দ্রো ভোল্টা আবিষ্কার করেন।
(খ) তড়িৎ বিশ্লেষ্য কোষ: যে পাত্রে তড়িৎ বিশ্লেষণ চালানো হয়, তাকে তড়িৎ বিশ্লেষ্য কোষ বলা হয়। তড়িৎ বিশ্লেষ্য কোষে ধনাত্মক তড়িৎদ্বারকে অ্যানোড এবং ঋণাত্মক তড়িৎদ্বারকে কে ক্যাথোড বলে।
# বহুনির্বাচনী প্রশ্ন
শুষ্ক কোষ (Dry Cell)
শুষ্ক কোষ একটি প্রাথমিক কোষ বা প্রাইমারি সেল। সাধারণ ড্রাইসেলে ইলেকট্রোড হিসাবে কার্বন দণ্ড (+) এবং দস্তার কৌটা (-) ব্যবহৃত হয়। শুষ্ক কোষে কার্বন দণ্ড ইলেকট্রন দান করে। কার্বন দণ্ডের চারপার্শ্বে কঠিন ম্যাঙ্গানিজ ডাই-অক্সাইড (MnO2) এবং কার্বন গুড়ার মিশ্রণ থাকে। এর চারপার্শ্বে অ্যামোনিয়াম ক্লোরাইডের (NH4CI) এর পেস্ট থাকে। NH4CI বিদ্যুৎ উত্তেজক হিসাবে এবং MnO2 ছদন নিবারক হিসাবে কাজ করে। বাজারে এটি ব্যাটারি নামে পরিচিত। ব্যাটারি থেকে আমরা D.C বিদ্যুৎ পাই। শুষ্ক কোষ একমুখী (DC) তড়িৎ প্রবাহ উৎপন্ন করে। এর তড়িচ্চালক বল ১.৫ ভোল্ট।
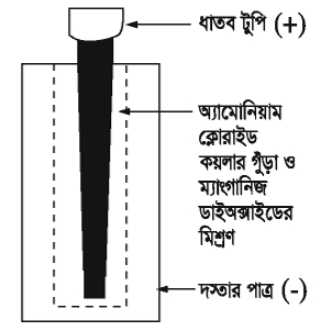
স্টোরেজ ব্যাটারি (Storage Battery)
গাড়িতে ব্যবহৃত এ সকল ব্যাটারিতে সীসার ইলেকট্রোডের সঙ্গে তড়িৎ বিশ্লেষ্য রূপে সালফিউরিক এসিড (H2SO4) ব্যবহৃত হয়।
জৈব রসায়ন (Organic Chemistry)
কার্বন শিকল দ্বারা গঠিত বিভিন্ন যৌগের রসায়নকে জৈব রসায়ন বলে। অন্যভাবে বলা যায় যে, রসায়নের যে শাখায় হাইড্রোকার্বন ও হাইড্রোকার্বনের বিভিন্ন জাতক সম্বন্ধে আলোচনা করা হয়, তাকে জৈব রসায়ন বলে।
# বহুনির্বাচনী প্রশ্ন
এটি একটি রাসায়নিক তরল পদার্থ
এটি একটি কাল্পনিক মাধ্যম যা মহাবিশ্বে সর্বত্র বিরাজমান ছিল
এ মাধ্যম ছাড়া তাড়িৎ চৌম্বক তরঙ্গ সঞ্চালন সম্ভব নয়
এ কাল্পনিক মাধ্যমটির স্থিতিস্থাপক ধর্ম ছিলো
জৈব যৌগ (Organic Compounds)
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বিমৌল যৌগসমূহকে হাইড্রোকার্বন বলে। জৈব যৌগ বলতে হাইড্রোকার্বন এবং হাইড্রোকার্বন থেকে উদ্ভুত যৌগসমূহকে বুঝায়। যেমন: মিথেন (CH4), ইথেন (C2H6), প্রোপেন (C3H8) প্রভৃতি। ফ্রেডারিক উহলারকে জৈব রসায়নের জনক বলা হয়। জৈব যৌগে কার্বন মৌলটি অবশ্যই থাকবে। বাজারে সিলিন্ডারে যে গ্যাস বিক্রি করা হয় তা মূলত বিউটেন। জৈব বস্তুর সম্পূর্ণ দহনে কার্বন ডাই-অক্সাইড এবং অসম্পূর্ণ দহনে কার্বন মনোক্সাইড উৎপন্ন হয়।
# বহুনির্বাচনী প্রশ্ন
অ্যালিফেটিক যৌগসমূহকে তিনটি শ্রেণীতে ভাগ করা যায় যথা-
ক) অ্যালকেন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত একক বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকেন বলে। অ্যালকেনের সাধারণ সংকেত CnH2n+2। যেমন- মিথেন (CH4), ইথেন (CH3-CH3), প্রোপেন (CH3-CH2- CH3) ইত্যাদি।
খ) অ্যালকিন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত দ্বি বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকিন বলে। অ্যালকেনসমূহের সাধারণ সংকেত CnH2n। যেমন- ইথিন (CH2=CH2), প্রোপিন (CH2= CH- CH2) ইত্যাদি।
গ) অ্যালকাইন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত ত্রি বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকাইন বলে। অ্যালকাইনসমূহের সাধারণ সংকেত CnH2n+2। যেমন- ইথাইন (CH = CH), প্রোপাইন (CH = C-CH3) ইত্যাদি।
বিভিন্ন খাদ্যে উপস্থিত জৈব এসিড।
বিভিন্ন প্রাকৃতিক খাদ্য ও ফলে বিভিন্ন ধরনের জৈব এসিড (Organic Acid) পাওয়া যায়, যা খাদ্যের স্বাদ, গন্ধ ও সংরক্ষণে ভূমিকা রাখে। প্রধান জৈব এসিডগুলোর মধ্যে লেবুতে সাইট্রিক এসিড, আপেলে ম্যালিক এসিড, তেঁতুলে টারটারিক এসিড, এবং দুধে ল্যাকটিক এসিড) অন্যতম।
# বহুনির্বাচনী প্রশ্ন
যে সব চাক্রিক বা হেটারোচাক্রিক যৌগে (4n + 2) সংখ্যক সঞ্চারণশীল পাই ইলেকট্রন বিদ্যমান, তাদেরকে অ্যারোমেটিক যৌগ বলে। 4n + 2 সূত্রে n = 1, 2, 3 হলে সঞ্চারণশীল পাই
ইলেকট্রন দাঁড়ায় যথাক্রমে 6, 10, 14। বেনজিন, ফেনল ও টলুইনে 6টি করে সঞ্চারণশীল পাই ইলেকট্রন বিদ্যমান। ন্যাপথালিন যৌগে 10টি পাই ইলেকট্রন বিদ্যমান। তাই এরা সবাই অ্যারোমেটিক যৌগ।
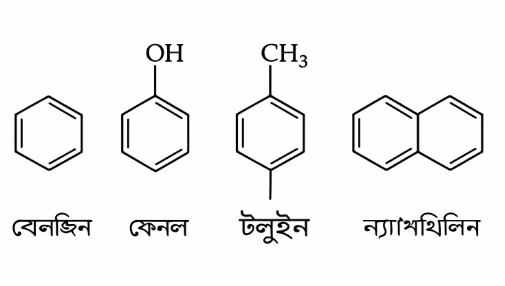
অধিকাংশ অ্যারোমেটিক যৌগই সুগন্ধযুক্ত ও এদের বেনজিন বলয় প্রতিস্থাপন বিক্রিয়া দেয়।
# বহুনির্বাচনী প্রশ্ন
প্রাত্যহিক জীবনে রসায়ন
আমাদের দৈনন্দিন জীবনের সকল ক্ষেত্রে রসায়ন এর ব্যাপক প্রভাব রয়েছে | আমরা প্রতিদিন যে খাবার খাই তাতে রসায়ন রয়েছে, যে বাতাসে আমরা নিশ্বাস নিই তাতে রসায়ন রয়েছে, আমাদের সাবান, আমাদের আবেগ এক কথায় যে সমস্ত বস্তু আমরা দেখতে ও স্পর্শ করতে পারি সকল কিছুতেই রসায়ন বিদ্যমান। আজ আমি আমাদের প্রাত্যহিক জীবনে কিসু মজার রসায়ন নিয়ে আলোচনা করব।
মানব দেহের উপাদান: মানব দেহের বেশির ভাগ হচ্ছে পানি । যেসমস্ত উপাদান দ্বারা তৈরী সেগুলো নিম্নরূপ:
১. অক্সিজেন (৬৫% )
২. কার্বন (১৮%)
৩. হাইধ্রজেন (১০%)
৪. নাইট্রজেন (৩%)
৫. কালসিয়াম (১.৫%)
৬. ফসফরাস (১.০%)
৭. পটাসিয়াম (০.৩৫%)
৮. সালফার (০.2৫%)
৯. সোডিয়াম (০.১৫%)
১০. ম্যাগনেসিয়াম (০.০৫%)
১১. কপার, জিঙ্ক, সেলেনিয়াম, মলিবডেনাম, ফ্লুরিন, ক্লোরিন, আয়োডিন, মান্গানিজ, কোবাল্ট, এবং আইরন (০.৭০%)
১২. লিথিয়াম, সট্রনিয়াম, এলুমিনিয়াম, সিলিকন, লীড ভানাদিয়াম, আর্সেনিক, ব্রোমিন ইত্যাদি ।
# বহুনির্বাচনী প্রশ্ন
নির্মাণ সামগ্রী
নির্মাণ সামগ্রী হিসেবে ইট এবং সিমেন্ট খুবই গুরুত্বপূর্ণ। বালি ও পানির সাথে সিমেন্ট মিশিয়ে ‘মর্টার’ এবং ইট বা পাথরের টুকরা, সিমেন্ট, বালি ও পানি মিশিয়ে কংক্রিট তৈরি করা হয়।
সিমেন্ট
নির্মাণ কাজের অপরিহার্য উপাদান সিমেন্ট। সিমেন্টের প্রধান উপাদান চুন (৬২%), সিলিকা (২২%), অ্যালুমিনা, লৌহ প্রভৃতি। সিমেন্ট দুই ধরনের। যথা- পোর্টল্যান্ড সিমেন্ট এবং অ্যালুমিনাস সিমেন্ট। সিমেন্টে দ্রুত জমাট বাঁধা রোধ করার জন্য জিপসাম যোগ করা হয়।
পোর্টল্যান্ড সিমেন্ট আমাদের দেশে সবচেয়ে বেশি ব্যবহৃত হয়। চুনাপাথর (Limestone) এর সাথে। সামান্য কাদা বা এ্যালুমিনো সিলিকেট (Al2SiO5) মিশিয়ে বিশেষায়িত চুল্লীর মাধ্যমে ক্লিঙ্কার তৈরি করা হয়। ক্লিঙ্কার চূর্ণ (>= ৯৭%) করে তার সাথে সামান্য জিপসাম (=<৩%) মিশিয়ে আধুনিক পোর্টল্যান্ড সিমেন্ট তৈরি করা হয়।
ইট (Brick): তৈরির পদ্ধতি অনুসারে ইটকে তিনভাগে ভাগ করা যায়। বাংলা ইট, সিরামিক ইট এবং কংক্রিটের তৈরি ইট। সাধারণ ইটকে বাংলা ইট বলে। মেশিনে বানানো ইটকে সিরামিক ইট বলে। সিরামিক ইটে সিলিকা (৫৫%), অ্যালুমিনা (৩০%), লৌহ অক্সাইড (৮%), ম্যাগনেসিয়া (৫%), জৈব পদার্থ (১%) থাকতে পারে।
কাঁচ (Glass): কাঁচ রাসায়নিকভাবে অত্যন্ত নিষ্ক্রিয়। কাঁচ বহুদিন রোদে বা পানিতে থাকলে নষ্ট, ক্ষয় বা বৃদ্ধি হয় না। কাচ তৈরির প্রধান কাঁচামাল হলো বালি। বালির প্রধান উপাদান হলো সিলিকা। সিলিকার রাসায়নিক নাম সিলিকন ডাই অক্সাইড (SiO2)। সিলিকার বিশুদ্ধ রূপ কোয়ার্টজ।
সারিন (Sarin): সারিন (C4H10FO2P) অত্যন্ত বিষাক্ত এক ধরনের বর্ণ ও গন্ধহীন তরল পদার্থ যা রাসায়নিক অস্ত্র হিসেবে ব্যবহৃত হয়। এটি স্নায়ুতন্ত্রকে আক্রমণ করে অকার্যকর করে দেয়।
নাইট্রোগ্লিসারিন (Nitroglycerin): নাইট্রোগ্লিসারিন বিস্ফোরক পদার্থটি সালফিউরিক এসিড ও নাইট্রিক এসিডের সংমিশ্রণে প্রস্তুত করা হয়। পাহাড় ভাঙ্গা, টানেল তৈরি ও খনিজ শিল্পে ব্যবহৃত বিস্ফোরক পদার্থ ডিনামাইট প্রস্তুতিতে নাইট্রোগ্লিসারিন ব্যবহৃত হয়।
টি.এন.টি (TNT): 2, 4, 6 ট্রাই নাইট্রো টলুইনকে সংক্ষেপে টি.এন.টি বলে। এটি প্রধানত বিস্ফোরক পদার্থ হিসেবে বিভিন্ন ধরনের বোমায় ব্যবহৃত হয়।
পিকরিক এসিড (Picric Acid): পিকরিক এসিডে রাসায়নিক নাম ২,৪,৬ এটাইনাইট্রোফেনল। এটি বিস্ফোরক যৌগ প্রস্তুতিতে ব্যবহৃত হয়। এছাড়া পোড়া ক্ষতের জ্বালা ও পচন নিবারণে
ডিডিটি (DDT): ডিডিটি এর রাসায়নিক নাম প্যারা প্যারা ডাইক্লোরো ডাই ফিনাইল ট্রাই ক্লোরো ইথেন। শক্তিশালী জীবাণুনাশক ও কীটনাশক হিসেবে ডি.ডি.টি প্রচুর ব্যবহৃত হয়।
গ্যামেক্সিন বা লিনডেন: গ্যামেক্সিন পাউডার বা লিনডেন এর রাসায়নিক নাম বেনজিন হেক্সাক্লোরাইড (C6H6Cl6)। এটি শক্তিশালী জীবাণুনাশক ও কীটনাশক হিসেবে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
ভৌত বিজ্ঞানের বিকাশ (The Development of Physical Science)
আবিষ্কার | আবিষ্কারক | দেশ | সময়কাল (খ্রি.) |
| প্লবতা | আর্কিমিডিস | সিসিলি | ২৮৭ খ্রিস্টপূর্ব |
| বিদ্যুৎ | উইলিয়াম গিলবার্ট | যুক্তরাজ্য | ১৫৭০ |
| রাডার | এ এইচ টেলর এবং লিও সি ইয়ং | যুক্তরাষ্ট্র | ১৯২২ |
| উড়োজাহাজ | অরভিল রাইট ও উইলবার রাইট | যুক্তরাষ্ট্র | ১৯০৩ |
| রকেট | ডব্লিউ কনগ্রিড | যুক্তরাজ্য | ১৮০০ |
| টেলিস্কোপ | গ্যালিলিও | ইতালি | ১৬১০ |
| টেলিগ্রাম | এফ. বি. মোর্স | ইতালি | ১৮৩২ |
| টেলিভিশন | জন এল বেয়ার্ড | যুক্তরাষ্ট্র | ১৯২৬ |
| টেলিফোন | আলেকজোন্ডার গ্রাহাম বেল | যুক্তরাষ্ট্র | ১৯২৬ |
| মাইক্রোফোন | আলেকজোন্ডার গ্রাহাম বেল | যুক্তরাষ্ট্র | ১৮৭৬ |
| রেডিও | জি. মার্কনি | ইতালি | ১৮৯৪ |
| ফলোগ্রাফ | টমাস আলফা এডিসন | যুক্তরাষ্ট্র | ১৮৭৭ |
| বৈদ্যুতিক বাতি | টমাস আলফা এডিসন | যুক্তরাষ্ট্র | ১৮৭৮ |
| থার্মোমিটার | গ্যালিলিও গ্যালিলি | ইতালি | ১৫৯৩ |
| রেফ্রিজারেটর | জেমস হ্যারিসন | যুক্তরাষ্ট্র | ১৮৫১ |
| বাষ্পচালিত ইঞ্জিন | জেমসওয়াট | স্কটল্যান্ড | ১৭৭১ |
| রেলওয়ে ইঞ্জিন | স্টিফেনসন | যুক্তরাজ্য | ১৮২৫ |
| পেট্রোল ইঞ্জিন | নিকোলাস অটো | জার্মানি | ১৮৭৬ |
| ডিজেল ইঞ্জিন | রুডলফ ডিজেল | জার্মানি | ১৮৯৫ |
| ডায়নামো | মাইকেল ফ্যারাডে | যুক্তরাজ্য | ১৮৩১ |
| এক্সরে | উলহহেলম রন্টজেন | রন্টজেন | ১৮৯৫ |
| লেজার | টি এইচ মাইম্যান | যুক্তরাষ্ট্র | ১৯৬০ |
| ডিনামাইট | আলফ্রেড নোবেল | সুইডেন | ১৮৬৭ |
| তেজষ্ক্রিয়তা | হেনরি বেকরেল | ফ্রান্স | ১৮৯৬ |
| ফিশন | অটোহ্যান | জার্মানি | ১৯৩৮ |
| পারমাণবিক বোমা | ওপেনহেইমার | যুক্তরাষ্ট্র | ১৯৪৫ |
| রেডিয়াম, পোলেনিয়াম | মাদাম কুরি | পোল্যান্ড | |
| পলিগ্রাফ | জন এ লারসন | - | ১৯২০ |
| ব্যারোমিটার | টরেসিলি | ইতালি | ১৬৪৩ |
| ছাপাযন্ত্র | জোহানেস গুটেনবার্গ | জার্মানি | |
| হেলিকপ্টার | ইগর সিকরস্কি | - | ১৯৩৯ |
# বহুনির্বাচনী প্রশ্ন
জারুল
গরান
গর্জন
শাল
পরিমাপ (Measurement)
কোন কিছুর পরিমাণ নির্ণয় করাকে পরিমাপ বলে। পরিমাপের আদর্শ পরিমাণকে পরিমাপের একক বলা হয়। যেমন; সময়ের পরিমাপ হচ্ছে সেকেন্ড, দৈর্ঘ্য পরিমাপের একক হচ্ছে মিটার ইত্যাদি।
রাশি (Star)
ভৌতজগতে যা কিছু পরিমাপ করা যায় তাকেই রাশি বলে। রাশি দুই প্রকার। যথা- মৌলিক রাশি এবং লব্ধ রাশি।
মৌলিক রাশি: যে সকল রাশি স্বাধীন বা নিরপেক্ষ যেগুলো অন্য রাশির উপর নির্ভর করে না বরং অন্যান্য রাশি এদের উপর নির্ভর করে তাদেরকে মৌলিক রাশি বলে। মৌলিক রাশি সাতটি। যথা: দৈর্ঘ্য, ভর, সময়, তাপমাত্রা, তড়িৎ প্রবাহ, দীপন ক্ষমতা এবং পদার্থের পরিমাণ।
লব্ধ রাশি: যে সকল রাশি মৌলিক রাশির উপর নির্ভর করে বা মৌলিক রাশি থেকে লাভ করা যায়, তাদেরকে লব্ধ রাশি বলে। মৌলিক রাশি সাতটি ছাড়া বাকি সবই লব্ধ রাশি। যথা: বেগ, ত্বরণ, বল, কাজ ইত্যাদি।
স্কেলার ও ভেক্টর রাশি
দিকের বিবেচনায় বস্তু জগতের সকল রাশিকে দুই ভাগে ভাগ করা যায়। যথা- স্কেলার রাশি এবং ভেক্টর রাশি। যে সকল ভৌত রাশিকে শুধু মান দ্বারা সম্পূর্ণরূপে প্রকাশ করা যায়, দিক নির্দেশের প্রয়োজন হয় না তাদেরকে স্কেলার রাশি বলে। উদাহরণ: দৈর্ঘ্য, ভর, দ্রুতি, কাজ, শক্তি, সময়, তাপমাত্রা ইত্যাদি।
যে সকল ভৌত রাশিকে সম্পূর্ণরূপে প্রকাশ করার জন্য মান ও দিক উভয়ের প্রয়োজন হয় তাদেরকে ভেক্টর রাশি বলে। উদাহরণ: সরণ, ওজন, বেগ, ভরবেগ, ত্বরণ, বল, তড়িৎ তীব্রতা, চৌম্বক তীব্রতা ইত্যাদি।
# বহুনির্বাচনী প্রশ্ন
বিভিন্ন যন্ত্রপাতি
যন্ত্রের নাম | যন্ত্রের ব্যবহার |
| মিটার স্কেল | দৈর্ঘ্য পরিমাপের সবচেয়ে সরল যন্ত্র |
| ভার্নিয়ার স্কেল | দৈর্ঘ্য পরিমাপক যন্ত্র (মিলিমিটারের ভগ্নাংশ পর্যন্ত) |
| ক্রু গজ | তারের ব্যাসার্ধ, সরু চোঙের ব্যাসার্ধ ও ছোট দৈর্ঘ্য পরিমাপক যন্ত্র |
| স্লাইড ক্যালিপার্স | বস্তুর দৈর্ঘ্য, চোঙ বা বেলনের উচ্চতা, ফাঁপা নলের অন্তঃব্যাস ও বহির্ব্যাস, গোলকের ব্যাস নির্ণয় করা যায় |
| স্প্রিং নিক্তি | সরাসরি বস্তুর ওজন নির্ণায়ক |
| তুলা যন্ত্র | খুব অল্প পরিমাণ জিনিসের ভর সূক্ষ্মভাবে নির্ণয় করার যন্ত্র |
| জাইরোকম্পাস | জাহাজের দিক নির্ণায়ক |
| অডিওমিটার | শব্দের তীব্রতা নির্ণায়ক |
| অডিও ফোন | কানে দিয়ে শোনার যন্ত্র |
| ফনোগ্রাফ | শব্দ রেকর্ড করার জন্য ব্যবহৃত |
| সিসমোগ্রাফ | ভূমিকম্প নির্ণায়ক |
| রেইনগেজ | বৃষ্টি পরিমাপক |
| সেক্সট্যান্ট | সূর্য ও অন্যান্য গ্রহের কৌণিক উন্নতি পরিমাপক |
| ক্রোনোমিটার | দ্রাঘিমা নির্ণয়/ সূক্ষ্ম সময় পরিমাপক |
| স্পিডোমিটার | দ্রুতি পরিমাপক |
| অ্যাক্সিলারোমিটার | ত্বরণ পরিমাপক |
| ভেলাটোমিটার | বেগ পরিমাপক |
| অ্যানিমোমিটার | বাতাসের গতিবেগ ও শক্তি পরিমাপক |
| ওডোমিটার | মোটর গাড়ির গতি নির্ণায়ক |
| ট্যাকোমিটার | উড়োজাহাজের গতি নির্ণায়ক |
| অলটিমিটার | উচ্চতা নির্ণায়ক |
| ফ্যাদেমিটার | সমুদ্রের গভীরতা নির্ণয়াক |
| ম্যানোমিটার | গ্যাসের চাপ নির্ণায়ক |
| ব্যারোমিটার | বায়ুমণ্ডলীয় চাপ (Atmospheric pressure) নির্ণায়ক |
| এনোমোমিটার | বায়ুর গতিবেগ পরিমাপক |
| হাইগ্রোমিটার | বায়ুতে আর্দ্রতা (Humidity) পরিমাপক |
| হাইড্রোমিটার | তরলের আপেক্ষিক গুরুত্ব (Specific gravity) বা ঘনত্ব নির্ণায়ক |
| হাইড্রোফোন | পানির তলায় শব্দ নিরূপক |
| ল্যাক্টোমিটার | দুধের বিশুদ্ধতা নির্ণায়ক |
| ক্যালরিমিটার | তাপ পরিমাপক |
| থার্মোমিটার | উষ্ণতা পরিমাপক |
| থার্মোস্ট্যাট | ফ্রিজ, ইস্ত্রি, ওভেন ইত্যাদিতে স্থির তাপমাত্রা নিয়ন্ত্রণের যন্ত্র |
| পাইরোমিটার | তারকাসমূহের (সূর্যের) উত্তাপ নির্ণায়ক |
| টেনসিওমিটার | তরলের পৃষ্ঠটান পরিমাপক |
| অ্যামিটার | বিদ্যুৎ প্রবাহ পরিমাপক |
| গ্যালভানোমিটার | ক্ষুদ্র মাপের বিদ্যুৎ প্রবাহ নির্ণায়ক |
| ওহম মিটার | পরিবাহীর রোধ নির্ণায়ক |
| ভোল্ট মিটার | বৈদ্যুতিক বিভব বা চাপ পরিমাপক |
| ইলেক্ট্রফেরাস | বৈদ্যুতিক আবেশ দ্বারা চার্জ উৎপাদনের সরল যন্ত্র |
| ভ্যানডিগ্রাফ | বৈদ্যুতিক আবেশ দ্বারা চার্জ উৎপাদনের আধুনিক যন্ত্র |
| তড়িৎবীক্ষণ যন্ত্র/ ইলেক্ট্রোস্কোপ | কোনো বস্তুতে আধানের অস্তিত্ব ও প্রকৃতি নির্ণায়ক |
| স্ফিগমোম্যানোমিটার | মানবেদেহের রক্তচাপ নির্ণায়ক |
| স্টেথোস্কোপ | হৃৎপিণ্ড ও ফুসফুসের শব্দ নিরূপক |
| কার্ডিওগ্রাফ | হৃৎপিণ্ডের গতি নির্ণায়ক |
| ক্রেস্কোগ্রাফ | উদ্ভিদের বৃদ্ধি নির্ণায়ক |
| ইনকিউবেটর | ডিম থেকে বাচ্চা ফুটানোর যন্ত্র |
| ড্রেজার | পানির নিচে মাটি কাটার যন্ত্র |
| পাওয়ার থ্রেসার | ধান মাড়াইয়ের মেশিন |
| গাইগার মুলার কাউন্টার | রেডিওঅ্যাকটিভ মৌল অনুসন্ধানের যন্ত্র |
# বহুনির্বাচনী প্রশ্ন
রাশি পরিমাপের পদ্ধতি
রাশি | C.G.S পদ্ধতিতে একক | M.K.S পদ্ধতিতে একক | F.P.S পদ্ধতিতে একক |
| দৈর্ঘ্য | Centimeter | Gram | Foot |
| ভর | Gram | Kilogram | Pound |
| সময় | Second | Second | Second |
S.I. পদ্ধতি
১৯৬০ সাল থেকে দুনিয়া জোড়া বিভিন্ন রাশির একই রকম একক চালু করার সিদ্ধান্ত হয়। এককের এই পদ্ধতিকে বলা হয় আন্তর্জাতিক পদ্ধতি (International Systems of Units) বা সংক্ষেপে এস.আই (S.I)। আন্তর্জাতিক পদ্ধতিতে M.K.S পদ্ধতিকে আত্মীয়করণ করা হয়েছে। এই পদ্ধতিতে সাতটি মৌলিক রাশির জন্য সাতটি মৌলিক একক ধরা হয়েছে এবং বাকী সকল একক এক বা একাধিক মৌলিক এককের গুণফল বা ভাগফল থেকে প্রতিপাদন করা হয়েছে।
সাতটি মৌলিক একক হলো-
মৌলিক রাশি | একক | মৌলিক রাশি | একক |
| দৈর্ঘ্য | মিটার | তড়িৎ প্রবাহ | অ্যাম্পিয়ার |
| ভর | কিলোগ্রাম | দীপন ক্ষমতা | ক্যান্ডেলা |
| সময় | সেকেন্ড | পদার্থের পরিমাণ | মোল |
| তাপমাত্রা | কেলভিন | - | - |
এস আই পদ্ধতিতে গুরুত্বপূর্ণ একক
রাশি | একক | রাশি | একক |
| ক্ষেত্রফল | মিটার২ | প্রসারণ সহগ | প্রতি কেলভিন |
| আয়তন | মিটার২ | তাপ ধারণ ক্ষমতা | জুল/ কেলভিন |
| সরণ | মিটার | আপেক্ষিক সুপ্ততাপ | জুল/ কিলোগ্রাম |
| বেগ বা দ্রুতি | মিটার/সেকেন্ড | Viscosity | Poise |
| ত্বরণ | মিটার/সেকেন্ড২ | চৌম্বক ফ্লাক্স | ওয়েবার |
| কৌণিক ত্বরণ | রেডিয়ান/সেকেন্ড২ | চৌম্বক আবেশ | (Tesla) টেসলা |
| ভরবেগ | কিলোগ্রাম-মিটার/ সে২ | আলোক ফ্লাক্স | লুমেন |
| বল বা ওজন | নিউটন | দীপন তীব্রতা | লাক্স |
| কাজ/ শক্তি/তাপ | জুল | লেন্সের ক্ষমতা | ডায়অপ্টার |
| ক্ষমতা | ওয়াট | আধান | কুলম্ব |
| ঘনত্ব | কিলোগ্রাম-মিটার৩ | বিভব পার্থক্য/ তড়িচ্চালক বল | ভোল্ট |
| চাপ | প্যাসকেল | তড়িৎ প্রাবল্য | নিউটন/কলম্ব |
| Stress | নিউটন/মিটার২ | রোধ | ওহম |
| দোলনকাল | সেকেন্ড | পরিবাহিতা | সিমেন্স |
| তরঙ্গ দৈর্ঘ্য | মিটার | তেজস্ক্রিয়তা | বেকরেল |
| কম্পাঙ্ক | হার্জ | এক্সরে | রন্টজেন |
# বহুনির্বাচনী প্রশ্ন
বলবিদ্যা (Mechanics)
সরণ (Displacement)
নির্দিষ্ট দিকে পরিপার্শ্বিকের সাপেক্ষে বস্তুর অবস্থানের পরিবর্তনকে সরণ বলে। সরণের একক হল দৈর্ঘ্যের একক অর্থাৎ মিটার।
দ্রুতি (Speed)
সময়ের সাথে কোন বস্তুর অবস্থানের পরিবর্তনের হারকে দ্রুতি বলে। দ্রুতির একক মি./সে.।
বেগ (Velocity)
সময়ের সাথে কোন বস্তুর সরণের হারকে বেগ বলে অর্থাৎ বস্তু নির্দিষ্ট দিকে একক সময়ে যে দূরত্ব অতিক্রম করে তাই বেগ। বেগের একক মিটার/সেকেন্ড বা (ms-1)।
ত্বরণ (Acceleration)
সময়ের সাথে বস্তুর অসম বেগের পরিবর্তনের হারকে ত্বরণ বলা হয়। একটি বস্তু সুষম বেগে না চলে এর বেগের বা মানের যে পরিবর্তন হয় তাই ত্বরণ। ত্বরণ একটি ভেক্টর রাশি। ত্বরণের একক মিটার/সেকেন্ড২ (m/s2) বা (ms-2)। কৌণিক ত্বরণের একক রেডিয়ান/সেকেন্ড২ (rd/s2) বা (rds-2)।
# বহুনির্বাচনী প্রশ্ন
নিউটনের গতি বিষয়ক সূত্র (Newton's Law of Motion)
১৬৮৭ সালে বিজ্ঞানী স্যার আইজ্যাক নিউটন তাঁর অমর গ্রন্থ "ফিলোসোফিয়া ন্যাচারালিস প্রিন্সিপিয়া ম্যাথমেটিকা'তে বস্তুর ভর, গতি ও বলের মধ্যে সম্পর্ক স্থাপন করে তিনটি সূত্র প্রকাশ করেন। এ তিনটি সূত্র নিউটনের 'গতি বিষয়ক সূত্র' নামে পরিচিত।
প্রথম সূত্র: বাহ্যিক কোনো বল প্রয়োগ না করলে স্থির বস্তু চিরকাল স্থিরই থাকবে এবং গতিশীল বস্তু সুষম দ্রুতিতে সরলপথে চলতে থ াকবে। (Every body continues in its state of rest, or of uniform motion in a straight line until an external force is applied to the body)
দ্বিতীয় সূত্র: বস্তুর ভরবেগের পরিবর্তনের হার এর উপর প্রযুক্ত বলের সমানুপাতিক এবং বল যেদিকে ক্রিয়া করে বস্তুর ভরবেগের পরিবর্তনও সেদিকে ঘটে। (The rate of change of momentum of a body is proportional to the applied force and takes place in the direction of the straight line along which the force acts).
তৃতীয় সূত্র: প্রত্যেক ক্রিয়ারই একটি সমান ও বিপরীত প্রতিক্রিয়া আছে। (To every action there is an equal and opposite reaction)।
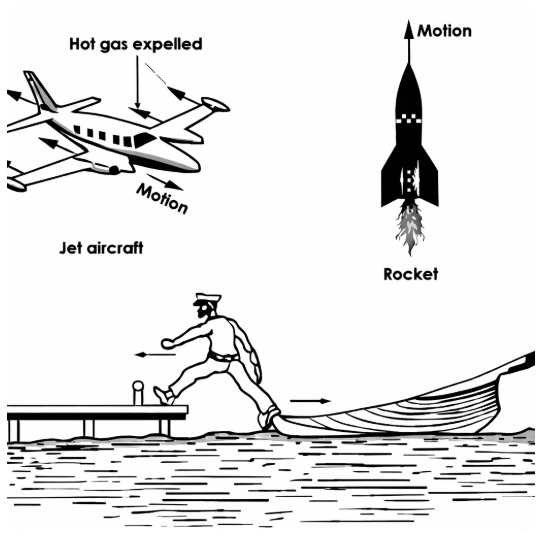
ক) প্রথম সূত্র থেকে জড়তা ও বলের ধারণা পাওয়া যায়।
খ) দ্বিতীয় সূত্র হতে পাই, বল = ভর ত্বরণ (F = ma)
গ) নিউটনের গতির তৃতীয় সূত্রের প্রয়োগ:
- মহাকাশযান (রকেট) উৎক্ষেপণ গতির তৃতীয় সূত্রেরএকটি ব্যবহারিক প্রয়োগ। রকেটে জ্বালানি পুড়িয়ে প্রচুর গ্যাস উৎপন্ন করা হয়। রকেটের পিছনের অংশ থেকে গ্যাস প্রচণ্ড বেগে নির্গত হওয়ায় গতির বিপরীত ক্রিয়ায় রকেটকে বিপরীত দিকে ধাক্কা দেয়। ফলে রকেট প্রচণ্ড বেগে উপরের দিকে এগিয়ে যায়।
- ফুলানো বেলুনের মুখ ছেড়ে দিলে বাতাস বেরিয়ে যাবার সঙ্গে সঙ্গে বেলুনটি ছুটে যায়। রকেট ইঞ্জিনের নীতির সঙ্গে এর মিল আছে।
- জেট ইঞ্জিন রি-অ্যাকশন ইঞ্জিন।
- বিমান ও রকেট চলার মধ্যে মূল পার্থক্য হলো রকেট চলার জন্য বাতাসের দরকার হয় না কিন্তু বিমান সম্পূর্ণভাবে বাতাস নির্ভর।
- মাঝির নৌকা চালানো গতির তৃতীয় সূত্রের সাহায্যে ব্যাখ্যা করা যায়।
# বহুনির্বাচনী প্রশ্ন
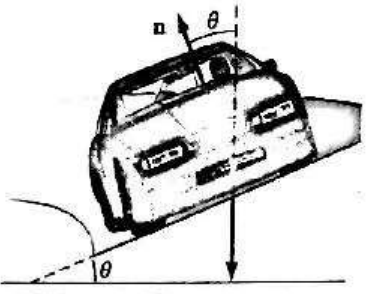
রাস্তার ব্যাংকিং (Banking of Roads)
বক্রপথে মোটর বা রেলগাড়ি চলার সময় একটি কেন্দ্রমুখী বলের প্রয়োজন হয়। কেন্দ্রমুখী বলের অভাবে গতি জড়তার কারণে যানবাহন উল্টে যাওয়ার সম্ভাবনা থাকে। এই জড়তাকে প্রশমিত করার জন্য বক্রপথে বাইরের রাস্তা ভিতরের দিকের চেয়ে কিছুটা উচু করে কেন্দ্রমুখী বল সৃষ্টি করা হয়। এ ব্যবস্থাকে রাস্তার ব্যাংকিং বলে।
ভরবেগ (Momentum)
বস্তুর ভর ও বেগের গুণফলকে ভরবেগ বলে। ভরবেগের একক Kgm/sec এবং মাত্রা সমীকরণ MLT-1 । ভরবেগ = ভর বেগ।
ভরবেগের সংরক্ষণ সূত্র: "একাধিক বস্তুর মধ্যে শুধু ক্রিয়া ও প্রতিক্রিয়া ছাড়া অন্য কোনো বল কাজ না করলে কোন নির্দিষ্ট দিকে তাদের মোট ভরবেগের কোনো পরিবর্তন হয় না"।
উদাহরণ: বন্দুক থেকে গুলি ছোড়া হলে বন্দুক পেছনের দিকে আসে। কারণ গুলি ও বন্দুকের ভরবেগ সমান কিন্তু বিপরীতমুখী। বন্দুকের ভর বেশি বলে বেগ কম হয় কিন্তু গুলির ভর কম বলে বেগ বেশি হয়।
- নৌকা থেকে আরোহীরা নামার সময় নৌকা পেছনের দিকে আসে কারণ নৌকা ও আরোহীর ভরবেগ পরস্পর সমান কিন্তু বিপরীতমুখী
# বহুনির্বাচনী প্রশ্ন
স্থিতিস্থাপকতা (Elasticity)
বস্তুর যে ধর্ম উহার উপর প্রযুক্ত বলের ক্রিয়ায় তার আকার বা আয়তন বা উভয়েরই পরিবর্তনের প্রচেষ্টাকে বাধা দেয় এবং প্রযুক্ত বল অপসারণ করলে তার পূর্বের আকার বা আয়তন ফেরত পায়, তাকে স্থিতিস্থাপকতা বলে। যার স্থিতিস্থাপকতা যত বেশি তার আকার বা আয়তন পরিবর্তনে তত অধিক বল প্রয়োগ করতে হয়।
ইস্পাত (বা লোহা) রাবার অপেক্ষা অধিক স্থিতিস্থাপক। একই পরিমাণ আকার বা আয়তন পরিবর্তনের জন্য ইস্পাতে রাবার অপেক্ষা অনেক বেশি বল প্রয়োগ করতে হয়। রাবার শক্ত ও স্থিতিস্থাপক বলে গাড়ির টায়ার তৈরিতে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
ইস্পাত
কপার
কাঁচ
পানি
মহাকর্ষ ও অভিকর্ষ (Gravitation & Gravity)
এই মহাবিশ্বের প্রত্যেকটি বস্তু কণা একে অপরকে নিজের দিকে আকর্ষণ করে। মহাবিশ্বের যে কোন দুটি বস্তুর মধ্যে যে আকর্ষণ তাকে মহাকর্ষ বলে। দুটি বস্তুর একটি যদি পৃথিবী হয় তবে তাকে অভিকর্ষ বা মাধ্যাকর্ষণ বলে অর্থাৎ কোনো বস্তুর উপর পৃথিবীর আকর্ষণকে অভিকর্ষ বা মাধ্যাকর্ষণ বলে। অভিকর্ষও এক ধরনের মহাকর্ষ। অভিকর্ষ বল একটি কেন্দ্রমুখী বল। মাধ্যাকর্ষণ বলের বা অভিকর্ষের জন্য পৃথিবীর ঘূর্ণনের ফলে আমরা ছিটকিয়ে পড়ি না। পৃথিবীর কেন্দ্রীয় আকর্ষণে আকৃষ্ট হয়ে বায়ুমণ্ডল পৃথিবীর সঙ্গে আবর্তিত হচ্ছে।
# বহুনির্বাচনী প্রশ্ন
নিউটনের মহাকর্ষ সূত্র (Newton's Law of Gravitation)
বিজ্ঞানী নিউটন মহাকর্ষ সম্পর্কে একটি সূত্র প্রদান করেছেন। সূত্রটি হল " মহাবিশ্বের প্রতিটি বস্তুকণা একে অপরকে নিজ দিকে আকর্ষণ করে এবং এই আকর্ষণ বলের মান বস্তু কণাদ্বয়ের ভরের গুণফলের সমানুপাতিক এবং দূরত্বের বর্গের ব্যস্তানুপাতিক এবং এই বল সংযোগ সরলরেখা বরাবর ক্রিয়া করে”। মহাকর্ষ বল শুধুমাত্র দুরত্ব এবং ভরের উপর নির্ভরশীল। G কে মহাকর্ষীয় ধ্রুবক বলে। এর একটি নির্দিষ্ট মান আছে। এই মান হল 6.673 10-11 Nm2Kg-2 ।
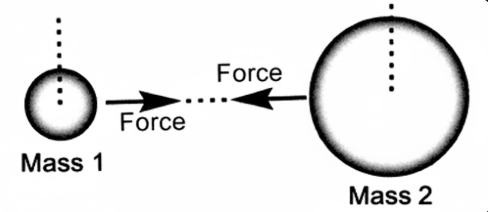
চিত্র: দুটি বস্তুর মধ্যে আকর্ষণ
# বহুনির্বাচনী প্রশ্ন
মাধ্যাকর্ষণজনিত ত্বরণ বা অভিকর্ষজ ত্বরণ (Acceleration due to Gravity)
অভিকর্ষ বলের প্রভাবে ভূপৃষ্ঠে মুক্তভাবে পড়ন্ত কোনো বস্তুর বেগ বৃদ্ধির হারকে অভিকর্ষজ ত্বরণ বলে। একে g দিয়ে প্রকাশ করা হয়। ভূপৃষ্ঠে বিভিন্ন স্থানে g এর মান বিভিন্ন। ভূ-পৃষ্ঠে মাধ্যাকর্ষণজনিত ত্বরণের মান সর্বোচ্চ। 45° অক্ষাংশে সমুদ্র সমতলে g এর মান আদর্শ ধরা হয়। g এর আদর্শ মান হচ্ছে 9.8 মিটার/সে২ বা (m/s2) বা (ms2)। পৃথিবীপৃষ্ঠ থেকে উপরে উঠলে বা ভিতরে গেলে মাধ্যাকর্ষণ বল কমে যায়, অর্থ্যাৎ g মান এর মান কমতে থাকে। পৃথিবীর কেন্দ্রে g এর মান শূন্য।
# বহুনির্বাচনী প্রশ্ন
পড়ন্ত বস্তুর সূত্র (Laws of falling bodies)
পড়ন্ত বস্তু সম্পর্কে গ্যালিলিও তিনটি সূত্র প্রদান করেন। এগুলোকে পড়ন্ত বস্তুর সূত্র বলে। সূত্রগুলো একমাত্র স্থির অবস্থান থেকে বিনা বাধায় পড়ন্ত বস্তুর ক্ষেত্রে প্রযোজ্য।
১) স্থির অবস্থান থেকে এবং একই উচ্চতা থেকে বিনা বাধায় পড়ন্ত সকল বস্তু সমান সময়ে সমান পথ অতিক্রম করে।
২) স্থির অবস্থান থেকে বিনা বাধায় পড়ন্ত বস্তুর নির্দিষ্ট সময়ে প্রাপ্ত বেগ ঐ সময়ের সমানুপাতিক।
৩) স্থির অবস্থান থেকে বিনা বাধায় পড়ন্ত বস্তু নির্দিষ্ট সময়ে যে দূরত্ব অতিক্রম করে তা ঐ সময়ের বর্গের সমানুপাতিক।
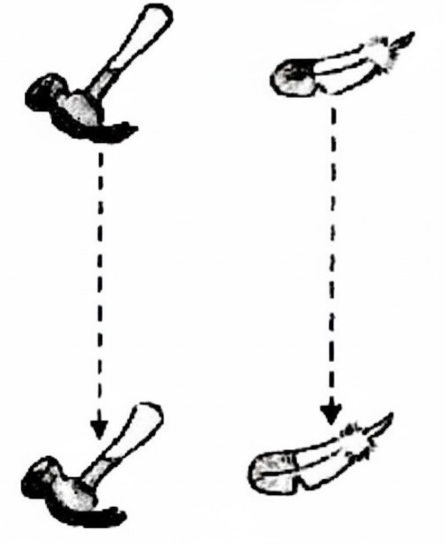
স্থির অবস্থান এবং একই উচ্চতা হতে একটি পালক ও একটি হাতুড়ি একই সাথে ফেলে দিলে তা একই সাথে মাটিতে পড়বে। কিন্তু বাতাসের বাধার কারণে এমনটি হয় না। তবে বাতাসের বাধা না থাকলে পালক ও হাতুড়ি একই সাথে মাটিতে পড়বে।
# বহুনির্বাচনী প্রশ্ন
ভর ও ওজন (Mass & Weight)
কোনো বস্তুর মধ্যে পদার্থের মোট পরিমাণকে ঐ বস্তুর ভর বলে। আন্তর্জাতিক পদ্ধতিতে ভরের একক কিলোগ্রাম (Kg)। স্থানভেদে বস্তুর ভরের কোনো পরিবর্তন হয় না। পৃথিবী পৃষ্ঠে কোনো বস্তুর ভর ৪৯ কেজি হলে চন্দ্রপৃষ্ঠে ঐ বস্তুটির ভর হবে ৪৯ কেজি। পৃথিবীপৃষ্ঠে কোনো বস্তুর ভর ৫০ কেজি হলে ভূ-কেন্দ্রে ঐ বস্তুটির ভর হবে ৫০ কেজি।
কোনো বস্তুকে পৃথিবী যে পরিমাণ বল দ্বারা তার কেন্দ্রের দিকে আকর্ষণ করে, তাকে ঐ বস্তুটির ওজন বলে। ওজনের একক নিউটন। বস্তুর ওজন = বস্তুর ভর ঐ স্থানে অভিকর্ষজ ত্বরণ
বস্তুর ওজন অভিকর্ষজ ত্বরণ উপর নির্ভরশীল। বিভিন্ন স্থানে অভিকর্ষজ ত্বরণের মান বিভিন্ন হওয়ায় স্থানভেদে বস্তুর ওজন পরিবর্তিত হয়। এজন্য কোনো বস্তুকে পৃথিবী থেকে চাঁদে বা অন্য কোনো স্থানে নিলে বস্তুর ভর একই থাকে কিন্তু ওজন পরিবর্তিত হয়। যেমন: চাঁদে অভিকর্ষজ ত্বরণের মান পৃথিবীর অভিকর্ষজ ত্বরণের মানের ৬ ভাগের ১ ভাগ। এজন্য চাঁদে কোনো বস্তুর ওজন পৃথিবীতে ঐ বস্তুর ওজনের ৬ ভাগের ১ ভাগ হবে।
বস্তুর অবস্থানের পরিবর্তনের সাথে সাথে অভিকর্ষজ ত্বরণের মান (মাধ্যাকর্ষণ বল) ও ওজনের পরিবর্তন
বস্তুর অবস্থান | অভিকর্ষজ ত্বরণের মান (মাধ্যাকর্ষণ বল | বস্তুর ওজন |
| মেরু অঞ্চল | সর্ব্বোচ | |
| নিরক্ষীয় অঞ্চল | সর্বনিম্ন | |
| চন্দ্রপৃষ্ঠ | পৃথিবীর ৬ ভাগের ১ ভাগ | |
| ভূপৃষ্ঠ থেকে উপরে | হ্রাস পায় | |
| ভূপৃষ্ঠের অভ্যন্তরে | ||
| পৃথিবীর কেন্দ্র | শূন্য | |
# বহুনির্বাচনী প্রশ্ন
লিফটে ও মহাশূন্যে ওজনের তারতম্য: ওজনহীনতা
Variation of weight in Lift and Space: Weightlessness
ব্যক্তির ভর m এবং ঐ স্থানের অভিকর্ষজ ত্বরণ ৪ হলে, ব্যক্তি ওজন হবে, W = mg। এক ব্যক্তি লিফটে সমবেগে উপরে উঠলে বা নিচে নামলে তার ওজনের কোনো পরিবর্তন হবে না। কিন্তু লিফটে a ত্বরণে উপরে উঠলে ব্যক্তি ওজন অনুভব করবে, W = m (g+a) অর্থাৎ বেশি ওজন অনুভব। করবে। আবার, ও ত্বরণে নিচে নামলে ব্যক্তি ওজন অনুভব করবে, W = m(g-a) অর্থ্যাৎ কম ওজন অনুভব করবে।
এক ব্যক্তি দালানের দশতলায় একটি লিফটে দাঁড়িয়ে আছে। তার হাতে কোনো স্প্রিং নিক্তি থেকে ঝুলানো একটি বস্তু 10 নিউটন ওজন নির্দেশ করছে। হঠাৎ লিফটের তার ছিড়ে লিফটটি মুক্তভাবে নিচে পড়তে থাকলে স্প্রিং নিক্তিতে বস্তুটির ওজন ০ নিউটন নির্দেশ করবে। কারণ মুক্তভাবে পড়ন্ত লিফটটির ত্বরণ হবে ৪ এবং সেক্ষেত্রে বস্তুর ত্বরণ হবে (g - g) = 0 সুতরাং বস্তুর ওজন হবে W = mx0=0 নিউটন। মহাশূন্যচারী মহাশূন্যযানে পৃথিবী প্রদক্ষিণরত থাকার সময় নিজেকে ওজনহীন মনে করেন কারণ মহাশূন্যচারীরা মহাশূন্যযানে করে পৃথিবীকে একটি নির্দিষ্ট উচ্চতায় বৃত্তকার কক্ষপথে প্রদক্ষিণ করে থাকেন। এই বৃত্তাকার গতির জন্য মহাশূন্যযানের পৃথিবীর কেন্দ্রের দিকে ঐ উচ্চতায় ৪ এর মানের সমান মানের একটি ত্বরণ হয়। এই অবস্থায় মহাশূন্যযানের দেয়ালের সাপেক্ষে মহাশূন্যচারীর ত্বরণ (g - g) = 0 হয় এবং মহাশূন্যচারী মহাশূন্যযানের দেয়াল বা মেঝেতে কোনো বল প্রয়োগ করে না। ফলে তিনি তাঁর ওজনের বিপরীত কোন প্রতিক্রিয়া বলও অনুভব করেন না। তাই তিনি ওজনহীনতা অনুভব করেন।
# বহুনির্বাচনী প্রশ্ন
1000 N
880 N
9680 N
11000 N
সরল দোলক (Simple Pendulum)
একটি ভারী আয়তনহীন বস্তুকণাকে ওজনহীন, নমনীয় ও অপ্রসারণশীল সুতা দিয়ে ঝুলিয়ে দিলে এটি যদি ঘর্ষণ এড়িয়ে স্বাধীনভাবে দুলতে পারে, তবে তাকে সরল দোলক বলে।
দোলকের দোলনকাল তার কার্যকরী দৈর্ঘ্য এবং ঐ স্থানের অভিকর্ষজ ত্বরণের উপর নির্ভর করে।
ক) কোনো নির্দিষ্ট স্থানে কোনো সরল দোলকের দোলনকাল (T) এর কার্যকরী দৈর্ঘ্যের (L) বর্গমূলের সমানুপাতে পরিবর্তিত হয়।
যখন L ধ্রুব।
সরল দোলকের সুতার দৈর্ঘ্য কমলে, দোলনকাল কমে। শীতকালে দোলক ঘড়ির কার্যকরী দৈর্ঘ্য কমে যায় বলে দোলনকাল হ্রাস পায়। ফলে ঘড়িটি দ্রুত চলে। গ্রীষ্মকালে অধিক তাপমাত্রার কারণে দোলক ঘড়ির কার্যকরি দৈর্ঘ্য বাড়ে। ফলে দোলনকাল বাড়ে এবং ঘড়িটি ধীরে চলে।
খ) সরল দোলকের কার্যকরী দৈর্ঘ্য অপরিবর্তিত থাকলে এর দোলনকাল (T) অভিকর্ষজ ত্বরণের বর্গমূলের ব্যস্তানুপাতে পরিবর্তিত হয়।
যখন L ধ্রুব।
অভিকর্ষজ ত্বরণের মান বাড়লে, সরলদোলকের দোলনকাল কমে। বিষুবরেখা অপেক্ষা মেরুতে অভিকর্ষজ ত্বরণের মান বেশি হয়। এজন্য একটি পেন্ডুলাম ঘড়ি বিষুবরেখা থেকে মেরুতে নিলে এর দোলনকাল হ্রাস পায়। ফলে ঘড়িটি দ্রুত চলে।
গ) দোলনকাল ববের ভরের উপর নির্ভরশীল নয়। যেমন: একজন বালিকা দোলনায় দোল খাচ্ছে। সে উঠে দাড়ালে দোলনকালের কোনো পরিবর্তন হবে না।
সরল দোলকের দোলন কাল T, কার্যকরি দৈর্ঘ্য L এবং অভিকর্ষজ ত্বরণ g হলে -
# বহুনির্বাচনী প্রশ্ন
কেপলারের সূত্র (Kepler's Law)
জ্যোর্তিবিজ্ঞানে কেপলারের গ্রহীয় গতিসূত্র সূর্যের চারিদিকে গ্রহগুলোর গতি ব্যাখ্যা করে। বিখ্যাত জার্মান জ্যোর্তিবিজ্ঞানী ইয়োহানেস কেপলার গ্রহের গতির তিনটি সূত্র প্রদান করেছেন, যা পরবর্তীতে কেপলারের সূত্র নামে পরিচিত। সূত্রগুলো হল:
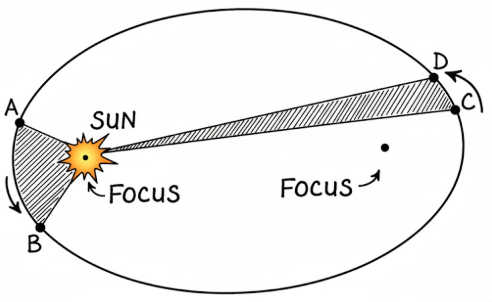
১. প্রতিটি গ্রহের কক্ষপথ একটি উপবৃত্ত, সূর্য যার একটি ফোকাসে অবস্থিত।
২. সূর্য এবং একটি গ্রহকে সংযোগকারী রেখা গ্রহের আবর্তনের সাথে সাথে সমান সময়ে সমান ক্ষেত্রফল অতিক্রম করে।
৩. একটি গ্রহের পর্যায়কালের বর্গ সূর্য হতে ঐ গ্রহের গড় দুরত্বের ঘনফলের সমানুপাতিক। অর্থ্যাৎ।
কাজ (Work)
কোনো বস্তুর উপর বল প্রয়োগে যদি বস্তুটির সরণ ঘটে, তাহলে বল এবং বলের দিকে বলের প্রয়োগবিন্দুর সরণের উপাংশের গুণফলকে কাজ বলে।
ক্ষমতা (Power)
কাজ সম্পাদনকারী কোনো ব্যক্তি বা উৎস এর কাজ করার হারকে ক্ষমতা বলে।
১ অশ্ব শক্তি (H.P) = ৭৪৬ ওয়াট = ০.৭৪৬ কিলোওয়াট
# বহুনির্বাচনী প্রশ্ন
কাজ (Work)
কোনো বস্তুর উপর বল প্রয়োগে যদি বস্তুটির সরণ ঘটে, তাহলে বল এবং বলের দিকে বলের প্রয়োগবিন্দুর সরণের উপাংশের গুণফলকে কাজ বলে। কাজের মাত্রা সমীকরণ ML2T-2।
কাজ = বল ⤫ বলের দিকে সরণের উপাংশ।
আন্তর্জাতিক পদ্ধতিতে কাজের একক জুল। সিজিএস পদ্ধতিতে কাজের একক আর্গ। 1 জুল= 107 আর্গ। পাহাড়ে ওঠা বা সিঁড়ি ভাঙ্গায় অভিকর্ষ বলের বিপরীতে কাজ করতে হয় বলে পরিশ্রম বেশি হয়। পক্ষান্তরে পাহাড় থেকে বা সিঁড়ি দিয়ে নামার সময় অভিকর্ষ বলের দিকে কাজ করতে হয় বলে পরিশ্রম কম হয়। পাহাড়ে ওঠার সময় শরীরকে স্থির রাখার জন্য সামনের দিকে ঝুঁকতে হয়।
# বহুনির্বাচনী প্রশ্ন
1n-m
1kg-mn
10n-m/s
10kg 31s
ক্ষমতা
কাজ
শক্তি
বল
ক্ষমতা (Power)
কাজ সম্পাদনকারী কোনো ব্যক্তি বা উৎস এর কাজ করার হারকে ক্ষমতা বলে।
ক্ষমতা = কাজ/সময়
ক্ষমতার একক ওয়াট।
# বহুনির্বাচনী প্রশ্ন
কাজ পরিমাপের একক
শক্তি পরিমাপের একক
ক্ষমতা পরিমাপের একক
চাপ পরিমাপের একক
শক্তি পরিমাপের একক
ক্ষমতা পরিমাপের একক
চাপ পরিমাপের একক
কাজ পরিমাপের একক
অশ্ব ক্ষমতা (Horse power)
ইঞ্জিনের ক্ষমতা কে প্রকাশ করার জন্য অশ্বক্ষমতা একক ব্যবহৃত হয়। ১ অশ্ব ক্ষমতা (H.P) = ৭৪৬ ওয়াট = ০.৭৪৬ কিলোওয়াট। অর্থাৎ প্রতি সেকেন্ডে ৭৪৬ জুল কাজ করার ক্ষমতাকে এক অশ্ব ক্ষমতা বলে।
# বহুনির্বাচনী প্রশ্ন
কাজ পরিমাপের একক
শক্তি পরিমাপের একক
ক্ষমতা পরিমাপের একক
চাপ পরিমাপের একক
শক্তি (Energy)
কোনো বস্তুর কাজ করার সামর্থ্যকে শক্তি বলে(energy)। বস্তু সর্বমোট যতটুকু কাজ করতে পারে তা দিয়েই বস্তুর শক্তির পরিমাপ করা হয়।
যেহেতু কোনো বস্তুর শক্তির পরিমাপ করা হয় তার দ্বারা সম্পন্ন কাজের পরিমাণ থেকে; সুতরাং শক্তি ও কাজের পরিমাণ অভিন্ন। কাজের মতো শক্তিও স্কেলার রাশি।
মাত্রা ও একক : শক্তির মাত্রা ও কাজের মাত্রা একই অর্থাৎ ML2T-2।
শক্তির একক ও কাজের একক একই অর্থাৎ জুল (J)।
# বহুনির্বাচনী প্রশ্ন
শক্তির রূপান্তর (Transformation of Energy)
তড়িৎ শক্তির রূপান্তর: বৈদ্যুতিক মোটরে তড়িৎ শক্তি যান্ত্রিক শক্তিতে রূপান্তরিত হয়। বৈদ্যুতিক ইস্ত্রি এবং হিটারে তড়িৎ শক্তি তাপ শক্তিতে রূপান্তরিত হয়। বৈদ্যুতিক বাল্বে তড়িৎ শক্তি আলোক শক্তিতে রূপান্তরিত হয়। বৈদ্যুতিক ঘণ্টা ও লাউড স্পিকারের মাধ্যমে তড়িৎশক্তি শব্দশক্তিতে রূপান্তরিত হয়।
আলোক শক্তির রূপান্তর: ফটো-ইলেকট্রিক কোষের উপর আলোক পড়লে বিদ্যুৎ উৎপন্ন হয়। এক্ষেত্রে আলোক শক্তি তড়িৎ শক্তিতে রূপান্তরিত হয়। হেরিকেনের চিমনিতে হাত দিলে গরম অনুভূত হয়। এখানে আলোক শক্তি তাপ শক্তিতে রূপান্তরিত হয়। ফটোগ্রাফিক কাগজের উপর আলোর ক্রিয়ায় আলোক শক্তি রাসায়নিক শক্তিতে রূপান্তরিত হয়।
যান্ত্রিক শক্তির রূপান্তর: দুই হাতের তালু পরস্পরের সাথে ঘষলে গরম অনুভূতি হয়। এখানে যান্ত্রিক শক্তি তাপশক্তিতে রূপান্তরিত হয়। জেনারেটরের সাহায্যে যন্ত্র শক্তিকে বিদ্যুৎ শক্তিতে রূপান্তরিত করা হয়। নদীতে বাঁধ দিয়ে জলবিদ্যুৎ (Hydroelectricity) উৎপাদনের সময় সঞ্চিত জলরাশিতে বিভবশক্তি জমা হয়। পানি নিচে প্রবাহিত হওয়ার সময় এই বিভবশক্তি গতিশক্তিতে পরিণত হয়। পানি প্রবাহের সাহায্যে টারবাইনের চাকা ঘুরিয়ে বিদ্যুৎ উৎপাদন করা হয়। এভাবে যান্ত্রিক শক্তি তড়িৎশক্তিতে রূপান্তরিত হয়।
শব্দ শক্তির রূপান্তর: টেলিফোন ও রেডিওর প্রেরকযন্ত্র এবং মাইক্রোফোনে শব্দশক্তি তড়িৎশক্তিতে রূপান্তরিত করা হয়। টেলিফোন লাইনের মধ্যে দিয়ে তড়িৎ শক্তি প্রবাহিত হয়। এখানে উল্লেখ্য, টেলিফোন ও রেডিওর গ্রাহক যন্ত্রে তড়িৎ শক্তি শব্দ শক্তিতে রূপান্তরিত হয়।
তাপ শক্তির রূপান্তর: রেলগাড়ির স্টীম ইঞ্জিনে তাপ শক্তি যান্ত্রিক শক্তিতে রূপান্তরিত হয়। বাল্বের ফিলামেন্টে তাপ শক্তি আলোক শক্তিতে রূপান্তরিত হয়।
রাসায়নিক শক্তির রূপান্তর: কাঠ, কয়লা, পেট্রোল, কেরোসিন, গ্যাস ইত্যাদি পোড়ালে রাসায়নিক শক্তি তাপ ও আলোক শক্তিতে রূপান্তরিত করা হয়।
# বহুনির্বাচনী প্রশ্ন
কর্মদক্ষতা (Efficiency)
ইঞ্জিনে যতটুকু শক্তি পাওয়া যায় তাকে কার্যকর শক্তি বলে। কোনো যন্ত্রের কর্মদক্ষতা বলতে যন্ত্র থেকে মোট যে কার্যকর শক্তি পাওয়া যায় এবং মোট যে শক্তি দেওয়া হয়েছে তার অনুপাতকে বুঝায়।
কর্মদক্ষতা = কার্যকর শক্তি/মোট প্রদত্ত শক্তি
কর্মদক্ষতাকে (গ্রীক-ইটা) দ্বারা প্রকাশ করা হয়। কর্মদক্ষতাকে সাধারণ শতকরা হিসাবে প্রকাশ করা হয়ে থাকে। কোনো যন্ত্রের কর্মদক্ষতা 90% বলতে কি বোঝায়, এই যন্ত্রে 100J শক্তি দেওয়া হলে যন্ত্র থেকে 90J কার্যকর শক্তি পাওয়া যাবে। বৈদ্যুতিক ইঞ্জিন সর্বাপেক্ষা বেশি দক্ষতাসম্পন্ন ইঞ্জিন।
# বহুনির্বাচনী প্রশ্ন
তরল: পদার্থ যখন তরল অবস্থায় থাকে তখন কণাগুলো তুলনামূলকভাবে কাছে হলেও একটা কণা অন্য কণার সাপেক্ষে নড়তে পারে, তাই সেগুলোর নির্দিষ্ট আয়তন থাকলেও কোনো নিয়মিত আকার নেই এবং তরল সহজেই প্রবাহিত হয়। তরল পদার্থকে যে পাত্রে রাখা হয় তরল পদার্থ সেই পাত্রের আকার ধারণ করে। তরল পদার্থের কণাগুলো কাছাকাছি থাকায় সেগুলোর মধ্যে ফাঁকা জায়গা নেই বলে চাপ দিয়ে সংকুচিত করা যায় না।
বায়বীয় পদার্থ: নির্দিষ্ট আকার বা আয়তন নেই, পাত্রকে সম্পূর্ণ পূর্ণ করে ।
# বহুনির্বাচনী প্রশ্ন
ঘনত্ব (Density)
বস্তুর একক আয়তনের ভরকে তার উপাদানের ঘনত্ব বলে। কোন বস্তুর ঘনত্ব বস্তুর উপাদান ও তাপমাত্রার উপর নির্ভর করে।
# বহুনির্বাচনী প্রশ্ন
কোনো পৃষ্ঠের একক ক্ষেত্রফলের উপর লম্বভাবে প্রযুক্ত বলের মানকে চাপ বলে। চাপের একক প্যাসকেল।
1 বায়ুমণ্ডলীয় চাপ = 101325 প্যাসকল।
চাপ = বল/ক্ষেত্রফল
প্যাসকেলের সূত্র: "পাত্রে আবদ্ধ তরল বা বায়বীয় পদার্থের কোন অংশের উপর বাইরে থেকে চাপ প্রয়োগ করলে সেই চাপ কিছুমাত্র না কমে তরল বা বায়বীয় পদার্থের সব দিকে সমানভাবে সঞ্চালিত হয় এবং তরল বা বায়বীয় পদার্থের সংলগ্ন পাত্রের গায়ে লম্বভাবে ক্রিয়া করে।" প্যাসকেলের সূত্রের উপর ভিত্তি করে হাইড্রোলিক প্রেস তৈরি করা হয়েছে।
কোনো নির্দিষ্ট স্থানে কোনো ব্যক্তির ওজন (বল) অপরিবর্তিত থাকে। শোয়া অবস্থায় শরীরের অধিক অংশ (ক্ষেত্রফল) পৃথিবীর সংস্পর্শে থাকে। ফলে বল অধিক ক্ষেত্রফলের মাধ্যমে পৃথিবীতে প্রযুক্ত হয়। এজন্য শোয়া অবস্থায় মানুষ সবচেয়ে কম চাপ দেয়। আবার দৌড়ানো অবস্থায় মানুষের একটি পা পৃথিবীর সংস্পর্শে থাকে। এখানে ব্যক্তির ওজন (বল) শুধু একটি পায়ের (স্বল্প ক্ষেত্রফলের) মাধ্যমে পৃথিবীতে প্রযুক্ত হয়। এজন্য দৌড়ানো অবস্থায় মানুষ পৃথিবীকে সবচেয়ে বেশি চাপ দেয়। বিভিন্ন অবস্থায় মানুষের চাপ প্রয়োগের ক্রম: দৌড়ানো > দাড়ানো > বসা > শোয়া।
# বহুনির্বাচনী প্রশ্ন
প্লবতা (Buoyancy)
কোনো বস্তু সম্পূর্ণ বা আংশিকভাবে কোনো স্থির তরল বা বায়বীয় পদার্থে নিমজ্জিত করলে তরল বা বায়বীয় পদার্থের চাপের জন্য বস্তু উপরের দিকে যে লব্ধি বল অনুভব করে, তাকে প্লবতা বলে। লবণাক্ত পানি সুস্বাদু পানি অপেক্ষা ভারী। এজন্য সাগরের পানির ঘনত্ব পুকুর, বিল, নদী বা সুইমিং পুলের পানির ঘনত্ব অপেক্ষা বেশি হয় এবং সাগরের পানি অপেক্ষাকৃত অধিক উর্ধ্বমুখী চাপ দেয়। সাগরের পানির প্লবতা অপেক্ষাকৃত বেশি বলে-
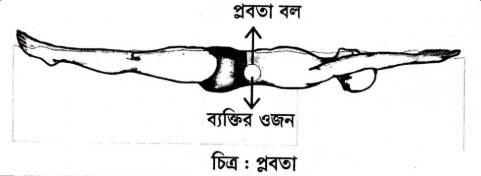
১. সাগরে সাঁতার কাটা পুকুর, বিল, নদী বা সুইমিং পুল অপেক্ষা সহজ।
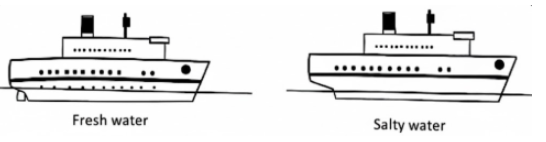
২. একটি জাহাজ সমুদ্র হতে নদীতে প্রবেশ করলে জাহাজের তল আরও ডুববে।
# বহুনির্বাচনী প্রশ্ন
পুকুরের পানিতে
নদীর পানিতে
সমুদ্রের পানিতে
সুইমিংপুলের পানিতে
আর্কিমিডিস এর নীতি (Archimedes' Principle)
আর্কিমিডিস একজন গ্রিক গণিতবিদ, পদার্থবিজ্ঞানী, প্রকৌশলী, জ্যোতির্বিদ এবং দার্শনিক। তিনি আনুমানিক ২৮৭ খ্রিষ্টপূর্বাব্দে গ্রিসের সিসিলি দ্বীপে জন্মগ্রহণ করেন। তিনি প্রমাণ করেন যে, “বস্তুকে কোনো স্থির তরল অথবা বায়বীয় পদার্থে আংশিক বা সম্পূর্ণ ডুবালে বস্তুটি কিছু ওজন হারায়। এই হারানো ওজন বস্তুটির দ্বারা অপসারিত তরল বা বায়বীয় পদার্থের ওজনের সমান।"
| বস্তুর ওজন > বস্তু দ্বারা অপসারিত তরলের ওজন | বস্তুটি ডুবে যাবে |
| বস্তুর ঘনত্ব > তরলের ঘনত্ব | |
| বস্তুর ওজন = বস্তু দ্বারা অপসারিত তরলের ওজন | বস্তুটি সম্পূর্ণভাবে নিমজ্জিত অবস্থায় ভাসবে |
| বস্তুর ঘনত্ব = তরলের ঘনত্ব | |
| বস্তুর ওজন < বস্তু দ্বারা অপসারিত তরলের ওজন | বস্তুটি ভাসবে |
| বস্তুর ঘনত্ব < তরলের ঘনত্ব |
আর্কিমিডিসের নীতির প্রয়োগের উদাহরণ
১. পানি বরফে পরিণত হলে এর আয়তন বেড়ে যায়। সুতরাং বরফের ঘনত্ব পানির ঘনত্বের চেয়ে কম আর তাই বরফ পানিতে ভাসে।
২. লোহা পানিতে ভাসে না কিন্তু লোহার তৈরি জাহাজ পানিতে ভাসে। আর্কিমিডিসের সূত্র দ্বারা জাহাজ পানিতে ভাসার কারণ ব্যাখ্যা করা যায়। লোহার টুকরা পানিতে ভাসে না কারণ লোহার খণ্ড দ্বারা অপসারিত পানির ওজন লোহা খণ্ডের ওজনের চেয়ে অনেক কম। কিন্তু লোহার তৈরি হলেও জাহাজ পানিতে ভাসে কারণ জাহাজের ভিতরটা ফাঁপা। ফলে জাহাজ যে আয়তনের পানি অপসারণ করে তার ওজন জাহাজের ওজনের চেয়ে বেশি হয়। এতে জাহাজ পানিতে নামালে প্রথমে ডুবতে শুরু করে। খানিকটা ডুবার পর যখন অপসারিত পানির ওজন জাহাজের ওজনের সমান হয় তখন জাহাজটি ভাসতে থাকে।
প্লিমসল লাইন (Plimsoll line)
প্লিমসল লাইন অতিরিক্ত মাল বোঝাই এড়ানোর জন্য জাহাজের গায়ে চিহ্নিত রেখাকে প্লিমসল লাইন বলে।
পৃষ্ঠটান (Surface Tension)
তরল মাত্রই একটি ধর্ম আছে - তরল পৃষ্ঠ সর্বদা সংকুচিত হয়ে সর্বনিম্ন ক্ষেত্রফলে আসতে চায়। তরলের মধ্যে যে বলের প্রভাবে এই বিশেষ ধর্ম প্রকাশ পায়, সেই বলকেই পৃষ্ঠটান বলে। তাপমাত্রা বাড়লে তরলের পৃষ্ঠটান হ্রাস পায়। আন্তর্জাতিক পদ্ধতিতে পৃষ্ঠটানের একক নিউটন/মিটার। তলীয় টানের জন্য পানির ছোট ফোঁটা বা বৃষ্টির ফোঁটা গোলাকৃতি হয়। পৃষ্ঠটানের জন্যই নদীর তীরে ভিজা বালুর উপর দিয়ে হেঁটে যাবার সাথে সাথে পদচিহ্ন মুছে যায়।
জেনে রাখা ভাল
১. কৈশিক চাপের কারণে কুপি হতে সলিতায় তেল আসে।
২. ডিম বক্র বহিরাবরণের কারণে ডিমকে দুই হাতে চেপে ভাঙ্গা যায় না।
# বহুনির্বাচনী প্রশ্ন
সান্দ্রতা
প্লবতা
তলীয়টান
পৃষ্ঠাটান
কৈশিক ক্রিয়া (Capillary action)
কৈশিক নল এর মধ্য দিয়ে তরলের উঠা বা নামা হল কৈশিক ক্রিয়া। কৌশিকী এর মাধ্যমে তরলের(যেমন পানি,তৈল ইত্যাদি) একটি অনুর উপর উঠে আসার সময় সংসক্তি বলের কারণে তার সাথে লেগে থাকা অন্য অনুটিয় উপরেও উঠে আসে। এ প্রক্রিয়ায় কুপি হতে সলিতায় তেল আসে।
সান্দ্রতা (Viscosity)
তরল পদার্থের অভ্যন্তরীণ ঘর্ষণের ফলে প্রবাহে (বয়ে যেতে) বাধা দেবার প্রবণতাকে সান্দ্রতা বলে। সান্দ্রতার একক Poise.
# বহুনির্বাচনী প্রশ্ন
চৌম্বকবিদ্যা
চৌম্বকবিদ্যা (Magnetism) হলো পদার্থবিজ্ঞানের একটি শাখা, যা চুম্বকের আকর্ষণ, বিকর্ষণ, চৌম্বক ক্ষেত্র এবং চৌম্বক পদার্থের ভৌত ধর্ম নিয়ে আলোচনা করে । এটি লোহা, নিকেল, কোবাল্ট ইত্যাদি পদার্থকে আকর্ষণ করে এবং এর উত্তর-দক্ষিণ মেরু থাকে । চলমান বৈদ্যুতিক চার্জ বা বিদ্যুৎ প্রবাহের কারণে এই ক্ষেত্র তৈরি হয় ।
# বহুনির্বাচনী প্রশ্ন
চৌম্বক এবং চুম্বকত্ত্ব (Magnetism and Magnetism)
যে বস্তু চৌম্বক ক্ষেত্র সৃষ্টি করে ফলে অন্য একটি চুম্বক বা চৌম্বক পদার্থের উপর বল প্রয়োগ করে তাকে চুম্বক বলে। চুম্বকের দুইটি বিশেষ ধর্ম রয়েছে। যথা:
১) আকর্ষণী ধর্ম (Property of attraction)
২) দিক নির্দেশক ধর্ম (Property of direction): চুম্বক মুক্ত অবস্থায় সবসময় উত্তর-দক্ষিণ (North-South) দিক বরাবর থাকে। চুষ্কীয় কম্পাসের সাহায্যে সহজেই দিক নির্ণয় করা যায়।
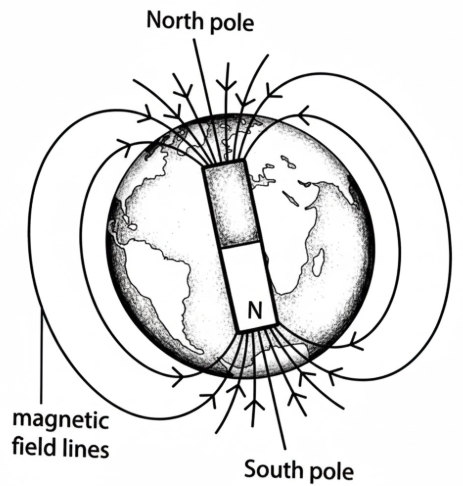
পৃথিবী একটি বিরাট চুম্বক
১৬০০ খি. ড. গিলবার্ট প্রথম বলেন, পৃথিবীও একটি বিরাট চুম্বক। ভূ-চুম্বকের উত্তর মেরু ভৌগোলিক দক্ষিণ মেরু হতে ২২০০ কিমি. পশ্চিমে অ্যান্টার্কটিকা মহাদেশের ভিক্টোরিয়া অঞ্চলে এবং ভূ-চুম্বকের দক্ষিণ মেরু ভৌগোলিক উত্তর মেরু হতে ২৫০০ কিমি. দূরে কানাডার বুথিয়া উপদ্বীপে অবস্থিত।
# বহুনির্বাচনী প্রশ্ন
পিতল
লৌহ
ইস্পাত
নিকেল
চৌম্বক পদার্থ (Magnetic material)
যে সকল পদার্থকে চুম্বক আকর্ষণ করে এবং যাদের চুম্বকে পরিণত করা যায়, তাদেরকে চৌম্বক পদার্থ বলে। যেমন: লোহা, লোহার যৌগ, লোহার সংকর ধাতু (যেমন- ইস্পাত), নিকেল এবং কোবাল্ট ইত্যাদি। যে সকল পদার্থকে চুম্বক আকর্ষণ করে না এবং যাদেরকে চুম্বকে পরিণত করা যায় না, তাদেরকে অচৌম্বক পদার্থ বলে। লোহা, ইস্পাত, নিকেল ও কোবাল্ট বাদে প্রায় সব অচৌম্বক পদার্থ। যেমনঃ সোনা, রূপা, তামা, পিতল, অ্যালুমিনিয়াম, দস্তা, টিন ইত্যাদি।
ক্যাসেট প্লেয়ারের টেপে চৌম্বক পদার্থ (যেমন- CrO2) ব্যবহার করা হয়। ক্যাসেটের ফিতায় শব্দ চৌম্বক ক্ষেত্র হিসেবে রক্ষিত থাকে।
# বহুনির্বাচনী প্রশ্ন
ডায়াচুম্বকীয় পদার্থ
প্যারাচুম্বকীয় পদার্থ
ফেরো চুম্বকীয় পদার্থ
অ্যান্টিফেরো চুম্বকীয় পদার্থ
চুম্বকের প্রকারভেদ (Types of magnets)
অস্থায়ী চুম্বক: চৌম্বক ক্ষেত্র অপসারিত হওয়ার সাথে সাথে যে কৃত্রিম চুম্বকের চুম্বকত্ব বিলুপ্ত হয়, তাকে অস্থায়ী চুম্বক বলে। সাধারণত কাঁচা লোহা, নিকেল ও লোহার সংকর ধাতু পারমালয় অস্থায়ী চুম্বক তৈরিতে ব্যবহৃত হয়। মটর, জেনারেটর, ট্রান্সফরমার ইত্যাদি তৈরিতে অস্থায়ী চুম্বক ব্যবহৃত হয়।
স্থায়ী চুম্বক: চৌম্বক ক্ষেত্র অপসারিত হলেও যে কৃত্রিম চুম্বকের চুম্বকত্ব সহজে বিলুপ্ত হয় না, তাকে স্থায়ী চুম্বক বলে। স্থায়ী চুম্বক তৈরিতে ইস্পাত, এলনিকো সংকর, ফেরাইট নামক যৌগিক পদার্থ ব্যবহৃত হয়।
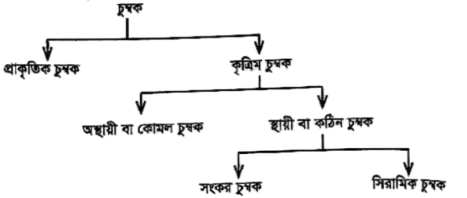
কলিং বেলে নরম লোহা ব্যবহার করা হয়, কারণ বিদ্যুৎ প্রবাহে নরম লোহা দ্রুত অস্থায়ী চুম্বকে পরিণত হতে পারে। টেপ রেকর্ডার এবং কম্পিউটারের স্মৃতির ফিতায় সিরামিক চুম্বক ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
শব্দ
পদার্থবিজ্ঞানে শব্দ হলো একধরনের কম্পন যা গ্যাস, তরল বা কঠিন মাধ্যমের সাহায্যে শব্দ তরঙ্গ হিসাবে সঞ্চালিত হয়।মানব শারীরতত্ত্ব এবং মনোবিজ্ঞানে শব্দ হলো একধরনের তরঙ্গের শ্রবণ এবং মস্তিষ্ক কর্তৃক এগুলো উপলব্ধি করা। যেসকল শব্দের কম্পাঙ্ক ২০ Hz থেকে ২০ kHz কম্পাঙ্ক সীমার মধ্যে অবস্থিত, কেবল সেই শব্দই মানুষের মধ্যে শ্রবণ অনুভূতি প্রকাশ করে। সাধারণ বায়ুমণ্ডলীয় চাপে ও বায়ু মাধ্যমে এই শব্দের তরঙ্গদৈর্ঘ্য ১৭ মিটার (৫৬ ফু) থেকে ১.৭ সেন্টিমিটার (০.৬৭ ইঞ্চি)। ২০ k Hz উপরের শব্দ তরঙ্গগুলি আল্ট্রাসাউন্ড বা শ্রবণাতীত শব্দ হিসাবে পরিচিত এবং এগুলো মানুষের কাছে শ্রবণীয় নয়। ২০ Hz নিচে শব্দ তরঙ্গগুলি ইনফ্রাসাউন্ড বা অবশ্রাব্য শব্দ হিসাবে পরিচিত। বিভিন্ন প্রজাতির প্রাণির শ্রবণসীমা বিভিন্ন হয়ে থাকে
তরঙ্গ হচ্ছে - যে পর্যাবৃত্ত আন্দোলন বা আলোড়নের সঞ্চালনের ফলে শক্তি এক স্থান থেকে আরেক স্থানে স্থানান্তরিত হয়। কিছু তরঙ্গ আছে যেগুলি সঞ্চালনের জন্য মাধ্যমের প্রয়োজন। আবার কিছু তরঙ্গ আছে যেগুলি সঞ্চালনের জন্য মাধ্যমের প্রয়োজন হয়না। এমনি দুইটি উদাহরণ হচ্ছে - শব্দ ও সূর্য থেকে পৃথিবীতে আসা শক্তি। শব্দ চলাচলের জন্য মাধ্যমের প্রয়োজন হলেও সূর্য থেকে যে শক্তি পৃথিবীতে আসে তা মাধ্যম ছাড়াই সঞ্চালিত হতে পারে। কেননা সূর্য থেকে পৃথিবীতে আসার সময় এই শক্তিকে এক বিশাল মাধ্যমহীন পথ অতিক্রম করে আসতে হয়।
# বহুনির্বাচনী প্রশ্ন
তরঙ্গ (Sound)
কোন স্থিতিস্থাপক জড় মাধ্যমের বিভিন্ন কণার সমষ্টিগত পর্যায়বৃত্ত কম্পনের ফলে মাধ্যমে যে আলোড়ন সৃষ্টি হয়, তাকে তরঙ্গ বলে। তরঙ্গ দুই প্রকার। যথা: লম্বিক বা অনুদৈর্ঘ্য তরঙ্গ এবং আড় বা অনুপ্রস্থ তরঙ্গ। শব্দ এক ধরনের অনুদৈর্ঘ্য তরঙ্গ।
তরঙ্গ বেগ (V) = তরঙ্গ দৈর্ঘ্য (V) কম্পাঙ্ক (f)
চাঁদে বায়ুমন্ডল নেই। তাই যদি চন্দ্রপৃষ্ঠে কোনো প্রচন্ড বিস্ফোরণ ঘটে তা পৃথিবীতে কখনও শোনা যাবে না। ভ্যাকুয়াম বা শূন্যের মধ্য দিয়ে শব্দ সঞ্চালিত হতে পারে না।
# বহুনির্বাচনী প্রশ্ন
1.11
0.707
0.637
1.414
শব্দ (Sound)
শব্দ শক্তির একটি বিশেষ তরঙ্গ রূপ যা আমাদের কানে শ্রবণের অনুভূতি জাগায়। বস্তুর কম্পনের ফলেই শব্দের উৎপত্তির হয়। কোনো একটি কম্পমান বস্তু বা কণা এক সেকেণ্ডে যতগুলো পূর্ণ কম্পন সম্পন্ন করে, তাকে তার কম্পাঙ্ক বলে। বস্তুর কম্পন হার্টস (Hz) এককে পরিমাপ করা হয়। মানবদেহে স্বরযন্ত্র শব্দ উৎপন্ন করে।
শব্দের যে বৈশিষ্ট্য দ্বারা কোন সুর চড়া ও কোন সুর মোটা তা বোঝা যায়, তাকে শব্দের তীক্ষ্ণতা বলে। শব্দের তীক্ষ্মতা বেল (Bel) বা ডেসিবেল (Decibel) এককে পরিমাপ করা হয়। শব্দের তীক্ষ্মতা ১০৫ ডিবি এর ওপরে মানুষ বধির হতে পারে। শব্দের তীক্ষ্ণতা শব্দ তরঙ্গের বিস্তার (Wave amplitude) উপর নির্ভর করে। একটি শূন্য পাত্রকে আঘাত করলে ভরা পাত্রের চেয়ে বেশি শব্দ হয়, কারণ শূন্য পাত্রে বাতাসে শব্দ তরঙ্গের বিস্তার বেশি হয়।
লোকভর্তি হল ঘরে শূন্যঘরের চেয়ে শব্দ ক্ষীণ হয় কারণ শূন্য ঘরে শব্দের শোষণ কম হয়। বাদ্যযন্ত্রসমূহ ফাঁকা থাকে কারণ ফাঁপা বাক্সের বায়ুতে অনুনাদ সৃষ্টি হয়ে শব্দের প্রাবল্য বৃদ্ধি পায়।
# বহুনির্বাচনী প্রশ্ন
20 Hz থেকে 200 Hz
20 Hz থেকে 2000 Hz
20 Hz থেকে 20000 Hz
20 Hz থেকে 200000 Hz
৭৫ ডিবি
৯০ ডিবি
১০৫ ডিবি
১২০ ডিবি
শব্দকে নিয়ন্ত্রণ করা
ধোয়া নির্গমণ করা
বায়ু দূষণমুক্ত করা
ইঞ্জিনের গরম বাতাস বেরে করা
শব্দের যে বৈশিষ্ট্য দ্বারা কোন সুর চড়া ও কোন সুর মোটা বুঝা যায় তাকে তীক্ষ্ণতা বলে। শব্দের তীক্ষ্ণতা শব্দ সৃষ্টিকারী বস্তুর কম্পাঙ্ক ও দৈর্ঘ্যের উপর নির্ভর করে। দৈর্ঘ্য বৃদ্ধি পেলে তীক্ষ্ণতা কমে এবং দৈর্ঘ্য কমলে তীক্ষ্ণতা বৃদ্ধি পায়। 'কাজেই বাঁশের বাঁশির দৈর্ঘ্য কম হলে শব্দের তীক্ষ্ণতা বৃদ্ধি পাবে।
# বহুনির্বাচনী প্রশ্ন
৭৫ ডিবি
৯০ ডিবি
১০৫ ডিবি
১২০ ডিবি
৩৭ ডেসিবেল
৯৫ ডেসিবেল
১০৫ ডেসিবেল
১২৫ ডেসিবেল
শব্দ সঞ্চারণ (Propagation of Sound)
শব্দ বিস্তারের জন্য স্থিতিস্থাপক মাধ্যমের প্রয়োজন হয়। শব্দের উৎস এবং আমাদের কানের মধ্যবর্তী স্থানে যদি কোনো স্থিতিস্থাপক জড় মাধ্যম না থাকে তাহলে শব্দ আমাদের কানে পৌছাতে পারে না। চাঁদে বায়ুমণ্ডল নেই। তাই যদি চন্দ্রপৃষ্ঠে কোনো প্রচণ্ড বিস্ফোরণ ঘটে তা পৃথিবীতে কখনও শোনা যাবে না। ভ্যাকুয়াম বা শূন্যর মধ্য দিয়ে শব্দ সঞ্চালিত হতে পারে না।
# বহুনির্বাচনী প্রশ্ন
শব্দের দ্রুতি (Speed of Sound)
শব্দ প্রতি সেকেন্ডে যে দূরত্ব অতিক্রম করে তাকে শব্দের গতি বা দ্রুতি বলে। বাতাসে শব্দের দ্রুতি সেকেন্ডে ৩৩২ মিটার বা ঘণ্টায়। কঠিন মাধ্যমে (যেমন- ইস্পাত, লোহা প্রভৃতি) শব্দ সবচেয়ে দ্রুত চলে, তরল মাধ্যমে (যেমন- পানি) তার চেয়ে ধীরে চলে। বায়বীয় মাধ্যমে শব্দের দ্রুতি সবচেয়ে কম আর ভ্যাকুয়াম বা শূন্যে শব্দের দ্রুতি শূন্য। বিভিন্ন মাধ্যম শব্দের বেগের ক্রম -
কঠিন > তরল > বায়বীয়
লোহার মধ্য শব্দ বাতাসের চেয়ে ১৫গুণ দ্রুত চলে। পানির মধ্যে শব্দ বাতাসের চেয়ে চারগুণ দ্রুত চলে। তাই কেউ পানিতে ডুব দিয়ে হাততালি দিলে, সেই তালির শব্দ ডুবন্ত অবস্থায় থাকা ব্যক্তি জোরে শুনতে পাবে। অনুরূপভাবে, সমুদ্রের তীরে একটা বিস্ফোরণ ঘটলে এক কিলোমিটার দূরে সমুদ্রের পানির নিচে অবস্থানকারী ব্যক্তি একই দূরত্বে সমুদ্রে বা ভূমিতে অবস্থানকারী ব্যক্তি অপেক্ষা আগে শুনতে পাবে।
0°C তাপমাত্রায় এবং স্বাভাবিক চাপে-
মাধ্যম | শব্দের দ্রুতি |
| লোহা | ৫২২১ মি./সে |
| ৭৫৭ মাইল/ঘণ্টা | |
| পানি | ১৪৫০ মি./সে |
| শুষ্ক বায়ু | ৩৩২ মি./সে |
শব্দের দ্রুতি নিম্নোক্ত নিয়ামকের উপর নির্ভরশীল। যথা-
ক) তাপমাত্রা: তাপমাত্রা বৃদ্ধি পেলে শব্দের বেগ বৃদ্ধি পায়। ১ সে. বা ১ কেলভিন তাপমাত্রা বৃদ্ধিতে বাতাসে শব্দের বেগ প্রায় ০.৬ মি./সে. বৃদ্ধি পায়। শীতকালের চেয়ে গ্রীষ্মকালে বায়ুর উষ্ণতা বেশি থাকে বলে শীতকালের চেয়ে গ্রীষ্মকালে বায়ুতে শব্দের বেগ বেশি হয়।
খ) আর্দ্রতা: বাতাসের আর্দ্রতা বেড়ে গেলে শব্দের বেগ বেড়ে যায়। বায়ুর আর্দ্রতা বেশি থাকে বলে বর্ষাকালে শব্দ দ্রুততর চলে।
বজ্রপাতের সময় আলোর ঝলক দেখার বেশ কিছু সময় পরে মেঘের গর্জন শোনা যায়। গর্জন এবং আলোর ঝলক একই সাথে ঘটে কিন্তু শব্দের চাইতে আলোর গতি অনেক বেশি। মধ্যকার দূরত্ব অতিক্রম করতে আলোর চেয়ে শব্দের বেশি সময় লাগে। ফলে আলোর ঝলক দেখার বেশ কিছু সময় পরে মেঘের গর্জন শোনা যায়। যে বিমান শব্দের চেয়ে বেশি দ্রুতগতিতে চলে, তাকে বলা হয় সুপারসনিক বিমান। যেমন: কনকর্ড একটি যাত্রীবাহী সুপারসনিক বিমান।
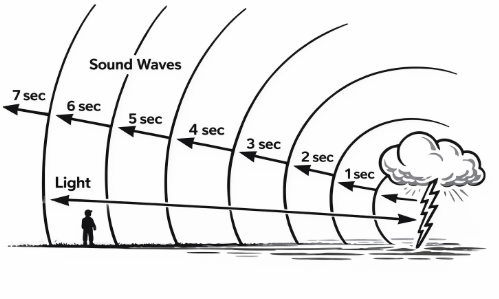
চিত্র: বিদুৎ চমকানোর সময় আলোর এবং শব্দের তুলনামূলক গতি
# বহুনির্বাচনী প্রশ্ন
প্রতিধ্বনি (Echo)
কোনো উৎস থেকে সৃষ্ট শব্দ যখন দূরবর্তী কোন মাধ্যমে বাধা পেয়ে উৎসের কাছে ফিরে আসে তখন মূল ধ্বনির যে পুনরাবৃত্তি হয় তাকে শব্দের প্রতিধ্বনি বলে। এককথায়, প্রতিফলিত শব্দকে বলা হয় প্রতিধ্বনি। কোন শব্দ শোনার পর প্রায় ০.১ সেকেন্ড পর্যন্ত এর রেশ আমাদের মস্তিষ্কে থাকে। এই সময়কে শব্দানুভূতির স্থায়িত্বকাল বলে। শব্দের প্রতিধ্বনি শোনার জন্য উৎস ও প্রতিফলকের মধ্যবর্তী দূরত্ব ন্যূনতম ১৬.৬ মিটার হওয়া প্রয়োজন। শব্দের প্রতিধ্বনি ব্যবহার করে সমুদ্র ও কুয়ার গভীরতা নির্ণয় করা যায়।
# বহুনির্বাচনী প্রশ্ন
শ্রাব্যতার পাল্লা এবং শব্দোত্তর ও শব্দেতর তরঙ্গ
Audibility range and Ultrasonic & Infrasonic waves
উৎসের কম্পাঙ্ক ২০ Hz থেকে ২০,০০০ Hz এর মধ্যে সীমিত থাকলেই কেবল মানুষ তা শুনতে পায়। এক শ্রাব্যতার পাল্লা বলে। যে তরঙ্গের কম্পাঙ্ক ২০,০০০ Hz এর চেয়ে বেশি, তাকে শব্দোত্তর (আল্ট্রাসনিক) তরঙ্গ বলে। আর কম্পাঙ্ক ২০ Hz এর চেয়ে কম তাকে শব্দেতর (ইনফ্রাসনিক) তরঙ্গ বলে। কোনো কোনো জীবজন্তু আল্ট্রাসনিক শব্দ শুনতে পায়। যেমন: কুকুরের শ্রাব্যতার ঊর্ধ্বসীমা প্রায় ৩৫,০০০ Hz এবং বাদুড়ের প্রায় ১,০০,০০০ Hz। বাদুড় চোখে দেখতে পারেনা। বাদুড় চলার সময় বিভিন্ন কম্পাঙ্কের শব্দোত্তর তরঙ্গ সৃষ্টি করে। বাদুড় তার সৃষ্ট শব্দোত্তর তরঙ্গের প্রতিধ্বনি শুনে প্রতিবন্ধকের অবস্থান এবং প্রকৃতি সম্বন্ধে ধারণা লাভ করে এবং পথ চলার সময় সেই প্রতিবন্ধকপরিহার করে। কোয়ার্টজ ক্রিস্টাল অসিলেটরের মাধ্যমে শব্দোত্তর তরঙ্গ উৎপন্ন করা যায়।
শব্দোত্তর তরঙ্গের ব্যবহার
১. রোগ নির্ণয় এবং চিকিৎসার ক্ষেত্রে শব্দোত্তর তরঙ্গ। আলট্রাসনোগ্রাফি হলো ছোট তরঙ্গ দৈর্ঘ্যের শব্দ ব্যবহার করে ইমেজিং।
২. সমুদ্রের গভীরতা নির্ণয়, হিমশৈল, ডুবোজাহাজ ইত্যাদির অবস্থান নির্ণয়।
৩. সূক্ষ্ম ইলেকট্রনিক যন্ত্রপাতি পরিষ্কার করার কাজে।
ডপলার ক্রিয়া বা প্রভাব (Doppler Effect)
শব্দের উৎস ও শ্রোতার মধ্যে আপেক্ষিক গতি বিদ্যমান থাকলে শ্রোতার নিকট উৎস হতে নিঃসৃত শব্দের তীক্ষ্ণতা বা কম্পাঙ্কের যে আপাত পরিবর্তন পরিলক্ষিত হয়, তাকে ডপলার ক্রিয়া বা প্রভাব বলে। ডপলার ক্রিয়ার ক্ষেত্রে নিম্নোক্ত তিনটি বিষয় বিবেচনা করা হয়-
ক) উৎস গতিশীল কিন্তু শ্রোতা স্থির
- উৎস শ্রোতার দিকে অগ্রসর হলে শব্দের কম্পাঙ্ক প্রকৃত কম্পাঙ্কের চেয়ে বেশি হবে।
- উৎস শ্রোতার থেকে দূরে সরে গেলে শব্দের আপাত কম্পাঙ্ক প্রকৃত কম্পাঙ্কের চেয়ে কম হবে।
খ) উৎস স্থির কিন্তু শ্রোতা গতিশীল
- শ্রোতা উৎসের দিকে অগ্রসর হলে শব্দের আপাত কম্পাঙ্ক প্রকৃত কম্পাঙ্কের চেয়ে বেশি হবে।
- শ্রোতা উৎসের থেকে দূরে সরে গেলে শব্দের আপাত কম্পাঙ্ক প্রকৃত কম্পাঙ্কের চেয়ে কম হবে।
গ) উৎস ও শ্রোতা উভয়ই গতিশীল
উৎস ও শ্রোতার মধ্যে আপেক্ষিক গতিবেগ না থাকলে কম্পাঙ্কের কোন পরিবর্তন হয়না। রেলওয়ে স্টেশনে আগমনরত ইঞ্জিনে বাঁশি বাজাতে থাকলে প্লাটফর্মে দাঁড়ানো ব্যক্তির কাছে বাঁশির কম্পনাঙ্ক আসলের চেয়ে বেশি হবে।
তাপ ও তাপগতিবিদ্যা
তাপ ও তাপগতিবিদ্যা পদার্থবিজ্ঞানের একটি গুরুত্বপূর্ণ শাখা, যা তাপশক্তি, তাপমাত্রা, কার্য এবং শক্তির স্থানান্তর নিয়ে আলোচনা করে। তাপ এক প্রকার শক্তি যা তাপমাত্রার পার্থক্যের কারণে প্রবাহিত হয় (SI একক জুল, J) ।
# বহুনির্বাচনী প্রশ্ন
তাপ (Heat)
তাপ এক প্রকার শক্তি যা ঠাণ্ডা বা গরমের অনুভূতি জাগায়।
একক: তাপ শক্তির একটি রূপ। তাই আন্তর্জাতিক (S.I) পদ্ধতিতে তাপের একক জুল (J)। সিজিএস পদ্ধতিতে তাপের একক ক্যালরি। এক গ্রাম পানির তাপমাত্রা 1° সেলসিয়াস বৃদ্ধির জন্য যে পরিমাণ তাপের প্রয়োজন, তাকে 1 ক্যালরি তাপ বলে।
1 ক্যালরি (cal) =4.2 জুল (j)
# বহুনির্বাচনী প্রশ্ন
তাপমাত্রা বা উষ্ণতা ( Temperature)
তাপমাত্রা হচ্ছে কোন বস্তুর তাপীয় অবস্থা যা নির্ধারণ করে ঐ বস্তুটি অন্য বস্তুর তাপীয় সংস্পর্শে এসে বস্তুটি তাপ গ্রহণ করবে না বর্জন করবে।
একক: আন্তর্জাতিক পদ্ধতিতে (SI) তাপমাত্রার একক কেলভিন (K)। সিজিএস পদ্ধতিতে উষ্ণতার একক হলো ডিগ্রি সেলসিয়াস (C)।
সেলসিয়াস, ফারেনহাইট এবং কেলভিন স্কেলের মধ্য সম্পর্ক
সেন্টিগ্রেড স্কেলে তাপমাত্রার পরিবর্তন = কেলভিন স্কেলে তাপমাত্রার পরিবর্তন। উদাহরণ: সেন্টিগ্রেড স্কেলে তাপমাত্রা 15° পরিবর্তিত হলে কেলভিন স্কেলে 15° তাপমাত্রা পরিবর্তিত হয়।
তাপমাত্রার বিভিন্ন স্কেলের তুলনামূলক চিত্র
স্কেলের নাম | সংকেত | নিম্ন স্থিরাঙ্ক | উর্ধ্ব স্থিরাঙ্ক |
বরফের গলনাংক | পানির স্ফুটনাংক | ||
| সেলসিয়াস/সেন্টিগ্রেড | C | 0° | 100° |
| ফারেনহাইট | F | 32° | 212° |
| কেলভিন | K | 273° | 373° |

# বহুনির্বাচনী প্রশ্ন
পরম শূন্য তাপমাত্রা ( Absolute zero temperature)
যে তাপমাত্রায় কোনো গ্যাসের আয়তন শূন্য হয়ে যায়, তাকে পরম শূন্য তাপমাত্রা বলে। - ২৭৩০ সেন্টিগ্রেড তাপমাত্রাকে পরম শূন্য তাপমাত্রা বলা হয়। পরমশূন্য তাপমাত্রাকে সর্বনিম্ন তাপমাত্রা বা চরম শূন্য তাপমাত্রা বা চরম শীতলতাও বলা হয়।
0° সেলসিয়াস = - 273° কেলভিন = 459.4° ফারেনহাইট
তাপমাত্রার কেলভিন স্কেলে 'শূন্য' ডিগ্রি সবচেয়ে বেশি ঠাণ্ডা।
# বহুনির্বাচনী প্রশ্ন
প্রমাণ তাপমাত্রা এবং চাপ (Standard Temperature and Pressure)
০°C তাপমাত্রা বা ২৭৩K তাপমাত্রাকে প্রমাণ তাপমাত্রা বলে। ৭৬৯ মিলিমিটার বা ৭৬ সেন্টিমিটার পারদচাপকে প্রমাণ চাপ বলে।
NTP = Normal Temperature & Pressure
# বহুনির্বাচনী প্রশ্ন
হৃৎপিণ্ডের প্রসারণ চাপ
হৃৎপিণ্ডের সংকোচন চাপ
উভয়টিই
কোনোটিই নয়
স্ফিগমোম্যানোমিটার
থার্মোমিটার
ম্যানোমিটার
ব্যারোমিটার
ক্লিনিক্যাল থার্মোমিটার (Clinical Thermometer)
যে থার্মোমিটারের সাহায্যে শরীরের তাপমাত্রা মাপা হয় তাকে ক্লিনিক্যাল থার্মোমিটার বলে। এই থার্মোমিটারে ফারেনহাইট (F) স্কেল ব্যবহার করা হয়। ক্লিনিক্যাল থার্মোমিটারে 95 - 110° ফা. পর্যন্ত দাগ কাঁটা থাকে। মানব দেহের স্বাভাবিক উষ্ণতা 98.4° ফারেনহাইট বা 36.9° সেলসিয়াস।

পদার্থের তাপজনিত প্রসারণ (Thermal Expantion of Material)
কঠিন পদার্থের পদার্থের প্রসারণ তিন প্রকার হয়; যথা- দৈর্ঘ্য প্রসারণ, ক্ষেত্র প্রসারণ এবং আয়তন প্রসারণ। কিন্তু তরল এবং বায়বীয় পদার্থের প্রসারণ বলতে এদের আয়তন প্রসারণকে বুঝায়। সামান্য কিছু ব্যতিক্রম ছাড়া সকল পদার্থই তাপ প্রয়োগে প্রসারিত এবং তাপ অপসারণ করলে সংকুচিত হয়। গ্যাসীয় পদার্থের চেয়ে তরল পদার্থের প্রসারণ অপেক্ষাকৃত কম এবং কঠিন পদার্থের প্রসারণ হয় সবচেয়ে কম। তাপ প্রয়োগে পদার্থের প্রসারণের ক্রম: বায়বীয় পদার্থ > তরল পদার্থ > কঠিন পদার্থ ।
প্রসারণের কয়েকটি উদাহরণ
১. মাঝখানে গোলাকার ছিদ্রবিশিষ্ট একটি প্লেটকে উত্তপ্ত করলে প্লেটের প্রসারণের ফলে মাঝখানের ছিদ্রটির ব্যাস কমবে।
২. পুরু কাচের গ্লাসে গরম পানীয় ঢাললে গ্লাসটি ফেটে যায়। গ্লাসে গরম পানীয় ঢালার ফলে ঐ গ্লাসের ভিতরের অংশ গরম পানির সংস্পর্শে প্রসারিত হয়। কিন্তু কাচ তাপর কুপরিবাহক বলে ঐ তাপ বাহিরের অংশে সঞ্চালিত হতে পারে না। তাই ভিতরের অংশ প্রসারিত হলেও বাহিরের অংশ প্রসারিত হতে পারে না। ফলে গ্লাসের ভিতর ও বাহিরে অসম আয়তন প্রসারণের জন্য গ্লাসটি ফেটে যায়।
৩. সূর্যের তাপে বা যখন ট্রেন চলে তখন চাকার ঘর্ষণের ফলে উৎপন্ন তাপে রেললাইন প্রসারিত হয়। ফিসপ্লেট দ্বারা রেললাইনের দুইটি রেলকে সংযুক্ত করা হলেও দুটি রেলের সংযোগস্থলে ফাঁক রাখা হয়, যাতে রেললাইন প্রসারণের জন্য যথেষ্ট জায়গা পায়। এরূপ ফাঁক না রাখলে এই প্রসারণের ফলে লাইন বেঁকে গিয়ে মারাত্মক দুর্ঘটনা ঘটার সম্ভাবনা থাকে।
৪. বিদ্যুৎ ও টেলিফোনের তার ঝুলিয়ে টানা হয়। কারণ তাপমাত্রা হ্রাস পেলে ধাতব তার সঙ্কুচিত হয়। তারগুলো যদি টান টান থাকে তাহলে শীতকালে সঙ্কোচনের ফলে ছিড়ে যেতে বা পোস্ট ভেঙ্গে যেতে পারে, তাই তারগুলো ঢিলা রাখা হয় যেন ছিঁড়ে না যায়।
৫. একখণ্ড পাথরকে উত্তপ্ত করলে পাথরের ভেতরের অংশ থেকে বাহিরের আবরণ বেশি উত্তপ্ত ও প্রসারিত হয়, তাই ফেটে যায়।
পানির ব্যতিক্রমী প্রসারণ (Anomalous expansion of water)
তরল পদার্থে তাপ প্রয়োগ করলে তার আয়তন বাড়ে, তাপ অপসারণ করলে আয়তন কমে। কিন্তু ০° সে. তাপমাত্রার পানিকে উত্তপ্ত করলে এর আয়তন বাড়ে না বরং কমে। ৪° সে. তাপমাত্রা পর্যন্ত এরূপ ঘটে। ৪° সে. তাপমাত্রার পানিতে গরম বা ঠাণ্ডা যাই করা হোক না কেন তা প্রসারিত হয়। এটি তরল পদার্থের প্রসারণের সাধারণ নিয়মের ব্যতিক্রম। তাই পানির এ প্রসারণকে ব্যতিক্রমী প্রসারণ বলে। ৪° সেলসিয়াল উষ্ণতায় পানির ঘনত্ব তাই সবচেয়ে বেশি। পানির এ ব্যতিক্রমী প্রসারণের জন্য শীতপ্রধান দেশে পুকুর, নদী বা সাগরের জলজ জীবেরা বেচে থাকতে পারে। পানির ব্যতিক্রমী প্রসারণের জন্য পুকুর, নদী বা সাগরের সমস্ত পানি জমে বরফ হয়ে যায় না। উপরে বরফ জমে গেলেও নিচে ৪° সে. তাপমাত্রার পানি থেকে যায় বলে জলজ জীবের পক্ষে বেচে থাকা সম্ভব হয়।
# বহুনির্বাচনী প্রশ্ন
ঘনত্ব বেড়ে যাবে
আয়তন বেড়ে যাবে
ভর কমে যাবে
আয়তনের পরিবর্তন ঘটবে না
গলনাঙ্কের উপর চাপের প্রভাব (Effect of pressure on Melting point)
তাপ প্রয়োগে কোনো কঠিন পদার্থ তরলে পরিণত হওয়াকে গলন বলে। কোনো কঠিন পদার্থকে তাপ দিলে প্রথমে তার উষ্ণতা বাড়তে থাকে। একটি নির্দিষ্ট উষ্ণতায় কঠিন পদার্থ গলতে শুরু করে। যতক্ষণ পর্যন্ত সমস্ত কঠিন পদার্থ তরলে পরিণত না হয় ততক্ষণ পর্যন্ত এ উষ্ণতা স্থির থাকে। এ নির্দিষ্ট উষ্ণতাকে কঠিন পদার্থের গলনাঙ্ক বলে। যেমন: স্বাভাবিক বায়ুমণ্ডলীয় চাপে বরফের গলনাঙ্ক ০° সেলসিয়াস বা ৩২° ফারেনহাইট।
অধিকাংশ পদার্থের কঠিন অবস্থা থেকে তরল অবস্থায় রূপান্তরের সময় আয়তন বৃদ্ধি পায়। পক্ষান্তরে তরল অবস্থা থেকে কঠিন অবস্থায় রূপান্তরের সময় আয়তন কমে যায়। তবে কিছু কিছু ক্ষেত্রে ব্যতিক্রমও দেখা যায়। যেমন: বরফ ( পানি), ঢালাই,লোহা,পিতল,বিসমাথ,অ্যান্টিমনি ইত্যাদি। এসব পদার্থ কঠিন থেকে তরল অবস্থায় রূপান্তরিত হলে আয়তন কমে যায় আর তরল অবস্থা থেকে কঠিন অবস্থায় রূপান্তরের সময় আয়তন বেড়ে যায়। কঠিন হতে তরলে রপান্তরের সময় যেসব পদার্থের আয়তন বৃদ্ধি পায়, চাপ বাড়লে ঐই সকল পদার্থ গলনাঙ্ক বেড়ে যায়। আর যেসব পদার্থ কঠিন হতে তরলে রূপান্তরের সময় আয়তন হ্রাস পায়,চাপ বাড়ালে ঐই সকল পদার্থ গলনাঙ্ক কমে যায়।
# বহুনির্বাচনী প্রশ্ন
পুন:শিলীভবন (REGELATION)
দুই টুকরো বরফে একত্রে ধীরে চাপ দিলে ওরা জোড়া লেগে যায়। যখন বরফ টুকরো দুইটির উপর চাপ দেয়া হয়, তখন তাদের সংযোগস্থলে গলনাঙ্ক ০° সে. এর নিচে নেমে আসে। কিন্তু সংযোগস্থলের তাপমাত্রা ০° থাকায় ঐ জায়গায় বরফ গলে যায়। এখন যেই চাপ অসাধারণ করা হয়, তখন গলনাঙ্ক আবার ০° সে. এ চলে আসে; ফলে সংযোগস্থলের বরফ গলা পানি জমাট বেধে টুকরো দুটিকে জুড়ে দেয়। এভাবে চাপ দিয়ে কঠিন বস্তকে তরলে পরিণত করে ও চাপ হ্রাস করে আবার কঠিন অবস্থায় আনাকে পুনঃশিলীভবন বলে।
স্ফুটনাঙ্কের উপর চাপের প্রভাব (Effect of pressure on Boiling point)
তাপ দিলে তরল পদার্থের উষ্ণতা বাড়তে শুরু করে। একটি নির্দিষ্ট উষ্ণতায় তরল পদার্থ ফুটতে শুরু করে এবং বাষ্পে পরিণত হতে থাকে। যতক্ষণ পর্যন্ত সম্পূর্ণ তরল বাষ্পে পরিণত না হয় ততক্ষণ ঐ উষ্ণতা স্থির থাকে। ঐ নির্দিষ্ট উষ্ণতাকে তরল পদার্থের স্ফুটনাংক বলে। যেমন: স্বাভাবিক বায়ুমণ্ডলীয় চাপে পানির স্ফুটনাংক ১০০° সেলসিয়াস বা ২১২° ফারেনহাইট। স্ফুটন শুরু হওয়ার পর ৩০ মিনিট ধরে স্ফুটন করলে পানি জীবাণুমুক্ত হয়।
খোলা পাত্রে রাখা তরলের ওপরে কিছু বাষ্প থাকে । পাত্রটি যদি শূন্যস্থানে থাকত তাহলে তরলের উপরিস্থিতি বাষ্পকে ঠেকিয়ে রাখার মতো কোনো চাপ থাকত না, ফলে সমস্ত তরল বাষ্প হয়ে যেত। কিন্তু বাস্তবে বায়ুচাপ তরলের বাষ্প অনুগুলোকে ছড়িয়ে পড়তে দেয়না। কক্ষ তাপমাত্রা পানির বাষ্পচাপ বায়ুর চাপের তুলনায় কম হয়, এই কারণে পানির বাষ্প বায়ুর অনুগুলোকে সরিয়ে মুক্ত হতে পারে না কিন্তু তাপমাত্রা যতই বাড়ানো হয়, পানির গড়গতি শক্তি বৃদ্ধি পায় অর্থাৎ আরও বেশি সংখ্যক অনু বাষ্পে যেতে পারে। এইভাবে যতই তরলের বাষ্প মুক্ত হতে থাকে, তরলস্থিত বাতাসের অনুগুলোকে সরিয়ে মুক্ত হতে পারে। এইভাবে যতই তরলের বাষ্প মুক্ত হতে থাকে, তরলস্থিত অনুও একটি নির্দিষ্ট তাপমাত্রায়। সেই তাপমাত্রাকে তরলের স্ফুটনাঙ্ক বলে। এজন্য চাপ বাড়ালে তরলের স্ফুটনাঙ্ক বেড়ে যায় এবং চাপ কমলে স্ফুটনাঙ্ক কমে যায়। স্বাভাবিক বায়ুমন্ডলীয় চাপে পানির স্ফুটনাঙ্ক ১০০° সে.। কিন্তু বায়ুর চাপ কম থাকায় এভারেস্ট পর্বতের উপর পানির স্ফুটনাঙ্ক কম বলে কম তাপমাত্রায় পানি ফুটতে শুরু করে, কিন্তু মাছ,মাংস,ডিম প্রভৃতি দ্রুত সিদ্ধ হয়না। এজন্য সুউচ্চপাহাড় বা পরবর্তের চূড়ায় রান্না করা দূরহ হয়ে পড়ে। ঢাকনা দেয়া পাত্র বা প্রেসার কুকার ব্যবহার করে এই অসুবিধা কাটানো যায়। প্রেসার কুকার উচ্চটাপে পানি স্ফুটনাঙ্ক বৃদ্ধি পায়। ফলে রান্না তাড়াতাড়ি হয়। পৃথিবীপৃষ্ঠ হতে যত উপরে উঠা যায় তত বায়ুর চাপ কমতে থাকে । কাজেই উপরে উঠলে দেহের ভেতরের চাপ বাহিরের বায়ুর চাপ অপেক্ষা অধিক হলে দেহের রক্তনালীতে প্রচন্ড চাপ পড়ে। এ চাপে নাক – মুখ দিয়ে রক্ত বের হয়ে আসে। এ জন্য পর্বত আরোহীকে আটসাট পোশাক পরিধান করতে হয়।
সমুদ্রতলে এবং ভূ-পৃষ্ঠ হতে ২ মাইল উঁচুতে (যেমন- পাহাড়ে) বায়ুতে অক্সিজেনের শতকরা সঙযুক্তি প্রায় সমান (২১%)। কিন্তু ভূ-পৃষ্ঠ হতে ২ মাইল বায়ুমন্ডলীয় চাপ সমুদ্রতলের বায়ুমন্ডলীয় চাপ অপেক্ষা ৩০% কম অর্থাৎ উঁচু স্থানে বায়ুর অণুসমূহ পরস্পর হতে দূরে অবস্থান করে চাপ কম হওয়ায় বায়ু হতে কম অক্সিজেন শরীরের রক্তনালীতে প্রবেশ করে। ফলে শ্বাস কষ্ট হয়। এজন্য পর্বত আরোহীরা উঁচু পর্বতে উঠতে গেলে সিলিন্ডারে করে অক্সিজেন নিয়ে যায়।
# বহুনির্বাচনী প্রশ্ন
ঠিক থাকে
বেশি হয়
কম হয়
কোনোটিই নয়
বাষ্পীভবন (Vaporization)
কোনো পদার্থের তরল অবস্থা থেকে বায়বীয় অবস্থায় পরিবর্তনকে বাষ্পীভবন বলে। সাধারণত দুভাবে বাষ্পীভবন সংঘটিত হয়। যথা- (ক) স্বতঃবাষ্পীভবন (Evaporation) (খ) স্ফুটন (Boiling)
বাষ্পীভবনের কয়েকটি উদাহরণ
১. মাটির কলসীর গায়ে অসংখ্য ক্ষুদ্র ক্ষুদ্র ছিদ্র থাকে। এসব ছিদ্র দিয়ে পানি কলসীর উপরিতলে এসে পৌঁছে এবং পানি বাষ্পায়ন ঘটে। বাষ্পায়নের প্রয়োজনীয় সুপ্ততাপ কলসীর পানি হতে গৃহীত হয়। ফলে তাপ হারিয়ে কলসীর পানি শীতল হয়।
২. ফ্যান চালালে আমরা ঠাণ্ডা অনুভব করি কারণ ফ্যান শরীর থেকে বাষ্পীভবনের হার বাড়িয়ে দেয়।
৩. ভিজাকাপড় গায়ে রাখলে কাপড়ের পানি ধীরে ধীরে বাষ্পীভূত হতে থাকে। এ বাষ্পীভবনের জন্য প্রয়োজনীয় সুপ্ততাপ শরীর হতে গৃহীত হয়। ফলে শরীরের তাপমাত্রা কমে যায়। বেশিক্ষণ শরীরে বাষ্পীভবন হলে শরীর ঠাণ্ডা হয়ে যায় এবং সর্দি হওয়ার সম্ভাবনা থাকে।
# বহুনির্বাচনী প্রশ্ন
সমুদ্রের তেল উত্তোলনে
সমুদ্রের তেল অপসারণে
সমুদ্রের গর্তীরতা নির্ণয়ে
সমুদ্রের সীমানা নির্ণয়ে
তাপ সঞ্চালন (Transmission of Heat)
তাপ সঞ্চালন হল তাপের স্থান পরিবর্তন, যা সর্বদা উচ্চ তাপমাত্রা বিশিষ্ট স্থান হতে নিম্ন তাপমাত্রা বিশিষ্ট স্থানে প্রবাহিত হয়।- তাপ তিন পদ্ধতিতে এক স্থান থেকে অন্য স্থানে সঞ্চালিত হতে পারে। যথা: পরিবহন, পরিচলন এবং বিকিরণ।
পরিবহন (Conduction)
যে পদ্ধতিতে পদার্থের অণুগুলো তাদের নিজস্ব স্থান পরিবর্তন না করে শুধু স্পন্দনের মাধ্যমে এক অণু পার্শ্ববর্তী অণুকে তাপ প্রদান করে পদার্থের উষ্ণতর অংশ হতে শীতলতর অংশে তাপ সঞ্চালিত করে সেই পদ্ধতিকে পরিবহন পদ্ধতি বলে।
তাপের পরিবহনের উল্লেখযোগ্য বৈশিষ্ট্য হলো-
১. জড় মাধ্যমের প্রয়োজন হয়, তাই শূন্যস্থানের তাপের কোনো পরিবহন হয় না। এ পদ্ধতিতে মাধ্যম উত্তপ্ত হয় কিন্তু মাধ্যমের কণাগুলোর স্থানচ্যুতি ঘটে না।
২. পরিবহন তাপ সঞ্চালনের ধীরতম পদ্ধতি।
৩. সাধারণত কঠিন পদার্থে এ পদ্ধতিতে তাপ সঞ্চালিত হয়। কঠিন পদার্থের মধ্যে দিয়ে তাপের পরিবহন সবচেয়ে বেশি হয়, তরলে তার চেয়ে কম, বায়বীয় পদার্থে অত্যন্ত কম। তাপ পরিবাহকত্বের মান পরিবাহকের উপাদান উপর নির্ভর করে। তামা সর্বোত্তম তাপ পরিবাহক। সাধারণত তাপ সুপরিবাহী পদার্থ বিদ্যুৎ সুরিবাহী হয়। মিকা এর ব্যতিক্রম। মিকা উত্তম তাপ পরিবাহক হলেও বিদ্যুৎ কুপরিবাহী।
পরিচলন (Convection)
যে পদ্ধতিতে তাপ কোন পদার্থের অনুগুলোর চলাচল দ্বারা উষ্ণতর অংশ থেকে শীতলতর অংশে সঞ্চালিত হয় তাকে পরিচলন পদ্ধতি বলে।
তাপের পরিচলনের উল্লেখযোগ্য বৈশিষ্ট্য হলো-
১. জড় মাধ্যমের প্রয়োজন হয়। মাধ্যম উত্তপ্ত হয় এবং মাধ্যমের কণাগুলোর স্থানচ্যুতি ঘটে।
২. এটি পরিবহনের চেয়ে অপেক্ষাকৃত দ্রুত পদ্ধতি।
৩. তরল ও বায়বীয় পদার্থে তাপ সঞ্চালিত হয়।
বিকিরণ (Radiation)
যে পদ্ধতিতে তাপ জড় মাধ্যমের সাহায্য ছাড়াই তাড়িত চৌম্বক তরঙ্গের আকারে উষ্ণ বস্তু থেকে শীতল বস্তুতে সঞ্চালিত হয়, তাকে বিকিরণ পদ্ধতি বলে।
তাপের বিকিরণের উল্লেখযোগ্য বৈশিষ্ট্য হলো-
১. জড় মাধ্যমের প্রয়োজন হয় না।
২. তাপ সঞ্চালনের দ্রুততম প্রক্রিয়া বিকিরণ। তাপ তাড়িত চৌম্বক তরঙ্গ আকারে সরলরেখায় আলোর বেগে সঞ্চালিত হয়।

৩. বায়বীয় ও শূন্য মাধ্যমে তাপ সঞ্চালিত হয়। শূন্যস্থান (Vaccum) এ তাপ বিকিরণ পদ্ধতিতে সঞ্চারিত হয়।
তাপের সঞ্চালনের উদাহরণ-
১. তাপের পরিবহনের জন্য চুলার উপর রাখলে অ্যালুমিনিয়ামের তৈরি কেটলির হাতল গরম হয়।
২. রান্না করার হাড়ি-পাতিল সাধারণত অ্যালুমিনিয়ামের তৈরি হয়। এর প্রধান কারণ এতে দ্রুত তাপ সঞ্চারিত হয়ে খাদ্যদ্রব্য তাড়াতাড়ি সিদ্ধ হয়।
৩. শীতকালে সুতোর কাপড়ের চেয়ে পশমের কাপড় পরলে বেশি গরম অনুভূত হয়। কারণ পশম তাপের কুপরিবাহী। পশমের মধ্যে অনেক আঁশ আলগাভাবে থাকে। তাই পশমের ফাঁকে ফাঁকে অনেক বেশি পরিমাণ বাতাস আটকে থাকতে পারে। আবার বাতাসও তাপের কুপরিবাহী। তাই পশমের পোশাক পরলে পশম এবং এর মধ্যে আটকে থাকা বায়ু আমাদের শরীরের তাপ বেরিয়ে যেতে বাধা দেয়। এ জন্য শরীর গরম থাকে। সুতোর কাপড়ের আঁশগুলো আলগাভাবে থাকে না। তাই সুতোর ফাঁকে বায়ুস্তর, আটকে থাকতে পারে না। ফলে শরীরের তাপ সহজেই বেরিয়ে যেতে পারে। এ জন্য শীতকালে সুতোর কাপড় পরলে ঠাণ্ডা অনুভূত হয়।
৪. শীতে শরীর কাঁপে কারণ শরীরের তাপের চেয়ে বাহিরের তাপ কম।
৫. সূর্য থেকে বিকিরণ পদ্ধতিতে পৃথিবীতে তাপ আসে।
৬. আগুনের পাশের কোনো স্থান থেকে একই দূরত্বে ঠিক উপরে বেশি গরম লাগে কারণ আগুনের পাশের কোনো স্থানে তাপ শুধু বিকিরণ পদ্ধতিতেই সঞ্চালিত হয়। কিন্তু একই দুরত্বে উপরের কোনো স্থানে তাপ বিকিরণ পদ্ধতি ছাড়াও পরিচলন পদ্ধতিতেও সঞ্চালিত হয়। কাজেই একই দূরত্বে পাশের কোন স্থান থেকে উপরের কোনো স্থানে দুই পদ্ধতিতে তাপ সঞ্চালিত হওয়ায় বেশি তাপ সঞ্চালিত হয়। ফলে পাশের কোন স্থান থেকে একই দূরত্বে ঠিক উপরে বেশি গরম লাগে।
৭. একটি জ্বলন্ত বৈদুতিক বাতি গরম থাকে, কারণ ভিতরের ফিলামেন্ট থেকে বিকিরণ পদ্ধতিতে বাতির গায়ে তাপ যায়।
৮. মেঘলারাত্রি অপেক্ষা মেঘহীন রাত্রি শিশির জমার জন্য অধিক অনুকূল। কারণ দিবাভাগে ভূ-পৃষ্ঠ তাপ শোষণ করে এবং রাত্রিকালে ভূ-পৃষ্ঠ তাপ বিকিরণ করে শীতল হয়। মেঘ তাপরোধী পদার্থ। তাই মেঘলারাত্রিতে ভূপৃষ্ঠ থেকে বিকীর্ণ তাপ মেঘের মধ্যে দিয়ে উর্ধ্বাকাশে যেতে পারে না উপরন্তু মেঘ দ্বারা প্রতিফলিত হয়ে ভূ-পৃষ্ঠে ফিরে আসে। ফলে ভূ-পৃষ্ঠ ঠাণ্ডা থাকে না এবং শিশির জমে না।
পক্ষান্তরে মেঘহীন রাত্রিতে ভূপৃষ্ঠ থেকে বিকীর্ণ তাপ উর্ধ্বাকাশে চলে যায়। ফলে ভূ-পৃষ্ঠ শীতল হয় এবং শিশির জমার জন্য অধিক অনুকূল পরিবেশ তৈরি হয়।
৯. টিন বেশি মাত্রায় তাপ বিকিরণ করে বলে টিনের ঘরে বেশি গরম লাগে।
# বহুনির্বাচনী প্রশ্ন
তাপের শোষণ এবং বিকিরণ ( Heat absorption and radiation)
কালো রঙের বস্তুর তাপ বিকিরণ এবং শোষণ ক্ষমতা সবচেয়ে বেশি। এজন্য গ্রীষ্মকালে কালো কাপড় পরিধান করা কষ্টদায়ক। কালো রঙ অধিক তাপ শোষণ করে বলে ছাতার কাপড়ের রঙ সাধারণত কালো হয়্ তাপ বিকিরণ ক্ষমতা অধিক বলে কালো রঙের কাপে চা তাড়াতাড়ি ঠান্ডা হয়। সাদা রঙের বস্তু রতাপ বিকিরণ এবং শোষণ ক্ষমতা সবচেয়ে কম। এজন্য গ্রীষ্মকালে সাদা কাপড় পরিধান করা আরামদায়ক। তাপের বিকিরণ থেকে বাঁচার জন্য শহরের রাষ্তায় ট্রাফিক পুলিশ সাধারণ সাদা ছাতা ও জামা ব্যবহার করে। তাপ বিকিরণ ক্ষমতা কম বলে সাদা রঙের কাপে চা বেশিক্ষণ গরম থাকে।
# বহুনির্বাচনী প্রশ্ন
আপেক্ষিক তাপ (Specific Heat)
কোনো বস্তুর 1 কেজি (Kg) ভরের তাপমাত্রা 1 কেলভিন (K) বাড়াতে যে তাপের প্রয়োজন হয়, তাকে ঐ বস্তুর উপাদানের আপেক্ষিক তাপ বলে। আপেক্ষিক তাপের একক জুল/ কেজি-কেলভিন (JKg-1K-1)। যেমন: পানির আপেক্ষিক তাপ 4200 JKg-1K-1, দুধের আপেক্ষিক তাপ 3930 JKg-1K-1। অন্যান্য পদার্থের তুলনায় পানির আপেক্ষিক তাপ অনেক বেশি। অনেক তাপ শোষণ করলেও পানির উষ্ণতা অল্প বৃদ্ধি পায়। পানির উচ্চ আপেক্ষিক তাপের জন্যই মোটরগাড়ির ইঞ্জিনকে ঠাণ্ডা রাখার জন্য পানি ব্যবহৃত হয়।
তাপধারণ ক্ষমতা (Heat Capacity)
কোন বস্তুর তাপমাত্রা 1K বাড়াতে যে তাপের প্রয়োজন হয় তাকে ঐ বস্তুর তাপধারণ ক্ষমতা বলে। তাপধারণ ক্ষমতার একক জুল/ কেলভিন। (Jk-1)।
তাপধারণ ক্ষমতা = ভর আপেক্ষিত তাপ।
# বহুনির্বাচনী প্রশ্ন
তাপ ইঞ্জিন ( Heat Engine)
যে যন্ত্র তাপ শক্তিকে যান্ত্রিক শক্তিতে রূপান্তরিত করে তাকে তাপ ইঞ্জিন বলে। যেমন: বাষ্পীয় ইঞ্জিন, পেট্রোল ইঞ্জিন, ডিজেল ইঞ্জিন ইত্যাদি ।
এক নজরে তাপীয় ইঞ্জিনসমূহ
তাপ ইঞ্জিন | আবিষ্কারক | দেশ | সময়কাল |
| বাষ্পীয় ইঞ্জিন | জেমসওয়াট | স্কটল্যান্ড | ১৭৮১ |
| রেলওয়ে ইঞ্জিন | ষ্টিফেনসন | যুক্তরাজ্য | ১৮২৫ |
| পেট্রোল ইঞ্জিন | ড. অটো | জার্মানি | ১৮৭৬ |
| ডিজেল ইঞ্জিন | রুডলফ ডিজেল | জার্মানি | ১৮৯২ |
# বহুনির্বাচনী প্রশ্ন
স্টেপ -আপ ট্রান্সফরমারের সাহায্যে
স্টেপ -ডাউন ট্রান্সফরমারের সাহায্যে
অ্যাডাপটারের সাহায্যে
ট্রান্সমিটারের সাহায্যে
পেট্রোল ইঞ্জিন (Petrol Engine)

পেট্রোল ইঞ্জিনে কার্বুরেটর থাকে। কারবুরেটরে পেট্রোলকে বাষ্পে রূপান্তরিত করা হয়। এই পেট্রোল বাষ্পকে যথাযথ অনুপাতে বায়ুর সাথে মিশিয়ে বিস্ফোরক গ্যাসে পরিণত করা হয়। এই মিশ্রণ ইঞ্জিনের জ্বালানি হিসেবে কাজ করে। পেট্রোল ইঞ্জিন একটি চতুর্ঘাত ইঞ্জিন। এ ইঞ্জিনে পিস্টনের দু'বার সামনে এবং দু'বার পিছনে এই চারবার গতির সময়ে মাত্র একবার জ্বালানি সরবরাহ করা হয় বলে এই ইঞ্জিনটিকে চতুর্ঘাত ইঞ্জিন বলে। ১৮৮৬ সালে ড. অটো সর্বপ্রথম সফলতার সাথে এই ইঞ্জিন চালু করেন বলে চক্রের পরপর চারটি ঘাতের ক্রিয়াকে অটোচক্র বলে। পেট্রোল ইঞ্জিনের দক্ষতা প্রায় ৩০%। মোটরগাড়ি, লঞ্চ, এরোপ্লেনে এ ধরনের ইঞ্জিন ব্যবহার করা হয়। সি.এন.জি চালিত গাড়িগুলোও অটো চক্রে চলে।
# বহুনির্বাচনী প্রশ্ন
রেফ্রিজারেটর বা হিমায়ক (Refrigerator)
রেফ্রিজারেটরে শীতলীকরণ প্রকোষ্ঠকে ঘিরে থাকে বাষ্পীভবন কুণ্ডলী। এই কুণ্ডলীতে থাকে উদ্বায়ী পদার্থ ফ্রেয়ন (বা অ্যামোনিয়া)। বাষ্পীভবন কুণ্ডলীতে নিম্নচাপে ফ্রেয়ন বাষ্পীভূত হয়। বাষ্পীভবনের জন্য প্রয়োজনীয় সুপ্ততাপ ফ্রেয়ন শীতলীকরণ প্রকোষ্ঠ থেকে সংগ্রহ করে, ফলে শীতলীকরণ ঘটে। বাষ্পীভূত ফ্রেয়নকে ঘনীভবন কুণ্ডলীর (Condenser) মধ্যে এনে কমপ্রেসরের সাহায্যে ফ্রেয়নকে ঘনীভূত করে। এ সময় ফ্রেয়ন গ্যাস সুপ্ততাপ বর্জন করে পুনরায় তরলে পরিণত করা হয়। ঘনীভবন কুণ্ডলীর সাথে সংযুক্ত তামার জালিতে এ তাপ পরিবহন প্রক্রিয়ায় সঞ্চালিত হয় এবং সেখান থেকে পরিচলন এবং বিকিরণ প্রক্রিয়ায় তাপ পরিবেশে ছড়িয়ে পড়ে। শীতলীকরণ ফ্রেয়নকে পুনরায় বাষ্পীভবন কুণ্ডলীর মধ্য দিয়ে চালনা করে সমস্ত প্রক্রিয়া পুনরাবৃত্তি করা হয়। একটি বদ্ধ ঘরে একটি চালু ফ্রিজের দরজা খুলে রাখলে ঘরের তাপমাত্রা অপরিবর্তিত থাকবে কারণ ঘরটি বদ্ধ বলে ফ্রেয়ন সুপ্ততাপ ঘর থেকে গ্রহণ করবে আবার ঘরেই সুপ্ততাপ বর্জন করবে।
শীতাতপ নিয়ন্ত্রণ ব্যবস্থা (Air Conditioning)
শীতাতপ নিয়ন্ত্রণ ব্যবস্থা হচ্ছে অভ্যন্তরীণ বাতাসে (indoor air) আর্দ্রতার পরিমাণ নিয়ন্ত্রণ করে আরামদায়ক পরিবেশ তৈরি। বিশদ অর্থে শীতলীকরণ, তাপমাত্রা বৃদ্ধি, বাতাসের গতি নিয়ন্ত্রণ ও বিশুদ্ধতা নিশ্চিতকরণই হলো শীতাতপ নিয়ন্ত্রণ ব্যবস্থা।
থার্মোফ্লাষ্ক (Thermo Flask)
থার্মোফ্লাস্ক দুই দেয়াল বিশিষ্ট কাচের পাত্র। এর দেয়াল কাচের তৈরি এবং মুখ কর্ক দিয়ে বন্ধ করা থাকে। তাই তাপ পরিবহন হয় খুব কম। দুই দেয়ালের মধ্যবর্তী স্থান বায়ুশূন্য বলে তাপ পরিবহন বা পরিচলন পদ্ধতিতে ভেতর থেকে বাহিরে বা বাহির থেকে ভিতরে যেতে পারে না। দুই দেয়ালই রূপার প্রলেপ দিয়ে চকচক করা থাকে বলে বিকিরণ পদ্ধতিতেও ভিতরের তাপ বাহিরে বা বাহিরের তাপ ভিতরে যেতে পারে না।

আলো (Light)
আলো এক প্রকার শক্তি (energy) বা বাহ্যিক কারণ (external cause) যা চোখে প্রবেশ করে দর্শনের অনুভূতি জন্মায়।
আলোকবর্ষ (Light-year)
আলো শূন্যস্থানে এক বৎসর সময়ে যে দূরত্ব অতিক্রম করে, তাকে আলোক বর্ষ বলে।
এক আলোকবর্ষ = ৯.৪৬১ ১০১২ কিমি
= ৫.৮৭৯ ১০১২ মাইল
শূন্য মাধ্যমে আলোর গতি |
৩ ১০৬ (৩ লক্ষ) কিলোমিটার/সে. |
৩ ১০৮ মিটার/ সে. |
৩ ১০১০ সেমি./সে. |
১,৮৬,০০০ মাইল/ সে. |
# বহুনির্বাচনী প্রশ্ন
আলোর প্রকৃতি (Nature of Light)
আলো কণা না তরঙ্গ সে বিষয়ে বিজ্ঞানীদের বিতর্কের অবসান এখনও হয় নি। এখন মনে করা হয় অবস্থা বিশেষ আলোক কণা অথবা তরঙ্গরূপে আচরণ করে। তবে কখনই একসঙ্গে কণা বা তরঙ্গ নয়। দীপ্তিমান বস্তু থেকে আলো কিভাবে আমাদের চোখে আসে তা ব্যাখ্যার জন্য বিজ্ঞানীরা এ পর্যন্ত চারটি তত্ত্ব প্রদান করেছেন। যথা-
তত্ত্ব | প্রবক্তা |
| কণাতত্ত্ব | স্যার আইজ্যাক নিউটন |
| তাড়িত চৌম্বক তত্ত্ব | ম্যাক্সওয়েল |
| তরঙ্গ তত্ত্ব | হাইগেন |
| কোয়ান্টাম তত্ত্ব | ম্যাক্স প্ল্যাঙ্ক |
# বহুনির্বাচনী প্রশ্ন
আলোর কোয়ান্টাম তত্ত্ব (Quantum theory of light)
আলোকশক্তি কোন উৎস থেকে অবিচ্ছিন্ন তরঙ্গের আকারে না বেরিয়ে অসংখ্য ক্ষুদ্র ক্ষুদ্র গুচ্ছ বা প্যাকেট আকারে বের হয়। প্রত্যেক রং এর আলোর জন্য এই শক্তি প্যাকেটের শক্তির একটা সর্বনিম্ন মান আছে। এই সর্ব নিম্নমানের শক্তি সম্পন্ন কণিকাকে কোয়ান্টাম বা ফোটন বলে।
Plank's Constant - এর মান ৬.৬৫ ১০-২৭ erg sec |
কোন কোন ধাতুর উপর আলো পড়লে তাৎক্ষণিক ইলেকট্রন নির্গত হয়, একে ফটো তড়িৎ ক্রিয়া বলে। ১৯০৫ সালে বিজ্ঞানী আইনস্টাইন কোয়ান্টাম তত্বের সাহায্যে ফটো তড়িৎ ক্রিয়া ব্যাখ্যা করেন, এর জন্য ১৯২১ সালে তিনি নোবেল পুরস্কারে ভূষিত হন।
তাড়িত চৌম্বক বর্ণালী (Electromagnetic Spectrum)
কোনো পদার্থের পরমাণুর মধ্যে ইলেকট্রনগুলো নির্দিষ্ট দূরত্বে বিভিন্ন খোলকে অবস্থান করে। পরমাণুতে কোনো শক্তি সরবরাহ করা হলে ইলেকট্রন এক খোলক থেকে লাফিয়ে অন্য খোলকে চলে যায়। পরে যখন ইলেকট্রনগুলো নিজ খোলকে ফিরে আসে তখন ইলেকট্রনের মধ্যে সঞ্চিত শক্তি বিকিরণ হয়। এই বিকিরিত শক্তিই আলো। শক্তি বিকিরণ তরঙ্গ আকারে ঘটে যা তাড়িতচৌম্বক তরঙ্গ। গামা রশ্মি, এক্সরে, দৃশ্যমান আলো, অবলোহিত রশ্মি এবং বেতার তরঙ্গ সবই তাড়িত চৌম্বক তরঙ্গ। সব তাড়িতচৌম্বক তরঙ্গের বেগ শূন্য মাধ্যমে একই এবং তা সেকেন্ডে প্রায় ৩ লক্ষ কিলোমিটার। সব তাড়িতচৌম্বক তরঙ্গের বেগ সমান হলেও এদের তরঙ্গ দৈর্ঘ্য বা কম্পাঙ্ক বিভিন্ন। আলোর তরঙ্গ দৈর্ঘ্য অ্যাংস্ট্রম এককে পরিমাপ করা হয়।
বিভিন্ন তাড়িতচৌম্বক তরঙ্গের তুলনামূলক চিত্র (তরঙ্গ দৈর্ঘ্যের উর্ধ্বক্রম অনুসারে)
তাড়িতচৌম্বক তরঙ্গ Name Of Ray | তরঙ্গ দৈর্ঘ্য | মন্তব্য |
গামা রশ্মি Gamma-ray | <10-11m ক্ষুদ্রতম তরঙ্গ দৈর্ঘ্যের বিকিরণ | পারমাণবিক বিস্ফোরণের তেজস্ক্রিয় গামা রশ্মি উৎপন্ন হয়। এ রশ্মি জীব বিশেষ করে মানুষের জন্য সবচেয়ে ক্ষতিকর। |
এক্সরে Х-гау | 10-11m থেকে 10-8m | ভাঙ্গা হাড়ের অবস্থান নির্ণয়ে ব্যবহৃত হয়। রঙিন টেলিভিশন থেকে ক্ষতিকর এক্সরে বের হয়। |
অতিবেগুণী রশ্মি Ultra violet-ray | 10-9m থেকে 3.510-7m | এই রশ্মি ত্বকে ভিটামিন-ডি তৈরিতে সাহায্য করে। |
দৃশ্যমান আলো Visible light | 410-7m থেকে 710-7m (400 - 700 ন্যানোমিটার) | তড়িৎ চুম্বকীয় বর্ণালির সেই অংশ যা মানুষের চোখে দৃশ্যমান অর্থ্যাৎ তরঙ্গ দৈর্ঘ্য সীমার তড়িৎ চুম্বকীয় বিকিরণকে দৃশ্যমান আলো বলে। |
অবলোহিত রশ্মি Infrared-ray | 10-6 m থেকে 10-3m | যে সকল তাড়িৎ চৌম্বক বিকিরণের তরঙ্গ দৈর্ঘ্যের সীমা ১ মাইক্রোমিটার থেকে ১ মিলিমিটার পর্যন্ত বিস্তৃত তাদের অবলোহিত রশি বলা হয়। সূর্য থেকে যে বিকীণ তাপ আসে তা অবলোহিত রশ্মি। উইলিয়াম হার্শেল ১৮০০ সালে এই বিকিরণ আবিষ্কার করেন। সাধারণত রিমোট কন্ট্রোল সমূহে অবলোহিত বা ইনফ্রারেড রে (Ray) ব্যবহৃত হয়। |
মাইক্রোওয়েভ Microwave | 10-3m থেকে 1m | RADAR (= Radio Detection And Ranging), টেলিভিশন ও মোবাইল ফোন প্রযুক্তিতে মাইক্রোওয়েভ তরঙ্গ ব্যবহৃত হয়। বাংলাদেশে টিভি সম্প্রচারের ক্ষেত্রে অডিও সিগনাল ফ্রিকুয়েন্সী মডুলেশন করে পাঠানো হয়। |
বেতার তরঙ্গ Radio wave | 1m হতে 104m. সর্বাপেক্ষা বড় তরঙ্গ দৈর্ঘ্যের বিকিরণ | বেতার তরঙ্গ বায়ুমণ্ডলের আয়নোস্ফিয়ারে প্রতিফলিত হয়। |
কম্পাঙ্ক এবং তরঙ্গ দৈর্ঘ্য: যে চৌম্বক তরঙ্গের তরঙ্গদৈর্ঘ্য যত কম তার কম্পাঙ্ক তত বেশি। গামা রশ্মির কম্পাঙ্ক সবচেয়ে বেশি এবং বেতার তরঙ্গের কম্পাঙ্ক সবচেয়ে কম।
# বহুনির্বাচনী প্রশ্ন
বেগুনী ও হলুদ
লাল ও নীল
বেগুনী ও লাল
নীল ও সবুজ
দৃশ্যমান আলো (Visible light)
তড়িৎ চুম্বকীয় বর্ণালির সেই অংশ যা মানুষের চোখে দৃশ্যমান অর্থ্যাৎ তরঙ্গ দৈর্ঘ্য সীমার তড়িৎ চুম্বকীয় বিকিরণকে দৃশ্যমান আলো বলে। আলোকের বর্ণ নির্ধারণ করে তার তরঙ্গ দৈর্ঘ্য। দৃশ্যমান আলোর তরঙ্গ দৈর্ঘ্যের উর্দ্ধক্রম-
Violet (বেগুনী) < Indigo (আসমানী) < Blue (নীল) < Green (সবুজ) < Yellow (হলুদ) < Orange (কমলা) < Red (লাল)
দৃশ্যমান বর্ণালীর মধ্যে -
আলোর বর্ণ | তরঙ্গ দৈর্ঘ্য | প্রতিসরণ | বিচ্যুতি | বিক্ষেপণ |
| লাল | সবচেয়ে বেশি | সবচেয়ে কম | ||
| বেগুনী | সবচেয়ে কম | সবচেয়ে বেশি | ||
লাল আলোর তরঙ্গ দৈর্ঘ্য বেশি বলে এটি বেশি দূর থেকে দেখা যায়। বিপদ সংকেতের জন্যে তাই লাল আলো ব্যবহার করা হয়। লাল আলোর তরঙ্গদৈর্ঘ্য অধিক বলে সূর্যোদয় বা সূর্যাস্তের সময় আমরা সূর্যকে লাল দেখি।
# বহুনির্বাচনী প্রশ্ন
আলোর প্রতিফলন (Reflection of light)
আলো যখন বায়ু বা অন্য স্বচ্ছ মাধ্যমের ভিতর দিয়ে যাওয়ার সময় অন্য কোন মাধ্যমে বাধা পায় তখন দুই মাধ্যমের বিভেদতল থেকে কিছু পরিমাণ আলো প্রথম মাধ্যমে আসে। একে আলোর প্রতিফলন বলে।

# বহুনির্বাচনী প্রশ্ন
দর্পণ (Mirror)
যে মসৃণ তলে আলোর নিয়মিত প্রতিফলন ঘটে তাকে দর্পণ বলে। সাধারণত কাচের একদিকে ধাতুর (সাধারণত রূপা অথবা মার্কারির) প্রলেপ দিয়ে দর্পণ তৈরি করা হয়। কাচের উপর ধাতুর প্রলেপ দেওয়াকে পারা লাগান বা সিলভারিং বলে।
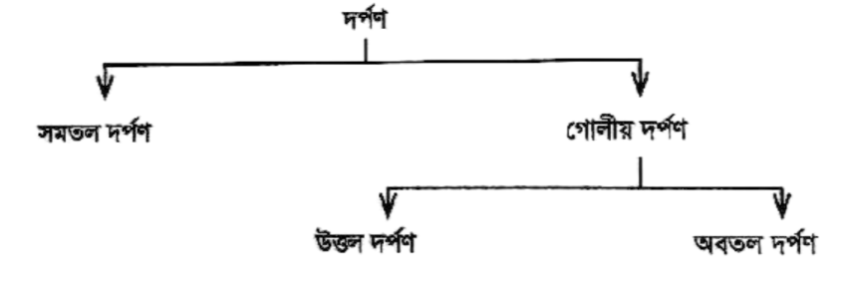
সমতল দর্পণ (Plane Mirror)
একটি সমতল দর্পন হতে বস্তুর দুরত্ব যত, দর্পণ হতে বিশ্বের দূরত্বও তত হয়। সমতল দর্পণে নিজের পূর্ণ বিম্ব দেখতে হলে দর্পণের দৈর্ঘ্য দর্শকের উচ্চতার কমপক্ষে অর্ধেক হওয়া প্রয়োজন। যেমন: একজন লোকের উচ্চতা ৬ ফুট। লোকটি আয়নায় নিজের পূর্ণ প্রতিবিম্ব দেখতে চাইলে আয়নার দৈর্ঘ্য কমপক্ষে (৬ ২) = ৩ ফুট হতে হবে। সরল পেরিস্কোপ তৈরিতে সমতল দর্পণ ব্যবহৃত হয়।
সরল পেরিস্কোপ (Simple Periscope): প্রতিফলন ও ব্যতিচার নীতির উপর ভিত্তি করে পেরিস্কোপ তৈরি হয়। কোনো দূরের জিনিস সোজাসুজি দেখতে বাধা থাকলে এই যন্ত্র ব্যবহার করা হয়। ভীড় এড়িয়ে খেলা দেখা, শত্রু সৈন্যের গতিবিধি পর্যবেক্ষণে এই যন্ত্র ব্যবহৃত হয়। ডুবোজাহাজ বা সাবমেরিনের নাবিকেরা পেরিস্কোপের সাহায্যে পানির নিচ থেকে উপরের দৃশ্য দেখে।
গোলীয় দর্পণ (Spherical Mirror)
উত্তল দর্পণ (Convex Mirror): পিছনের যানবাহন বা পথচারী দেখার জন্য বিভিন্ন গাড়িতে উত্তল দর্পণ ব্যবহৃত হয়। আলোকরশ্মি চারদিকে ছড়িয়ে দেয় বলে মোটর গাড়ির হেডলাইট এবং রাস্তার লাইটে প্রতিফলক হিসেবে উত্তল দর্পণ ব্যবহৃত হয়।
অবতল দর্পণ (Concave Mirror): বিবর্ধিত বিম্ব তৈরি করা যায় বলে রূপ চর্চা ও দাঁড়ি কাঁটার সময় ব্যবহৃত হয়। ডাক্তাররা চোখ, নাক, কান ও গলা পর্যবেক্ষণ করার সময় এই দর্পণ ব্যবহার করেন। স্টীমারের সার্চ লাইচের প্রতিফলক হিসেবে ব্যবহৃত হয়। নভো দূরবীক্ষণে অবতল দর্পণের ব্যবহার দেখা যায়।
বিম্ব (Image)
কোনো বিন্দু থেকে নিঃসৃত আলোক রশ্মিগুচ্ছ প্রতিফলিত বা প্রতিসরিত হয়ে যদি দ্বিতীয় কোনো বিন্দুতে মিলিত হয় বা দ্বিতীয় কোন বিন্দু থেকে অপসৃত হচ্ছে বলে মনে হয়, তাহলে ঐ দ্বিতীয় বিন্দুকে প্রথম বিন্দুর বিম্ব বলে। বিম্ব দুই রকমের হয়। যথা- সদ বিম্ব এবং অসদ বিম্ব।
বিম্বের পার্শ্ব পরিবর্তন (Lateral Inversion of Image)
সমতল দর্পণের সামনে দাঁড়ালে আমাদের ডান হাতকে বাম হাত এবং বাম হাতকে ডান হাত বলে মনে হয়। মনে হয় যেন সমগ্র দেহের পার্শ্ব পরিবর্তন হয়েছে। একে বিম্বের পার্শ্ব পরিবর্তন বলে। যেমনঃ একটি কাগজে 'F' অক্ষর লিখে একটি সমতল দর্পণের সামনে ধরলে দেখা যাবে প্রতিবিম্ব উল্টে গেছে। তবে প্রতিসম বস্তুর ক্ষেত্রে পার্শ্ব পরিবর্তন বুঝা যায় না। যেমন: ইংরেজি 'O' বা 'T' এর পার্শ্ব পরিবর্তন বুঝা যায় না।
# বহুনির্বাচনী প্রশ্ন
আলোর প্রতিসরণ (Refraction of Light)

আলোকরশ্মি এক স্বচ্ছ মাধ্যম থেকে অন্য স্বচ্ছ মাধ্যমে যাওয়ার সময় মাধ্যমদ্বয়ের বিভেদ তলে তীর্যকভাবে আপতিত আলোকরশ্মির দিক পরিবর্তন করার ঘটনাকে আলোর প্রতিসরণ বলে। আলোর প্রতিসরণ জন্য পানিতে নৌকার বৈঠা বাঁকা দেখা যায়। বায়ুমণ্ডলীয় আলোর প্রতিসরণের জন্য সূর্যোদয়ের খানিকটা পূর্বে ও পরে সূর্যকে দেখা যায়, চাঁদ দিগন্তের কাছে অনেক বড় দেখায় এবং রাতের আকাশে তারাগুলো ঝিকমিক করে বলে মনে হয়।
প্রতিসরণাঙ্ক: আলোকরশ্মি যখন এক স্বচ্ছ মাধ্যম থেকে অন্য স্বচ্ছ মাধ্যমে তীর্যকভাবে প্রবেশ করে তখন নির্দিষ্ট রঙের আলোর জন্য আপতন কোণের সাইন ও প্রতিসরণ কোণের সাইন-এর অনুপাত যে ধ্রুব হয় তাকে প্রথম মাধ্যমের সাপেক্ষে দ্বিতীয় মাধ্যমের প্রতিসরণাঙ্ক বলে।
ক্রান্তি কোণ: আলোকরশ্মি ঘন মাধ্যম থেকে হালকা মাধ্যমে প্রতিসরিত হওয়ার সময় আপতন কোণের যে মানের জন্য প্রতিসরণ কোণের মান ৯০° হয়, অর্থাৎ প্রতিসরিত রশ্মি বিভেদ তল ঘেষে চলে যায় তাকে হালকা মাধ্যমের সাপেক্ষে ঘন মাধ্যমর ক্রান্তি কোণ বলে।
# বহুনির্বাচনী প্রশ্ন
পূর্ণ অভ্যন্তরীণ প্রতিফলন (Total Internal Reflection)
আলোকরশ্মি যখন ঘন মাধ্যম থেকে হালকা মাধ্যমে ক্রান্তি কোণের চেয়ে বড় মানের কোণে আপতিত হয় তখন প্রতিসরণের পরিবর্তে আলোকরশ্মি সম্পূর্ণরূপে ঘন মাধ্যমের অভ্যন্তরে প্রতিফলনের সূত্রানুযায়ী প্রতিফলিত হয়। এই ঘটনাকে আলোর পূর্ণ অভ্যন্তরীণ প্রতিফলন বলে। আলোর এই ধর্মকে কাজে লাগিয়ে ফাইবার অপটিক ক্যাবল তৈরি করা হয়েছে।
আলোর পূর্ণ অভ্যন্তরীণ প্রতিফলনের জন্য -
- হীরক উজ্জ্বল দেখায়।
- পদ্ম পাতার উপর বৃষ্টির ফোঁটা পড়লে চকচক করে।
- গ্রীষ্মের প্রখর রৌদ্রে উত্তপ্ত পিচঢালা মসৃন রাজপথকে বৃষ্টির অব্যবহিত পরবর্তী সময়ের মত ভেজা ও চকচকে মনে হয়।
- মরুভূমির মরীচিকার (Mirage) সৃষ্টি হয়।
# বহুনির্বাচনী প্রশ্ন
লেন্স (Lens)
দুই গোলীয় পৃষ্ঠ দ্বারা সীমাবদ্ধ কোন স্বচ্ছ প্রতিসারক মাধ্যমকে লেন্স বলে। লেন্স প্রধানত দুই প্রকার। যথা- উত্তল লেন্স এবং অবতল লেন্স। লেন্সের ক্ষমতার প্রচলিত একক ডাইঅপ্টার। উত্তল লেন্সের ক্ষমতা ধনাত্মক এবং অবতল লেন্সের ক্ষমতা ঋনাত্মক।
উত্তল লেন্সের ব্যবহার:
- আতশী কাচ হিসাবে এবং আগুন জ্বালানোর কাজে ব্যবহৃত হয়।
- চশমা, ক্যামেরা, বিবর্ধক কাচ, অণুবীক্ষণ যন্ত্র ইত্যাদি আলোক যন্ত্রে ব্যবহৃত হয়।
অবতল লেন্সের ব্যবহার:
- প্রধানত চশমায় ব্যবহার করা হয়।
- গ্যালিলিওর দূরবীক্ষণ যন্ত্র এবং সিনেমাস্কোপ প্রজেক্টারে অবতল লেন্স ব্যবহার করা হয়।
# বহুনির্বাচনী প্রশ্ন
৩০°
৬০°
৯০°
১২০° পর্যন্ত
প্রিজম (Prism)
দুইটি হেলানো সমতল পৃষ্ঠ দ্বারা সীমাবদ্ধ প্রতিসারক মাধ্যমকে প্রিজম বলা হয়। প্রিজমে পতিত আলো সাধারণত প্রতিসরিত হয়।
# বহুনির্বাচনী প্রশ্ন
৭
৩
৫
অসংখ্য
রঙধনু বা রামধনু (Rainbow)
রঙধনু একটি আলোকীয় ঘটনা। এক পশলা বৃষ্টির পর আবার যখন সূর্য উঠে তখন কখনও কখনও সূর্যের বিপরীত দিকে আকাশে উজ্জ্বল রঙের অর্ধবৃত্ত দেখা যায়। একে বলা হয় রঙধনু। রংধনু সৃষ্টির সময় পানির কণাগুলো প্রিজমের কাজ করে। রংধনুতে বর্নালীর ৭টি রঙ থাকে। সূর্যের বিপরীতে গঠিত হয় বলে সকালে পশ্চিমাকাশে এবং বিকালে পূর্বাকাশে রংধনু দেখা যায়।
আলোর বিচ্ছুরণ (Dispersion of light)
সূর্যের সাদা আলো যদি কোনো কাচের প্রিজমের মধ্যে দিয়ে যায় তাহলে তা সাতটি রঙে বিশ্লিষ্ট হয়। প্রিজম থেকে নির্গত আলোকরশ্মি যদি কোনো পর্দার উপর ফেলা হয়, তাহলে পর্দায় ৭টি রঙের পট্টি দেখা যায়। আলোর এই রঙিন পট্টিকে বর্ণালী (Spectrum) বলে। কোনো মাধ্যমে প্রতিসরণের ফলে যৌগিক আলো থেকে মূল বর্ণের আলো পাওয়ার পদ্ধতিকে আলোর বিচ্ছুরণ বলে। বর্ণালীতে বেগুনি (Violet), আসমানী (Indigo), নীল (Blue), সবুজ (Green), হলুদ (Yellow), কমলা (Orange) ও লাল (Red) এ সাতটি রঙ পরপর দেখা যায়। রঙগুলোর নাম এবং এদের ক্রম মনে রাখার জন্য এদের নামের আদ্যক্ষর নিয়ে ইংরেজিতে VIBGYOR ও বাংলায় বেনীআসহকলা শব্দ গঠন করা হয়। বর্ণালীর লাল আলোর বিচ্যুতি সবচেয়ে কম এবং বেগুনী আলোর বিচ্যুতি সবচেয়ে বেশি। হলুদ রঙের আলোর বিচ্যুতি লাল ও বেগুনি আলোর মাঝামাঝি বলে এর বিচ্যুতিকে গড় বিচ্যুতি এবং হলুদ রশ্মিকে মধ্যরশ্মি বলে। বর্ণালীতে হলুদ রঙের পাশের দুটি রঙ হলো সবুজ ও কমলা। বিজ্ঞানী নিউটন প্রমাণ করেন যে, সাদা আলোর প্রকৃতি যৌগিক এবং এই সাদা আলো সাতটি মূল রঙের আলোর সমষ্টি।
# বহুনির্বাচনী প্রশ্ন
মৌলিক বর্ণ (Primary Colour)
সাতটি মূল বর্ণের সমন্বয়ে বর্ণালী গঠিত হয়। তবে এই সাতটি রঙের মধ্যে তিনটি রঙ আছে যাদেরকে পরিমাণ মতো মিশিয়ে অপর যে কোন রঙ তৈরি করা যেতে পারে। এদেরকে মৌলিক বর্ণ বলে। এই তিনটি রঙ হচ্ছে - লাল (Red), সবুজ (Green), ও নীল (Blue)।
মনে রাখার সহজ উপায়ঃ 'আসল' রঙ - আ ঃ নীল (আসমানী), স ঃ সবুজ, ল ঃ লাল।
মৌলিক বর্ণগুলো মিশিয়ে বিভিন্ন বর্ণ তৈরি করা যায়। যথা-
লাল + নীল = বেগুনি,
লাল + হলুদ = কমলা
নীল + হলুদ = সবুজ
# বহুনির্বাচনী প্রশ্ন
বেগুনী
কালো
হলুদ
লাল
পরিপূরক বর্ণ (Complementary Colour)
একটি লাল কাচকে উত্তপ্ত করলে সবুজ রঙ বের হয়। আর সবুজ কাচকে উত্তপ্ত করলে লাল রঙ বের হয়। একটি নীল কাচকে উত্তপ্ত করলে হলুদ রঙ বের হয়। আর হলুদ কাচকে উত্তপ্ত করলে নীল রঙ বের হয়।
# বহুনির্বাচনী প্রশ্ন
বেগুনী
কালো
হলুদ
লাল
আলোর শোষণ, প্রতিফলন ও বস্তুর বর্ণ
Absorption and reflection of light and colour of a body
কোনো বস্তু তার নিজস্ব রঙে দেখা যায়, কারণ নির্দিষ্ট রঙের বস্তুটি নিজের রঙ ছাড়া সকল রঙ শোষণ করে এবং নিজের রঙ প্রতিফলিত করে। তাই বস্তু তার নিজের রঙে দেখা যায়। সাতটি রঙের সমন্বয়ে সাদা রঙ হয়, সব রঙের অনুপস্থিতির জন্য কালো রঙ হয়। যে বস্তু আলোর সব রঙ প্রতিফলিত করে তা সাদা দেখায়। কোনো বস্তু যখন সমস্ত আলো শোষণ করে তখন তাকে কালো দেখায়। যেমন: আলোর সকল বর্ণ প্রতিফলিত করে বলে বরফ সাদা দেখায়।
দিনের বেলা সূর্যালোকে গাছের পাতা সবুজ দেখায় কিন্তু লাল আলোতে গাছের পাতা কালো বলে মনে হয়। দিনে গাছের সবুজ পাতা সূর্যালোকের সবুজ বাদে সাতটি বর্ণের সবকটিই শোষণ করে ফলে সবুজ দেখায়। কিন্তু সবুজ পাতা লাল আলোকে শোষণ করে নেয় বলে কোনো আলোই প্রতিফলিত হয় না তাই লাল আলোতে সবুজ পাতা কালো দেখায়। একইভাবে, লাল আলোতে নীল রঙের ফুল কালো দেখা যায়; সবুজ আলোতে একটি হলুদ রঙের বস্তু কালো দেখায়; সোডিয়াম লাইটের হলুদ আলোতে রাতে লাল কাপড় কালো দেখায়। নীল কাঁচের মধ্যে দিয়ে সাদা ফুল নীল দেখায় কারণ একটি সাদা ফুল সূর্যের সাতটি আলোই প্রতিফলিত করে বলে তা সাদা দেখায়। সাদা ফুল থেকে প্রতিফলিত আলোক রশ্মি যখন নীল কাঁচের মধ্যে দিয়ে আসে তখন ঐ কাঁচ নীল বাদে অন্য সব বর্ণের আলো শোষণ করে নেয় তাই আমাদের চোখে শুধু নীল আলো পৌছে। ফলে ফুলটি নীল দেখায়। নীল কাঁচের মধ্যে দিয়ে হলুদ ফুল কালো দেখায় কারণ হলুদ ফুল শুধু হলুদ বর্ণের আলো প্রতিফলিত করে বলে তা হলুদ দেখায়। কিন্তু হলুদ বর্ণের আলোক নীল কাঁচের মধ্যে দিয়ে আসার সময় শোষিত হয় তাই হলুদ ফুলকে নীল কাঁচের মধ্যে দিয়ে দেখলে কালো দেখায়।
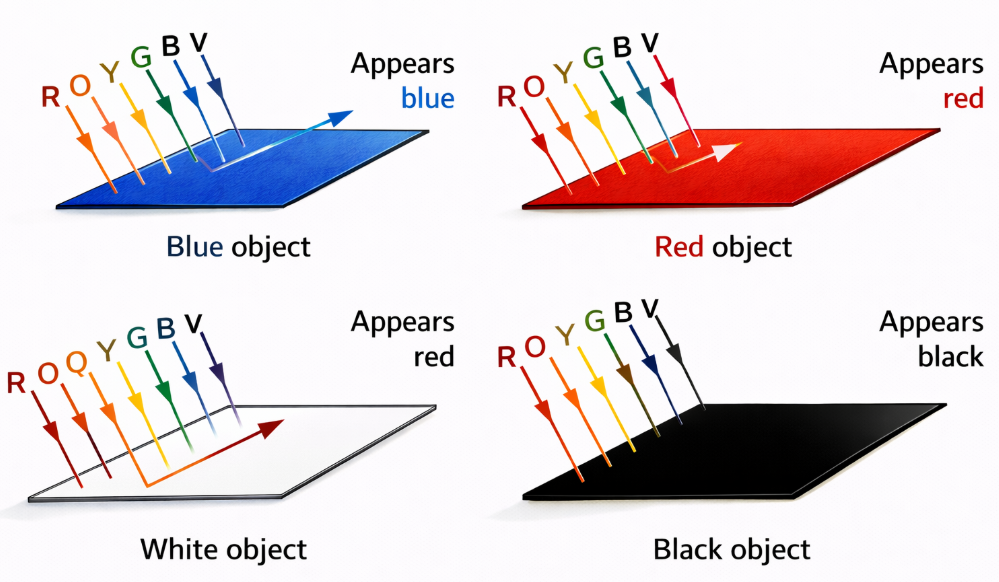
মানুষের চোখ (Human Eye)
মানুষের চোখের গঠন এবং কার্যাবলী অনেকটা ক্যামেরার মতো। মানব চোখের লেন্সটি উভ উত্তল বা দ্বি উত্তল। চোখের আলোকসংবেদী অংশের নাম রেটিনা। কোনো বস্তু হতে আলোক রশ্মি চোখের-লেন্স দ্বারা প্রতিসরিত হয়ে রেটিনায় বিশ্ব গঠন করে। রেটিনায় গঠিত বিশ্বটি হয় সদ, উল্টো ও খর্বিত। রেটিনা আলোক শক্তিকে তড়িৎশক্তিতে পরিণত করে। মানুষের চোখে রেটিনা ও চক্ষুলেন্সের মধ্যবর্তী স্থান ভিট্রিয়াস হিউমার নামক জেলী জাতীয় পদার্থ দ্বারা পূর্ণ থাকে। রেটিনাতে দুই ধরনের আলোক সংবেদী কোষ থাকে। যথা-রডস এবং কোনস। রডস অন্ধকারে এবং কোনস আলোতে দেখতে সহায়তা করে। পেঁচা দিনে দেখতে পায়না কিন্তু রাতে দেখতে পায় কারণ পেঁচার চোখের রেটিনাতে রডস এর সংখ্যা বেশি কিন্তু কোনস এর সংখ্যা কম। রাতের বেলা বিড়াল ও কুকুরের চোখ জ্বলজ্বল করে, কারণ কুকুর ও বিড়ালের চোখে টেপেটাম নামক রঞ্জক কোষ থাকে। যদি কোনো বস্তুকে চোখের সামনে থেকে সরিয়ে নেয়া হয়, তাহলে সরিয়ে নেওয়ার ০.১ সেকেন্ড পর্যন্ত এর অনুভূতি আমাদের মস্তিষ্কে থেকে যায়। এই সময়কে দর্শনানুভূতির স্থায়িত্বকাল বলে। সবুজ-হলুদ আলোতে মানুষের দর্শনানুভূতি সুবচেয়ে বেশি পক্ষান্তরে লাল-বেগুনি আলোতে মানুষের দর্শনানুভূতি সর্বনিম্ন। স্বাভাবিক চোখের দৃষ্টির পাল্লা ২৫ সেমি থেকে অসীম পর্যন্ত। যদি কোনো চোখ এই পাল্লার মধ্যে কোনো বস্তুকে স্পষ্ট দেখতে না পায়, তাহলে সে চোখ ত্রুটিপূর্ণ বলে ধরা হয়। চোখের ত্রুটি প্রধানত দুই প্রকার। যথা-হ্রস্বদৃষ্টি (Myopia) এবং দীর্ঘদৃষ্টি (Hypermetropia)।
| চোখের ত্রুটি | নিকট বস্তু দর্শণ | দূরের বস্তু দর্শণ | চিকিৎসায় প্রয়োজন |
| দীর্ঘদৃষ্টি (Hypermetropia) | X | √ | উত্তল লেন্স |
| হ্রস্বদৃষ্টি (Myopia) | √ | X | অবতল লেন্স |
বিষম দৃষ্টি (Astigmatism): চোখের এই ত্রুটির কারণে একই দূরত্বে অবস্থিত আনুভূমিক ও উলম্ব রেখাকে সমান স্পষ্টভাবে দেখা যায় না। বিষমদৃষ্টি ত্রুটি চিকিৎসায় সিলিন্ড্রিক্যাল লেন্স ব্যবহৃত হয়। বর্তমানে 'টরিক কন্ট্যাক্ট লেন্স' এর ব্যবহারও জনপ্রিয় হয়ে উঠেছে। সাধারণ কন্ট্যাক্ট লেন্সসমূহ Polyvinyl chloride (পলিভিনাইল ক্লোরাইড) দিয়ে তৈরি। কিন্তু টরিক কনট্যাক্ট লেন্স সিলিকন হাইড্রোজেল দিয়ে তৈরি।
চোখের ছানি (Cataract): চোখের লেন্স অস্বচ্ছ হয়ে গেলে চোখের দৃষ্টিশক্তি হ্রাস পায়। একে চোখের ছানি পড়া বলে। চিকিৎসা -অপারেশনের মাধ্যমে অস্বচ্ছ লেন্স অপসারণ করে স্বচ্ছ লেন্স সংযোজন।
# বহুনির্বাচনী প্রশ্ন
ক্যামেরা (Camera)
ক্যামেরা এবং মানুষের চোখের গঠন এবং কার্যপ্রণালীর অনেক মিল আছে। ফটোগ্রাফিক প্লেটে সিলভার হ্যালাইড (AgBr বা Agl) এর আবরণ থাকে।
দৃষ্টি সহায়ক যন্ত্র (Vision Aid Instruments)
যে সকল যন্ত্র কোন বস্তু দেখার ব্যাপারে আমাদের চোখকে সাহায্য করে তাদেরকে দৃষ্টি সহায়ক যন্ত্র বলে। যেমন: অণুবীক্ষণ যন্ত্র বা মাইক্রোস্কোপ, দূরবীক্ষণ যন্ত্র বা টেলিস্কোপ, বাইনোকুলার ইত্যাদি।
যন্ত্র বা অঙ্গ | সৃষ্ট প্রতিবিম্বের ধরন |
| চোখ | সদ, উল্টো ও খর্বিত |
| ক্যামেরা | সদ, উল্টো ও খর্বিত |
| সরল অণুবীক্ষণ যন্ত্র বা অতশী কাঁচ | সোজা, বিবর্ধিত ও অসদ বিম্ব |
| জটিল অণুবীক্ষণ যন্ত্র | উল্টো ও বিবর্ধিত |
বিবিধ
- অধিকাংশ ফটোকপি মেশিন পোলারয়েড পদ্ধতিতে কাজ করে। ফটোস্ট্যাট মেশিনে সেলেনিয়াম ব্যবহৃত হয়।
- আধুনিক মুদ্রণ ব্যবস্থায় ধাতু নির্মিত অক্ষরের প্রয়োজন ফুরাবার বড় কারণ ফটো লিথোগ্রাফি।
তড়িৎ বা বিদ্যুৎ এক প্রকার শক্তি। দৈনন্দিন জীবনের প্রায় প্রতিটি ক্ষেত্রেই বিদ্যুতের প্রয়োগ দেখা যায়। তড়িৎ বা বিদ্যুৎ হল পদার্থের একটি ধর্ম যা কোনো তড়িৎ পরিবাহকের (Conductor) মধ্যে দিয়ে তড়িৎ আধানের বা ইলেকট্রন প্রবাহের (Flow of electrons) ফলস্বরূপ সৃষ্টি হয়। তড়িৎ দুই প্রকার: স্থির তড়িৎ (Statical Electricity) এবং চল তড়িৎ (Current Electricity)। চল তড়িৎ দুই প্রকার- যথা: সমপ্রবাহ (Direct current বা D.C) এবং পর্যাবৃত্ত প্রবাহ (Alternating current বা A.C)। তড়িৎ প্রবাহ যদি সর্বদা একই দিকে প্রবাহিত হয় বা সময়ের সাথে তড়িৎ প্রবাহের দিকের কোনো পরিবর্তন না হয় তাহলে সেই প্রবাহকে সমপ্রবাহ বলে। তড়িৎকোষ (ব্যাটারি) থেকে আমরা সমপ্রবাহ পাই। যে তড়িৎ প্রবাহ নির্দিষ্ট সময় পরপর দিক পরিবর্তন করে অথ্যাৎ যে তড়িৎ প্রবাহের দিক পর্যাবৃত্তভাবে পরিবর্তিত হয় তাকে পর্যাবৃত্ত প্রবাহ বলে। আমাদের দেশে বাসাবাড়িতে যে পর্যাবৃত্ত প্রবাহ ব্যবহার করা হয় তা প্রতি সেকেন্ডে ৫০ (পঞ্চাশ) বার দিক পরিবর্তন করে। তড়িৎ প্রবাহের একক হলো অ্যাম্পিয়ার। যে চালিকা শক্তি বর্তনীতে বিদ্যুৎ প্রবাহ বজায় রাখে, তাকে তড়িচ্চালক শক্তি বলে। তড়িচ্চালক শক্তির একক ভোল্ট। বৈদ্যুতিক চাপের পরিমাণকে 'Voltage' বলে। বাংলাদেশের বাসা-বাড়িতে বিদ্যুতের ভোল্টেজ ২২০ ভোল্ট এ.সি।
# বহুনির্বাচনী প্রশ্ন
তড়িৎ পরিবাহিতা (Electric Conductance)
তড়িৎ পরিবাহী ধর্মের উপর ভিত্তি করে পদার্থসমূহ ৩ প্রকার। যথা:
১) পরিবাহক (Conductor)
২) অন্তরক (Insulator)
৩) অর্ধপরিবাহী (Semiconductor)
পরিবাহক (Conductor)
যেসব বস্তুর ভিতর তড়িৎ আধান সহজে চলাচল করতে পারে, তাদের বলা হয় পরিবাহক। সকল ধাতু, মানবদেহ, আর্দ্র বায়ু, পানি, মাটি প্রভৃতি বিদ্যুৎ পরিবহন করে। গ্রাফাইট অধাতু হলেও তড়িৎ পরিবাহী। রূপা সর্বোত্তম তড়িৎ পরিবাহক। আর্দ্র বায়ু বা মেঘযুক্ত তড়িৎ পরিবাহী বলে এর মধ্যে দিয়ে বিমান চালনা করা ঝুঁকিপূর্ণ।
অন্তরক বা অপরিবাহক (Insulator)
যেসব বস্তুর ভিতর দিয়ে তড়িৎ আধান চলাচল করতে বা পরিবাহিত হতে পারে না তাদের বলা হয় অন্তরক। অধাতু, প্লাস্টিক, কাঠ, কাঁচ, রাবার, চীনামাটি, রেশম, শুষ্ক বাতাস প্রভৃতি অন্তরক পদার্থ।
অর্ধপরিবাহী (Semiconductor)
যেসব পদার্থের তড়িৎ পরিবাহীতা পরিবাহী পদার্থের চেয়ে অনেক কম, কিন্তু অন্তরক পদার্থের চেয়ে অনেক বেশী, তাদের অর্ধপরিবাহী, (Semiconductor) বলে। যেমন: সিলিকন (Silicon), জার্মেনিয়াম (Germenium) ক্যাডমিয়াম সালফাইড, গ্যালিয়াম আর্সেনাইড প্রভৃতি।
বিদ্যুৎ চমকানো এবং বজ্রপাত (Shining Power & Lightning)
বাতাসে রয়েছে পানির কণা, ধূলিকণা এবং বিভিন্ন রকম গ্যাসের কণা। এইসব কণার মধ্যে ঘর্ষণের ফলে উৎপন্ন হয় স্থির বিদ্যুৎ অর্থাৎ কণাগুলো চার্জিত হয়। এরূপ কোটি কোটি চার্জিত পানি কণা মিলে সৃষ্টি হয় মেঘ। এই মেঘ ধনাত্মক বা ঋণাত্মক চার্জে চার্জিত হতে পারে। ধনাত্মক চার্জযুক্ত মেঘ এবং ঋণাত্মক চার্জযুক্ত মেঘের মধ্যে আকর্ষণের ফলে পরস্পরের সাথে প্রবল বেগে ঘর্ষণ হয় এবং এই সাথে তাপ, আলো এবং শব্দের সৃষ্টি হয়। আলোর বেগ শব্দের বেগের চাইতে বহুগুণ বেশি বলে আমরা আলো আগে দেখি এবং শব্দ পরে শুনি। এই আলোর ঝমকানিকে বিদ্যুৎ চমকানো বলে। অনেক সময় তীব্র চার্জযুক্ত মেঘ পৃথিবীর কাছাকাছি চলে আসে। তখন বিদ্যুৎক্ষরণ ঘটে বায়ুমণ্ডলকে ভেদ করে মেঘ এবং মাটির মধ্যে। একে বলা হয় বজ্রপাত। বজ্রপাতের সময় যে শব্দ শোনা যায়, তাকে বলে বজ্রনাদ। মাটির উপর যে জিনিস যত উঁচু সেই জিনিস মেঘের তত কাছাকাছি থাকে। তাই বজ্রপাত সাধারণত হয় উঁচু দালান বা গাছের মাথায়। এমনকি মাঠের মধ্যে দাড়িয়ে থাকা কোনো মানুষের মাথায়ও বজ্রপাত হতে পারে। ঝড়বৃষ্টির সময় তাই গাছের নিচে বা খোলা স্থানে দাড়িয়ে থাকা নিরাপদ নয়। বজ্রপাতের সময় থাকা উচিত গুহার ভিতর বা মাটিতে শুয়ে।
বজ্রপাত থেকে বাঁচার কয়েকটি উপায় হলো:
১. দালান বা পাকা ভবনের নিচে আশ্রয় নেওয়া।
২. উঁচু গাছপালা ও বিদ্যুতের লাইন বা খুঁটি থেকে দূরে থাকা।
৩. বজ্রপাতের সময় গাড়ীর ভিতরে থাকলে সম্ভব হলে গাড়ীটিকে কোনো কংক্রিটের ছাউনির নিচে আশ্রয় নেওয়া। গাড়ীর ধাতব বস্তু স্পর্শ করা থেকে বিরত থাকুন; এমনকি গাড়ীর কাঁচেও হাত দিবেন না।
৪. বজ্রপাতের সময় খোলা ও উঁচু জায়গা হতে সাবধান। ধানক্ষেত বা বড় মাঠে থাকলে তাড়াতাড়ি নিচু হয়ে যাওয়া উচিত।
# বহুনির্বাচনী প্রশ্ন
নিউরন
নেফ্রন
পেসমেকার
হেপাটোসাইট
রোধ (Resistance)
পরিবাহকের যে ধর্মের জন্য এর মধ্য দিয়ে বিদ্যুৎ প্রবাহ বিঘ্নিত হয়, তাকে রোধ (Resistance) বলে। রোধের একক ওহম (Ohm)।
ও'মের সূত্র (Law's of Ohm)
নির্দিষ্ট তাপমাত্রায় কোনো পরিবাহীর মধ্য দিয়ে যে বিদ্যুৎ প্রবাহ চলে, তা ঐ পরিবাহীর দুই প্রান্তের বিভব পার্থক্যের সমানুপাতিক। বিভব পার্থক্য = রোধ বিদ্যুৎ প্রবাহ (V = RI)
রোধের সূত্র (Law's of Resistance)
কোনো পরিবাহকের রোধ চারটি বিষয়ের উপর নির্ভর করে। যথা: পরিবাহকের দৈর্ঘ্য, পরিবাহকের প্রস্থচ্ছেদের ক্ষেত্রফল, পরিবাহকের উপাদান এবং পরিবাহকের তাপমাত্রা। একই উপাদানের তৈরি সুষম প্রস্থচ্ছেদের লম্বা তারের রোধ ছোট তার অপেক্ষা বেশি হয়। একই উপাদান এবং একই দৈর্ঘ্যের মোটা তারের চেয়ে চিকন তারের রোধ বেশি হয়।
১. অধিক দূরত্বে তড়িৎ প্রেরণে ভোল্টেজ বাড়ানো হয় এবং তড়িৎ প্রবাহ কমানো হয়, কারণ এতে তাপ শক্তি উৎপাদন কম হয় বলে বিদ্যুতের অপচয় কম হয়।
২. বৈদ্যুতিক পাখার ঘূর্ণনের গতি রেগুলেটরের মাধ্যমে নিয়ন্ত্রিত হয়। রেগুলেটরে থাকে পরিবর্তনশীল রোধ। রেগুলেটরের রোধ বাড়িয়ে দিলে বিদ্যুৎ প্রবাহ কমে যায়, ফলে পাখা ধীরে ঘোরে। কিন্তু এক্ষেত্রে বিদ্যুৎ সাশ্রয় হয় না কারণ রেগুলেটরে সাশ্রয়কৃত বিদ্যুৎ তাপশক্তি হিসেবে অপচয় হয়।
৩. সাধারণ বৈদ্যুতিক বাতির ফিলামেন্টে রোধের কারণে তাপ সৃষ্টি হয়। ফলে তাপশক্তি হিসেবে কারণে বিদ্যুতের অপচয় হয়।
জেনে রাখা ভালো
১. PN-ডায়াডকে ফরোয়ার্ড বায়াস করলে রোধ কমে।
২. PN-ডায়াডকে রিভার্স বায়াস করলে রোধ বাড়ে।
# বহুনির্বাচনী প্রশ্ন
তড়িৎ পরিবাহিতা (Electric Conductance)
তড়িৎ পরিবাহিতা তড়িৎ মাধ্যমের একটি ধর্ম যা এর মধ্য যে তড়িৎ প্রবাহিত করতে সহায়তা করে। তড়িৎ পরিবাহিতার একক সিমেন্স। তড়িৎ পরিবাহী ধর্মের উপর ভিত্তি করে পদার্থসমূহকে তিন ভাগে ভাগ করা যায়। যথা- পরিবাহী, অর্ধপরিবাহী এবং অন্তরক।
(ক) পরিবাহক (Conductor): যে সব বস্তুর ভিতর তড়িৎ আধান সহজে চলাচল করতে পারে, তাদের বিদ্যুৎ পরিবাহী বলে। সকল ধাতু, মানবদেহ, আর্দ্র বায়ু, পানি, মাটি প্রভৃতি বিদ্যুৎ পরিবর্তন করে। গ্রাফাইট অধাতু হলেও তড়িৎ পরিবাহী। রূপা সর্বোত্তম তড়িৎ পরিবাহক। আর্দ্র বায়ু বা মেঘযুক্ত তড়িৎ পরিবাহী বলে এর মধ্যে দিয়ে বিমান চালনা করা ঝুঁকিপূর্ণ।
(খ) অন্তরক বা অপরিবাহক (Insulator): যেসব বস্তুর ভিতর দিয়ে তড়িৎ আধান চলাচল করতে বা পরিবাহিত হতে পারে না তাদের বলা হয় অন্তরক। যেমন; অধাতু,প্লাস্টিক, কাঠ, কাঁচ, রাবার, চীনামাটি, রেশম, শুষ্ক বাতাস প্রভৃতি অন্তরক পদার্থ।
(গ) অর্ধপরিবাহী (Semiconductor): যেসব পদার্থের তড়িৎ পরিবাহীতা পরিবাহী পদার্থের চেয়ে অনেক কম, কিন্তু অন্তরক পদার্থের চেয়ে অনেক বেশী, তাদের অর্ধপরিবাহী বলে। যেমন : সিলিকন, জার্মেনিয়াম, ক্যাডমিয়াম সালফাইড, গ্যালিয়াম আর্সেনাইড, ইনডিয়াম এবং অ্যানটিমোনাইড। তাপমাত্রা বাড়লে প্রায় সকল পরিবাহকেরই পরিবাহিতা হ্রাস পায়। তবে এর ব্যতিক্রমও দেখা যায়। সিলিকন, জার্মেনিয়াম ইত্যাদি অর্ধপরিবাহী ধাতুর তাপমাত্রা বাড়লে এদের পরিবাহীতা উল্লেখযোগ্য হারে বৃদ্ধি পায়। কার্বন অর্ধপরিবাহী না হলেও তাপমাত্রা বৃদ্ধির সাথে এর পরিবাহিতা বৃদ্ধি পায়।
# বহুনির্বাচনী প্রশ্ন
তড়িৎ ক্ষমতা (Electrical Power)
কোন পরিবাহক বা তড়িৎ যন্ত্রের মধ্যে দিয়ে এক সেকেন্ড ধরে তড়িৎ প্রবাহের ফলে যে কাজ সম্পন্ন হয় বা যে পরিমাণ তড়িৎ শক্তি অন্য শক্তিতে (আলো, তাপ, যান্ত্রিক শক্তি ইত্যাদি) রূপান্তরিত হয়, তাকে তাড়িৎক্ষমতা বা বৈদ্যুতিক ক্ষমতা বলে। বৈদ্যুতিক ক্ষমতাকে P দ্বারা প্রকাশ করা হয়।
P = VI = I2R = V2/R
তড়িৎ ক্ষমতার একক ওয়াট (watt)। ১ ওয়াট = ১ ভোল্ট ১ অ্যাম্পিয়ার। বৈদ্যুতিক বিল কিলোওয়াট-ঘন্টা (Kilowatt-hour) বা B.O.T এককে হিসাব করা হয়।
১ কিলোওয়াট-ঘণ্টা = ৩৬০০ কিলোজুল (kj).
# বহুনির্বাচনী প্রশ্ন
তড়িৎ শক্তি (Electric Energy)
কাজ করার সামর্থ্যকে শক্তি বলে। বিদ্যুৎ শক্তির বাণিজ্যিক একক 'কিলোওয়াট-ঘণ্টা'। এক কিলোওয়াট ক্ষমতাসম্পন্ন কোনো বৈদ্যুতিক যন্ত্র এক ঘণ্টা কাজ করলে যে পরিমাণ বিদ্যুৎ শক্তি খরচ হয়, তাকে এক কিলোওয়াট-ঘণ্টা বলে। সারা বিশ্বের বিদ্যুৎ ব্যবহারকারী সংস্থাগুলো এই একক ব্যবহার করে বিদ্যুৎ বিল প্রণয়ন করে। এ একককে বোর্ড অব ট্রেড ইউনিট বা সংক্ষেপে শুধু ইউনিটও বলে। অর্থাৎ এক কিলোওয়াট ঘণ্টাকে এক ইউনিট ধরা হয়।
১ ইউনিট = ১ কিলোওয়াট-ঘণ্টা = ৩৬০০ কিলোজুল = ১০০০ ওয়াট-ঘণ্টা = ৩.৬ ১০৬ জুল।
# বহুনির্বাচনী প্রশ্ন
ফিউজ (Fuse)
বৈদ্যুতিক যন্ত্রপাতিতে একটি নির্দিষ্ট মাত্রার চেয়ে বেশি বিদ্যুৎ প্রবাহিত হলে তা নষ্ট হয়ে যায়। এ ধরনের বৈদ্যুতিক দুর্ঘটনা এড়াবার জন্য ফিউজ তার ব্যবহার করা হয়। ফিউজ হচ্ছে নিম্ন গলনাঙ্কবিশিষ্ট ছোট সরু তার যা টিন (২৫%) ও সীসা (৭৫%) এর মিশ্রণে তৈরি একটি সংকর ধাতু।
সার্কিট ব্রেকার (Circuit Breaker)
সার্কিট ব্রেকার এক ধরনের ফিউজ যা স্বয়ংক্রিয়ভাবে বর্তনী ভেঙ্গে দেয় আবার জোড়া লাগায়। বর্তনীতে কোনো কারণে হঠাৎ প্রবাহ বেড়ে সার্কিট ব্রেকার অফ হয়ে যায়। আবার বিদ্যুৎ প্রবাহ স্বাভাবিক হলে তা স্বয়ংক্রিয়ভাবে অন হয়ে যায়। এভাবে সার্কিট ব্রেকার অতিমাত্রায় বিদ্যুৎ প্রবাহজনিত দুর্ঘটনা পথকে উদ্দেশ্যে বৈদ্যুতিক যন্ত্রপাতিকে রক্ষা করে।
# বহুনির্বাচনী প্রশ্ন
তাড়িত চৌম্বক আবেশ (Electromagnetic Induction)
কোন তার বা তার কুন্ডলীর কাছে আমরা যদি কোন চুম্বককে নাড়াচাড়া করি বা আনা নেওয়া করি বা কোন চুম্বকের নিকট কোন তার কুন্ডলীকে আনা নেওয়া করি, তাহলে তার কুন্ডলীতে তড়িৎপ্রবাহ উৎপন্ন করে। একে তাড়িতচৌম্বক আবেশ বলে। ব্রিটিশ বিজ্ঞানী মাইকেল ফ্যারাডেকে তাড়িতচৌম্বক আবেশের আবিষ্কর্তা বলা হয়।
দূর-দূরান্তে তড়িৎ প্রেরণ
পাওয়ার স্টেশনে তড়িৎ উৎপাদন করা হয়। তড়িৎকে পাওয়ার স্টেশন থেকে একটি প্রেরণ ব্যবস্থার মাধ্যমে সারাদেশে পাঠানো হয়। এই ব্যবস্থায় পাওয়ার স্টেশনগুলো পরস্পরের সাথে সংযুক্ত থাকে। এই ব্যবস্থার নাম জাতীয় গ্রীড। তড়িৎ প্রেরণ করা হয় তারের মাধ্যমে। এ সব তার উচু টাওয়ারের মাধ্যমে টানানো থাকে। প্রেরক তারে যে রোধ থাকে তা খুব সামান্য কিন্তু এই রোধ তাৎপর্যপূর্ণ রোধের কারণে তড়িৎ প্রবাহের সময় তড়িৎ শক্তি তাপ শক্তি হিসাবে অপচয় হয়। দূরত্ব যত বেশি হয়, অপচয়ও তত বেশি হয়। এজন্য অধিক দূরত্বে তড়িৎ প্রেরণের সময় অপচয় রোধকল্পে আরোহী বা স্টেপআপ ট্রান্সফর্মারের সাহায্যে তড়িৎ প্রবাহ কমিয়ে ভোল্টেজ বাড়ানো হয়। এজন্য টাওয়ারের তারে উচ্চভোল্টেজের তড়িৎ থাকে, কিন্তু তড়িৎ প্রবাহের মান কম থাকে।
উচ্চ ভোল্টেজ এবং কম মানের তড়িৎ প্রবাহ গ্রাহকের ব্যবহার উপযোগী নয়। তাই এই ভোল্টেজ আবার অনেকগুলো অবরোহী বা নিম্নধাপী ট্রান্সফর্মারের মধ্য দিয়ে চালনা করা হয়। এতে ভোল্টেজ কমে যায় এবং তড়িৎ প্রবাহের মান বৃদ্ধি পায়। ফলে তড়িৎ গ্রাহকের উপযোগী হয়। বাংলাদেশে উচ্চ ভোল্টেজকে কমিয়ে ২২০ V নিয়ে আসা হয়।
ইলেক্ট্রনিক্স (Electronics)
P টাইপ ও n টাইপ অধৃপরিবাহী
সিলিকনের বহির্খোলকে থাকে চারটি ইলেকট্রন যা যোজন ইলেক্ট্রন রূপে কাজ করে। সিলিকনের সবচেয়ে স্থিত গঠনের জন্য এর চারটি ইলেক্ট্রন লাভ করা অর্থাৎ ভাগাভাগি বা শেয়ার করার প্রবণতা থাকে। বিশুদ্ধ সিলিকন পরমাণুর বহিঃস্থ যোজন ইলেকট্রন সহযোগী অনুবন্ধের মাধ্যমে সংযুক্ত হয়, ফলে সিলিকনে কোনো মুক্ত ইলেকট্রন থাকে না। বিশুদ্ধ সিলিকন তাই উত্তম অন্তরক। সামান্য তাপমাত্রা বৃদ্ধি করলে সিলিকনের কিছু কিছু অনুবন্ধ ভেঙ্গে যায় এবং ইলেকট্রন চলাচলের জন্য মুক্ত হতে থাকে, ফলে তড়িৎ প্রবাহের সৃষ্টি হয়। সিলিকনকে আরেক ভাবে তড়িৎ পরিবাহী করা যায়। এই কাজটি করা হয় বিশুদ্ধ সিলিকনের সাথে খুব সামান্য ভেজাল নিয়ন্ত্রিতভাবে মিশিয়ে। একে বলা হয় ডোপায়ন (Doping)। ডোপিত মৌলের প্রকৃতি থেকে নির্ধারিত হয় সিলিকন p-টাইপ (ধনাত্মক টাইপ) হবে না n-টাইপ (ঋণাত্মক টাইপ) হবে। যে সব মৌলের (যেমন: অ্যালুমিনিয়াম, বোরন, গ্যালিয়াম বা ইনডিয়াম) তিনটি যোজন ইলেকট্রন থাকে, তাদের ভেজাল হিসেবে ব্যবহার করা হলে সিলিকন বা জার্মেনিয়াম p-টাইপ বস্তুতে p-টাইপ অর্ধপরিবাহীতে পরিণত হয়। যে সকল মৌলের (যেমন; ফসফরাস, আর্সেনিক বা অ্যান্টিমনি) বহির্খোলকে পাঁচটি ইলেকট্রন থাকে, তাদের ভেজাল হিসেবে ব্যবহার করা হলে সিলিকন বা জার্মেনিয়াম n-টাইপ বস্তুতে বা n-টাইপ অর্ধপরিবাহীতে পরিণত হয়।
# বহুনির্বাচনী প্রশ্ন
অর্ধপরিবাহী ডায়োড (Semiconductor Diode)
একটি p টাইপ অর্ধপরিবাহী ও একটি n টাইপ অর্ধপরিবাহী পাশাপাশি জোড়া লাগিয়ে p-n জংশন ডায়োড তৈরি করা হয়। এটি মূলত রেকটিফায়ার হিসেবে কাজ করে। রেকটিফায়ার এসি (পরিবর্তী) প্রবাহকে ডিসি (একমুখী) প্রবাহে রূপান্তর করে।
ক) সন্মুখী ঝোঁক (Forward Bias) অবস্থায় থাকলে p-n জংশন দিয়ে তড়িৎপ্রবাহ চলবে।
খ) বিমুখী ঝোঁক (Reverse Bias) অবস্থায় থাকলে p-n জংশন দিয়ে কোন তড়িৎ প্রবাহ চলে না।
# বহুনির্বাচনী প্রশ্ন
অ্যাডাপ্টার (Adapter)
একটি বৈদ্যুতিক সিস্টেম বা ডিভাইসের জন্য বেমানান কোন বৈশিষ্ট্যকে এডাপ্টারের সাহায্যে সিস্টেমটির জন্য গ্রহণযোগ্য বৈশিষ্ট্যকে এডাপ্টারের সাহায্যে সিস্টেমটির জন্য গ্রহণযোগ্য বৈশিষ্টে রূপান্তর করা হয়। যেমন: মোবাইলের চার্জার এক ধরণের অ্যাডাপ্টার কারণ এটি বাসা-বাড়ীর বিদ্যুৎ সরবরাহ লাইনের ২২০ ভোল্ট এসি প্রবাহ মোবাইলের জন্য গ্রহণযোগ্য নিম্ন ভোল্টেজ ডিসি প্রবাহে রূপান্তর করে।
# বহুনির্বাচনী প্রশ্ন
ভোল্টেজ
কারেন্ট
ইম্পিডেন্স
ক্যাপসিটেপ
ট্রানজিস্টর
১৯৪৮ সালে তার ট্রানজিস্টর (Trasistor) আবিষ্কৃত হবার পর কম্পিউটারে ভাল্বের বদ্লে ট্রানজিস্ট্ররের ব্যবহার শুরু হয়। ট্রানজিস্টর ব্যবহৃত কম্পিউটার ছোট হয়ে যেতে শুরু করে। কম্পিউটার গুলো আগের কম্পিউটার অপেক্ষা উন্নত ছিল। দুটি অর্ধপরিবাহী ডায়োড কি পাশাপাশি যুক্ত করে একটি অর্ধপরিবাহী ট্রায়োড তৈরি করা হয়। একে ট্রানজিস্টর বলা হয়। আমেরিকার বেল ল্যাবরেটরিতে ১৯৪৮ সালে জন বারডিন (Jhon Bardeen), উইলিয়াম শকলে (William Shocley) এবং ওয়াল্টার ব্রাটেইন (Walter Brattain) ট্রানজিস্টর উদ্ভাবন করেন। ট্রানজিস্টর আবিষ্কারের মধ্য দিয়ে ইলেকট্রনিক্স বিপ্লব শুরু হয়। ট্রানজিস্টর তৈরিতে অর্ধপরিবাহী (Semiconductor) এর প্রয়োজন হয়। এতে অর্ধপরিবাহী হিসাবে সিলিকন বা জার্মেনিয়াম ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
অ্যামপ্লিফায়ার (Amplifier)
যে যন্ত্র এর অন্তর্গামীতে (Input) প্রদত্ত সংকেতকে বর্হিগামীতে বিবর্ধিত (Amplify) করে, তাকে অ্যামপ্লিফায়ার বলে। কার্যক্ষমতার উপর নির্ভর করে তিন শ্রেণীর অ্যামপ্লিফায়ার আছে। যথা- এ ম্রেণী, বি শ্রেণী, সি শ্রেণী। এ ক্লাস বা শ্রেণী অ্যামপ্লিফায়ার কার্যক্ষমতা সবচেয়ে বেশি, প্রায় ৯০%।
# বহুনির্বাচনী প্রশ্ন
৯০°
১৮০°
০°
৭০°
সমন্বিত বর্তনী (Integrated Circuit or I.C)
আধুনিক কম্পিউটারের দ্রুত অগ্রগতির মূলে রয়েছে ইন্টিগ্রেটেড সার্কিট। ১৯৫৮ সালে জ্যাক কেলবি (Jack Kilby) নামক একজন বিজ্ঞানী Transistor, Registor এবং Capacitor সমন্বিত করে একটি সার্কিট তৈরি করেন যা IC নামে পরিচিতি লাভ করে। আইসি ব্যবহারের ফলে কম্পিউটারের আকার ছোট হয় এবং এর ক্ষমতা অনেক বেড়ে যায়- সঙ্গে সঙ্গে কমে আসে কম্পিউটারের মূল্য এবং হিসাব-নিকাশের সময়।
# বহুনির্বাচনী প্রশ্ন
সিরিজ সার্কিট
প্যারালাল সার্কিট
মিশ্র সার্কিট
স্ট্রিং সার্কিট
দৈনন্দিন জীবনের প্রতিটি মুহূর্তে, হাঁটা থেকে শুরু করে স্মার্টফোন ব্যবহার পর্যন্ত, পদার্থবিজ্ঞানের সূত্র কার্যকর থাকে। ঘর্ষণ, মহাকর্ষ, আলোকবিজ্ঞান, তাপগতিবিদ্যা এবং বিদ্যুৎ—এসবই আমাদের সকালের অ্যালার্ম থেকে শুরু করে রাতের লাইট বন্ধ করা পর্যন্ত প্রতিটা কাজকে সহজ ও আধুনিক করে তোলে।
দৈনন্দিন জীবনে পদার্থবিজ্ঞানের উল্লেখযোগ্য উদাহরণ:
চলন ও ঘর্ষণ: মেঝেতে হাঁটা, সাইকেল চালানো বা গাড়ির ব্রেক করা—সবই ঘর্ষণ এবং গতির (Newton's Laws) ওপর নির্ভরশীল ।
গৃহস্থালি সরঞ্জাম: পানির কেটলি ফুটানো (তাপগতিবিদ্যা), খাবার গরম করার মাইক্রোওয়েভ (তড়িৎচৌম্বক তরঙ্গ), এবং রেফ্রিজারেটর (তাপ স্থানান্তর) পদার্থবিজ্ঞানের প্রয়োগ ।
স্মার্টফোন ও যোগাযোগ: টাচস্ক্রিন, ওয়াইফাই, এবং ব্লুটুথ—এগুলো তড়িৎচৌম্বক ক্ষেত্র ও তরঙ্গ প্রযুক্তির উদাহরণ ।
আলো ও দৃষ্টি: আয়নায় নিজের প্রতিবিম্ব দেখা, চশমা বা কন্টাক্ট লেন্স ব্যবহার—সবই আলোর প্রতিফলন ও প্রতিসরণের (Optics) নিয়ম মেনে চলে ।
মহাকর্ষ: কলম হাত থেকে নিচে পড়া, বা সাইকেলের ভারসাম্য বজায় রাখা—মহাকর্ষ এবং জড়তার (Inertia) উদাহরণ।
এছাড়াও, বিদ্যুৎ উৎপাদন, টেলিভিশন, উড়োজাহাজ ও জিপিএস (GPS) প্রযুক্তি—সবকিছুর মূলেই রয়েছে পদার্থবিজ্ঞানের মৌলিক নিয়মাবলি ।
# বহুনির্বাচনী প্রশ্ন
৬০
১২০
৯০
৩৬০
নীল আলোর তরঙ্গদৈর্ঘ্য বেশি বলে
নীল আলোর বিক্ষেপণ অপেক্ষাকৃত বেশি বলে
নীল সমুদ্রের প্রতিফলনের ফলে
নীল আলোর প্রতিফলন বেশি বলে
বৈদ্যুতিক বাতি (Electric Bulb)
কোনো পরিবাহী তারের ভিতর দিয়ে বিদ্যুৎ প্রবাহিত করলে তারটি গরম হয়। তার যত সরু হয়, তত বেশি গরম হয়অ আর যত বেশি গরম হয়, তত বেশি লাল হয়ে শেষে সাদা ও উজ্জ্বল হয়ে যায়। ফলে তারটি থেকে আলো বের হয়। বৈদ্যুতিক বাল্বে এই ঘটনাই ঘটে। বৈদ্যুতিক বাল্বের ভিতরে খুব সরু তারের একটি কুন্ডলী থাকে। এ কুন্ডলীকে ফিলামেন্ট বলে। ফিলামেন্টটি টাংস্টেনের তার দিয়ে তৈরি। এর গলনাঙ্ক অত্যন্ত বেশি (প্রায় ৩৪১০০ সে.) ফলে অধিক তাপে এটি জারিত হয় না। বৈদ্যুতিক বাল্বটি সম্পূর্ণরূপে বায়ুশূন্য থাকে তবে সামান্য পরিমাণে নাইট্রোজেন বা নিষ্ক্রিয় গ্যাস (আর্গন) থাকে। নাইট্রোজেন গ্যাস সাধারণ বৈদ্যুতিক বাল্বের ভিতরে এবং নিয়ন, আর্গন প্রভৃতি নিষ্ক্রিয় গ্যাস টিউব লাইটে ব্যবহৃত হয়। মার্কিন বিজ্ঞানী টমাস এডিসন ১৮৭৯ সালে সর্বপ্রথম বৈদ্যুতিক বাতি আবিষ্কার করেন।
# বহুনির্বাচনী প্রশ্ন
বৈদ্যুতিক ইস্ত্রি (Electric Iron)
বৈদ্যুতিক ইস্ত্রিতে একটি অভ্রের প্লেটের গায়ে সংকর ধাতু নাইক্রোমের (নিকেল-৬০% + আয়রন-২৫% + ক্রোমিয়াম-১৫%) সরুতার জড়ানো থাকে। এই প্লেটের উপরে ও নিচে দুটি অভ্রের পাত দিয়ে ঢেকে লোহার পাত দিয়ে চেপে রাখা হয়। অভ্র বিদ্যুৎ অপরিবাহী কিন্তু তাপ পরিবাহী। তাই তারের ভিতর দিয়ে বিদ্যুৎ প্রবাহিত করলে তা লোহাকে স্পর্শ করে না কিন্তু তার উত্তপ্ত হলে তা লোহাকে উত্তপ্ত করে। ইস্ত্রির বাহিরের আবরণটি স্টেইনলেস স্টীলের তৈরি, ত্রিভুজাকৃতি এবং ভারী। কুন্ডলীর ভিতর দিয়ে বিদ্যুৎ প্রবাহিত করলে বাহিরের আবরণটি উত্তপ্ত হয়।
# বহুনির্বাচনী প্রশ্ন
ফটোকপি মেশিন (Photocopier)
অধিকাংশ ফটোকপি মেশিন পোলারয়েড পদ্ধতিতে কাজ করে থাকে। ফটোকপি মেশিনের ভেতরে একটি ড্রাম ও একটি টোনার থাকে। প্রথমে ড্রামটিকে আহিত বা চার্জিত করা হয়। চার্জিত হওয়ার পর এটি এক ধরণের আকর্ষণের মাধ্যমে টোনারের খণাকে আকর্ষণ করে। ফলে ফটোকপি মেশিন কোন কালো লেকার কাগজকে অবিকল কপি করে ফেলতে পারে। বর্তমানে ফটোস্ট্যাস্ট মেশিনে সেলেনিয়াম মৌলটি ব্যবহার করা হয়।
# বহুনির্বাচনী প্রশ্ন
অফসেট মুদ্রণ পদ্ধতিতে
পোলারয়েড ফটোগ্রাফি পদ্ধতিতে
ডিজিট্যাল ইমেজিং পদ্ধতিতে
স্থির বৈদ্যুতিক ইমেজিং পদ্ধতিতে
টেলিগ্রাফ (Telegraph)
টেলিগ্রাফি হচ্ছে দূর দূরান্তে লিখিত বার্তা বা পত্র প্রেরণের এমন একটি পদ্ধতি যা মূল লিখিত পত্রটিকে প্রেরণ না করে সাধারণত তারের মাধ্যমে প্রেরিত মোর্স কোডে লিখিত টেলিগ্রাফি বার্তাকে টেলিগ্রাম বলা হতো। মোর্স কোড কোন ভাষার বর্ণকে কোডে রূপান্তরের এক ধরণের পদ্ধতি। স্যামুয়েল মোর্স ১৮৪০ সালে এ কোড তৈরি করেন। মোর্স কোড কোন উপাদানের ‘সংক্ষিপ্ত এবং দীর্ঘ’ এ দুটি আবশ্যকীয় ্েুপাদান নিয়ে গঠিত। এতে ডট (.) ‘টরে’ এবং ড্যাশ (-) কে ‘টক্কা’ বলে।
টেলিফোন, টেলেক্স ও ফ্যাক্স (Telephone-Telex-Fax)
টেলিফোন বা দুরালাপনি একটি যোগাযোগের মাধ্যম। ১৮৭৬ খ্রিস্টাব্দে স্কটিশ বিজ্ঞানী আলেকজান্ডার গ্রাহম বেল টেলিফোন আবিষ্কার করেন। টেলিফোনে যেমন নম্বর আছে, টেলেক্স এবং ফ্যাক্সে তেমন নম্বর আছে। টেলেক্স এক ধরণের টেলিপ্রিন্টার। এতে একটি টাইপরাইটার থাকে। যে তথ্য, সংবাদ বা চিঠি প্রেরণ করতে হবে তা এ টাইপ রাইটারে টাইপ করতে হয়। প্রেরিত শব্দ বা কথাবর্তা টেলিপ্রিন্টারের সাহায্যে টাইপ হয়ে প্রাপকের নিকট পৌঁছে যায়। ফ্যাক্স মেশিন একটি টেলিফোনের সাথে যুক্ত থাকে। যে তথ্য প্রেরণ করতে হবে তা একটি কাগজে টাইপ করে বা লিখে রাখতে হয়। যে নাম্বারে ফ্যাক্স প্রেরণ করতে হবে সেই নম্বর ডায়াল করে কাগজটি মেশিনে ঢুকিয়ে দেয়া হয়। অপর প্রান্তে তার হুবহু নকল বেরিয়ে আসে।
# বহুনির্বাচনী প্রশ্ন
টেলিফোন, টেলেক্স ও ফ্যাক্স (Telephone-Telex-Fax)
টেলিফোন বা দুরালাপনি একটি যোগাযোগের মাধ্যম। ১৮৭৬ খ্রিস্টাব্দে স্কটিশ বিজ্ঞানী আলেকজান্ডার গ্রাহম বেল টেলিফোন আবিষ্কার করেন। টেলিফোনে যেমন নম্বর আছে, টেলেক্স এবং ফ্যাক্সে তেমন নম্বর আছে। টেলেক্স এক ধরণের টেলিপ্রিন্টার। এতে একটি টাইপরাইটার থাকে। যে তথ্য, সংবাদ বা চিঠি প্রেরণ করতে হবে তা এ টাইপ রাইটারে টাইপ করতে হয়। প্রেরিত শব্দ বা কথাবর্তা টেলিপ্রিন্টারের সাহায্যে টাইপ হয়ে প্রাপকের নিকট পৌঁছে যায়। ফ্যাক্স মেশিন একটি টেলিফোনের সাথে যুক্ত থাকে। যে তথ্য প্রেরণ করতে হবে তা একটি কাগজে টাইপ করে বা লিখে রাখতে হয়। যে নাম্বারে ফ্যাক্স প্রেরণ করতে হবে সেই নম্বর ডায়াল করে কাগজটি মেশিনে ঢুকিয়ে দেয়া হয়। অপর প্রান্তে তার হুবহু নকল বেরিয়ে আসে।
রেডিও (Radio)
বেতার হল তার ব্যতীত যোগাযোগের একটি শক্তিশালী মাধ্যম। এতে তড়িৎ চৌম্বকীয় তরঙ্গ ব্যবহার করে তথ্য প্রেরণ বা গ্রহণ করা হয়। ১৮৯৬ সালে ইতালীয় প্রকৌশলী গুলিয়েলমো মার্কোনি বেতার যন্ত্রের সম্প্রচার পদ্ধতি উদ্ভাবন করেন। রেডিও, রেডিও টেলিস্কোপ ইত্যাদি তারবিহীন যে কোনো যোগাযোগের মূলনীতিই হলো বেতার। মার্কোনির আগেই স্যার জগদীশচন্দ্র বসু রেডিও আবিষ্কার করেছিলেন বলে বাঙালি মহলে একটি ধারণা প্রচলিত আছে। মার্কোনি আধুনিক ছোট বা শর্ট তরঙ্গ মাপের বেতার তরঙ্গ ব্যবহার করে দূরে বেতার সংকেত পাঠাতে সফল হয়েছিলেন যার ফলশ্রুতি হলো রেডিও। কিন্তু জগদীশচন্দ্র কাজ করেছিলেন অতি ক্ষুদ্র তথা মাইক্রোওয়েভ তরঙ্গ নিয়ে যার প্রয়োগ ঘটে আধুনিক টেলিভিশন, রাডার এবং মোবাইল যোগাযোগের ক্ষেত্রে।
# বহুনির্বাচনী প্রশ্ন
টেলিভিশন (Television)
টেলিভিশন হলো এমন একটি যন্ত্র যার সাহায্যে আমরা দূরবর্তী কোনো স্থান থেকে শব্দ এবং ছবি দেখতে পাই। স্কটিশ বিজ্ঞানী জন লজি বেয়ার্ড (John Logie Baird) ১৯২৬ সালে টেলিভিশন আবিষ্কার করেন। টেলিভিশনে ছবি প্রেরণের সময় ছবিকে যে পদ্ধতিতে ক্ষুদ্র ক্ষুদ্র অংশে বিভক্ত করা হয়, তাকে স্ক্যানিং বলা হয়। বাংলাদেশে টিভি সম্প্রচারে বা বেতার কেন্দ্রগুলোর ক্ষেত্রে অডিও সিগন্যালের ফ্রিকুয়েন্সি মডুলেশন করে পাঠানো হয়।
# বহুনির্বাচনী প্রশ্ন
রাডার (Radar)
RADAR (Radio Detection And Ranging) এমন একটি যন্ত্র যার সাহায্যে দূরবর্তী কোনো বস্তুর উপস্থিতি, দূরত্ব ও দিক নির্ণয় করা যায়। রাডার হল এমন একটি কৌশল বা ব্যবস্থা যার সাহায্যে রেডিও প্রতিধ্বনির মাধ্যমে কোন বস্তুর উপস্থিতি জানা যায়। যুদ্ধে শত্রু বিমানের উপস্থিতি ও গতিবিধি, বিমানের পথ নির্দেশ, ঝড়ের পূর্বাভাস ইত্যাদি কাজে এটি ব্যবহৃত হয়। ১৯২২ সালে এ এইট টেলর এবং লিও সি ইয়ং রাডার উদ্ভাবন করেন।
# বহুনির্বাচনী প্রশ্ন
গামা রশ্মি
মাইক্রোওয়েভ
অবলোহিত বিকিরণ
আলোক তরঙ্গ
উড়োজাহাজ ও হেলিকপ্টার (Aeroplane & Helecopter)
রেনেসাঁ যুগে উন্নত উড্ডয়ন যন্ত্রের চিত্র অঙ্কন করেন শিল্পী লিওনার্দো দ্য ভিঞ্চি। তিনি সর্বপ্রথম আকাশে উড়ার একটি তাত্ত্বিক ধারণাও দেন। তাঁর ডিজাইন করা উড্ডয়ন যন্ত্রের নাম দিয়েছিলেন ‘ওরিনিথপ্টার’। ১৪৯৬ সালে তিনি এর পরীক্ষামূলক উড্ডয়নের চেষ্টা করলেও তা সফল হয় নি। প্রথম উড়োজাহাজ বা এরোপ্লেন বানিয়েছিলেন অরভিল রাইট এবং উইলবার রাইট ভ্রাতৃদ্বয়। যুক্তরাষ্ট্রের নর্থ ক্যারোলিনার কিল ডেভিল হিলস ১৯০৩ সালে ১৮ ডিসেম্বর তাঁরা Flyer-1 এর সফল উড্ডয়ন করান। কোন স্থানে খাড়া ভাবে উড়তে (take off) ও নামতে (landing) হেলিকপ্টার ব্যবহার করা হয়। হেলিকপ্টারের জন্ম মানুষের ওড়াউড়ির প্রথম অর্ধশতাব্দীর মধ্যে হলেও ১৯৪২ সালে ইগর সিকোরস্কির তৈরি করা নকশার হেলিকপ্টারই প্রথম বাণিজ্যিকভাবে উৎপাদিত হয়। কোন বিমান বিধ্বস্ত হলে দুর্ঘটনাটির কারণ উদঘাটনের জন্য বিমানের ব্ল্যাক বক্স খুবই গুরুত্বপূর্ণ। বিমান পরিবহন ব্যবস্থায় বিমানের উড্য়ন কালের যাবতীয় তথ্য রেকর্ডের ডিভাইস হলো flight data recorder এবং উড্ডয়নকালে ককপিটের সবরকম কথাবার্তা ও শব্দ রেকর্ডের ডিভাইস হচ্ছে cockpit voice recorder। এই ডিভাইসগুলোর আরেক নাম ব্ল্যাক বক্স। এই ব্ল্যাক বক্সগুলো সাধারণত লাল বা কমলা রংয়ের হয় যাতে বিমানের ধ্বংসাবশেষ থেকে বক্সগুলো সহজে সনাক্ত করা যায়। বিজ্ঞান প্রযুক্তিতে black box একটি টেকনিক্যাল টার্ম, যার থেকে এই নামকরণ। ব্ল্যাক বক্সগুলো এমনভাবে প্রস্তুত করা হয় যে উচ্চমাত্রার তাপ ও চাপ এর কোন ক্ষতি করতে পারে না।
পলিগ্রাফ (Polygraph)
মিথ্যা ধরার যন্ত্রকে পলিগ্রাফ বলে। ১৯২১ সালে জন এ লারসন পলিগ্রাফ আবিষ্কার করেন। মিথ্যা ধরার সবচেয়ে বড় হাতিয়ার হলো মিথ্যাবাদীর শরীর। একজন মানুষ যখন মিথ্যা কথা বলে তখন সাধারণত তার শ্বাস-প্রশ্বাস হার, হৃদস্পন্দন, রক্তচাপ, ঘাম প্রভৃতির কিছু পরিবর্তন লক্ষ্য করা যায়। পলিগ্রাফ এই পরিবর্তনগুলোকেই পর্যালোচনা করে।
# বহুনির্বাচনী প্রশ্ন
আধুনিক পদার্থবিজ্ঞান হলো পদার্থবিজ্ঞানের সেই শাখা যা বিংশ শতাব্দীর শুরু থেকে বিকশিত হয়েছে এবং মূলত অতি ক্ষুদ্র (পারমাণবিক ও উপ-পারমাণবিক) বা অতি দ্রুত (আলোর গতির কাছাকাছি) গতির বিষয়গুলো নিয়ে কাজ করে। ১৯০০ সালে ম্যাক্স প্লাঙ্কের কোয়ান্টাম তত্ত্ব আবিষ্কারের মাধ্যমে এই যুগের সূচনা হয় ।
আধুনিক পদার্থবিজ্ঞানের প্রধান শাখা ও ধারণা
আধুনিক পদার্থবিজ্ঞান মূলত দুটি স্তম্ভের ওপর দাঁড়িয়ে আছে:
আপেক্ষিকতা তত্ত্ব (Theory of Relativity): বিজ্ঞানী আলবার্ট আইনস্টাইন প্রবর্তিত এই তত্ত্ব স্থান, সময় এবং ভরের পারস্পরিক সম্পর্ক ব্যাখ্যা করে। এটি মূলত মহাজাগতিক স্কেলে কাজ করে ।
কোয়ান্টাম বলবিদ্যা (Quantum Mechanics): এটি পরমাণু এবং এর ভেতরের অতি ক্ষুদ্র কণিকাগুলোর (যেমন- ইলেকট্রন, প্রোটন) আচরণ ব্যাখ্যা করে। এই তত্ত্বে সম্ভাব্যতা নীতির গুরুত্ব বেশি।
উল্লেখযোগ্য অন্যান্য ক্ষেত্র
পারমাণবিক পদার্থবিজ্ঞান (Atomic Physics): পরমাণুর গঠন ও ইলেকট্রনের বিন্যাস নিয়ে আলোচনা করে।
নিউক্লীয় পদার্থবিজ্ঞান (Nuclear Physics): পরমাণুর কেন্দ্র বা নিউক্লিয়াস এবং তেজস্ক্রিয়তা নিয়ে কাজ করে ।
কণা পদার্থবিজ্ঞান (Particle Physics): মহাবিশ্বের মৌলিক কণিকাগুলো (যেমন- হিগস বোসন) নিয়ে গবেষণা করে।
কঠিন অবস্থার পদার্থবিজ্ঞান (Solid State Physics): কঠিন পদার্থের অভ্যন্তরীণ গঠন ও বৈশিষ্ট্য নিয়ে আলোচনা করে, যা আধুনিক ইলেকট্রনিক্সের ভিত্তি ।
আধুনিক পদার্থবিজ্ঞানের প্রভাব
আধুনিক পদার্থবিজ্ঞানের ওপর ভিত্তি করেই বর্তমানের লেজার, কম্পিউটার, স্মার্টফোন, এমআরআই (MRI) মেশিন এবং পারমাণবিক শক্তি উৎপাদিত হচ্ছে । আলবার্ট আইনস্টাইনকে প্রায়ই "আধুনিক পদার্থবিজ্ঞানের জনক" বলা হয় ।
# বহুনির্বাচনী প্রশ্ন
স্টিফেন হকিং
মাও সেতুং
বারাক ওবামা
অমর্ত্য সেন
১০ কি.মি.
১২ কি.মি.
১৪ কি.মি.
১৬ কি.মি.
রঞ্জন রশ্মি বা অজানা রশ্মি (X-ray)
ক্যাথোড রশ্মি হচ্ছে এক রাশি ইলেকট্রন। বিজ্ঞানী উলহহেলম রন্টজেন আবিষ্কার করেন যে, তড়িৎক্ষরণ নল থেকে যখন ক্যাথোড রশ্মি নলের দেয়ালে পড়ে তখন এক্সরে উৎপন্ন হয়। এক্সরে হলো ক্ষুদ্র তরঙ্গদৈর্ঘ্য বিশিষ্ট তাড়িত চৌম্বক বিকিরণ। এক্সরে উচ্চ ভেদন ক্ষমতা সম্পন্ন। এক্সরে হীরকের ভিতর দিয়ে যেতে পারে কিন্তু গ্রাফাইটের ভিতর দিয়ে যেতে পারে না। স্থানচ্যুত হাড়, হাড়ে দাগ বা ফাটল, ভেঙ্গে যাওয়া হাড়, শরীরের ভিতরের কোনো বস্তুর বা ফুসফুসে কোনো ক্ষতের অবস্থান নির্ণয়ে, গোয়েন্দা বিভাগে যেমন; কাঠের বাক্স বা চামড়ার থলিতে বিস্ফোরক লুকিয়ে রাখলে তা খুঁজে বের করতে এক্স রশ্মি ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
The flow of positive charge
Electromagnetic wave
The flow of natural particles
The flow of electron
তেজস্ক্রিয়তা (Radioactivity)
ভারী মৌলিক পদার্থের নিউক্লিয়াস থেকে স্বতঃস্ফুর্তভাবে আলফা, বিটা ও গামা রশ্মি নির্গমনের প্রক্রিয়াকে তেজস্ক্রিয়তা বলে। যে সকল মৌল হতে তেজষ্ক্রিয় রশ্মি নির্গত হয়, তাকে তেজস্ক্রিয় মৌল বলে। যে সকল মৌলের পারমাণবিক সংখ্যা ৮২ এর বেশি, সাধারণত সে সকল মৌল তেজস্ক্রিয় হয়। যেমন: ইউরেনিয়াম, প্লুটোনিয়াম, নেপচুনিয়াম, রেডিয়াম, রেডন, থোরিয়াম ইত্যাদি তেজস্ক্রিয় পদার্থ। আন্তর্জাতিক (SI) পদ্ধতিতে তেজস্ক্রিয়তার একক পরিমাপের একক বেকেরেল (Bq)। হেরি বেকরেল ১৯০৩ সালে তেজষ্ক্রিয়তা আবিষ্কারের জন্য পদার্থবিজ্ঞানে নোবেল পুরস্কার লাভ করেন।
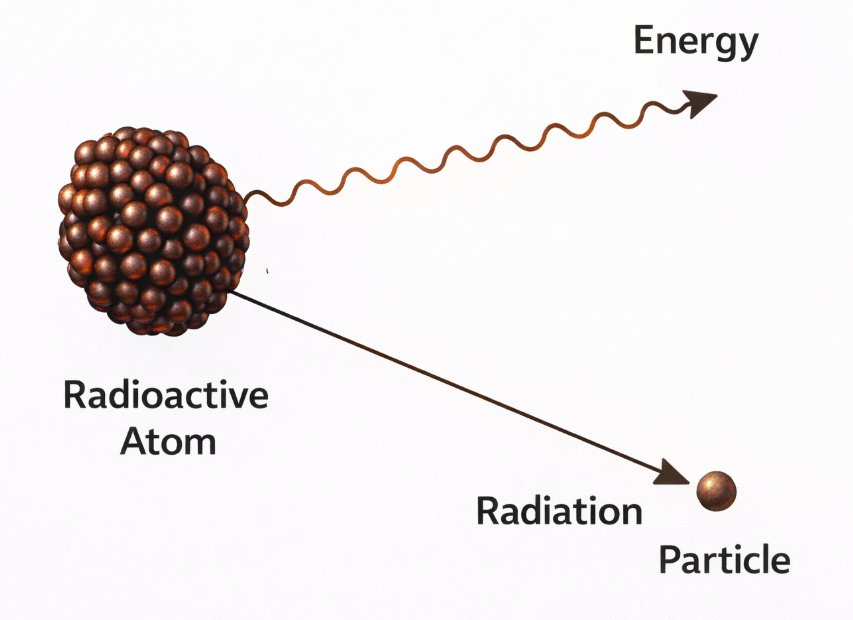
তেজস্ক্রিয় আইসোটোপ (Radioactive Isotopes)
অস্থিত আইসোটোপগুলো স্বতঃস্ফুর্তভাবে বিভিন্ন ধরনের রশ্মি বিকিরণ করে নিজের নিউক্লিয়াসে পরিবর্তন এনে অন্য মৌলের স্থিত আইসোটোপে পরিণত হয়, এই ধরনের আইসোটোপ গুলোকে তেজস্ক্রিয় আইসোটোপ বলে। যেমন; Carbon-14, ইউরেনিয়াম-২৩৬, আয়োডিন-১৩০ ইত্যাদি রেডিও আইসোটোপ। Carbon-14 এর অর্ধায়ু ৫৭৩০ বছর। গলগণ্ড রোগ নির্ণয়ে রেডিও আইসোটোপ ব্যবহৃত হয়। রেডিও আইসোটোপ থেকে নির্গত গামা রশ্মি টিউমার, ক্যান্সার প্রভৃতি রোগের চিকিৎসায় ব্যবহৃত হয়।
আলফা, বিটা ও গামা রশ্মি (Alfa, Beta and Gamma rays)
আলফা (): এটি একটি হিলিয়াম নিউক্লিয়াস বা দ্বি-আয়নিত হিলিয়াম পরমাণু। আলফা রশ্মি ধনাত্মক আধানযুক্ত। এই রশ্মি চৌম্বক ও তড়িৎ ক্ষেত্র দ্বারা বিচ্যুত হয়।
বিটা (): এই রশ্মি অতি উচ্চ দ্রুতি সম্পন্ন ইলেকট্রনের প্রবাহ। বিটা রশ্মির ঋণাত্মক আধানযুক্ত। এই রশ্মি চৌম্বক ও তড়িৎ ক্ষেত্র দ্বারা বিক্ষিপ্ত হয়।
গামা (): গামা রশ্মি অত্যন্ত ক্ষুদ্র তরঙ্গদৈর্ঘ্যের তাড়িত চৌম্বক বিকিরণ। এর কোনো চার্জ বা ভর নেই এবং ইহা চৌম্বক ক্ষে দ্বারা বিক্ষিপ্ত হয় না। এটি জীবজগতের জন্যে অত্যন্ত ক্ষতিকারক। তবে টিউমার, ক্যান্সার প্রভৃতি রোগের চিকিৎসায় এ রশ্মি ব্যবহার করা হয়। ক্যান্সার চিকিৎসায় ব্যবহৃত গামা বিকিরণের উৎস হলো -আইসোটোপ।
# বহুনির্বাচনী প্রশ্ন
এক্সয়ে
লেন্সের ক্ষমতা
তেজস্ক্রিয়তা
দীপন ক্ষমতা
প্রাকৃতিক সম্পদ (Natural resource)
প্রকৃতি থেকে আমরা যা কিছু পাই, তাই প্রাকৃতিক সম্পদ। প্রাকৃতিক সম্পদকে নবায়নযোগ্য (Renewable) ও নবায়ন অযোগ্য (Non Renewable) এই দুটি শ্রেণিতে ভাগ করা যায়।
নবায়নযোগ্য জ্বালানি (Renewable energy):
যে শক্তি বারবার ব্যবহার করা যায়, ব্যবহার ফলে যা নিঃশেষ হয়ে যায়না তাকে নবায়নযোগ্য জ্বালানি বলে। যেমন- সৌরশক্তি (Solar energy), বায়ুশক্তি (Wind energy), সমুদ্রস্রোত (Sea current), পরমাণুশক্তি (Atomic energy) প্রভৃতি। সূর্য সকল শক্তির উৎস। সূর্যে হাল্কা পরমাণুর ফিউশনের মাধ্যমে শক্তি উৎপন্ন হয়। সৌরকোষের (Solar cell) বিদ্যুৎ রাতেও ব্যবহার করা সম্ভব যদি এর সঙ্গে থাকে স্টোরেজ ব্যাটারি। সৌর কোষে ব্যবহৃত হয় ক্যাডমিয়াম (Cadmium)। বিশ্বের সর্ববৃহৎ সৌরশক্তি কেন্দ্র (Solar power plant) যুক্তরাষ্ট্রে অবস্থিত।
সৌরশক্তি চালিত বিশ্বের প্রথম রেলওয়ে সুড়ঙ্গ (Tunnel) বেলজিয়াম অবস্থিত।
পানি শক্তির অন্যতম উৎস। পানির প্রবাহকে ব্যবহার করে বিদ্যুৎ উৎপাদন করা হয়, এই বিদ্যুৎকে জলবিদ্যুৎ বা পানি বিদ্যুৎ (Hydroelectricity) বলা হয়।
নবায়ন অযোগ্য জ্বালানি (Unrenewable energy)
যে শক্তি বারবার ব্যবহার করা যায় না, এবং ব্যবহারে এক সময় শেষ হয়ে যায় তাকে নবায়ন অযোগ্য সম্পদ বলে। যেমন: গ্যাস, তেল, কয়লা ইত্যাদি।
জীবাশ্ম জ্বালানি (Fossil fuel)
জীবদেহ (প্রাণী ও উদ্ভিদ উভয়ই) মাটির নীচে চাপা পড়ে লক্ষ লক্ষ বছর পর তা রূপান্তরিত হয় কয়লা, তেল বা প্রাকৃতিক গ্যাসে। এজন্য কয়লা (Coal), খনিজ তেল (Petrolium) ও প্রাকৃতিক গ্যাসকে (Natural gas) জীবাশ্ম জ্বালানি বলা হয়। জীবাশ্ম জ্বালানি দহনের ফলে বায়ুমণ্ডলে গ্রিন হাউজ গ্যাস কার্বন ডাই-অক্সাইডের পরিমাণ সবচেয়ে বেশি বৃদ্ধি পাচ্ছে।
নবায়ন অযোগ্য জ্বালানি যেমন: ডিজেল পোড়ালে বাতাসে SO2 এর আধিক্য দেখা যায়। -কাঠ ও কয়লার প্রধান উপাদান কার্বন (Carbon)।
তাপ উৎপাদন ক্ষমতা ও কার্বনের পরিমাণের উপর ভিত্তি করে কয়লা তিন প্রকার। যথা:
১) অ্যানথ্রাসাইট ২) বিটুমিনাস ৩) পিট কয়লা।
নিম্নে কিছু কয়লার নাম ও বৈশিষ্ট্য উল্লেখ করা হল:-
কয়লার নাম | বৈশিষ্ট্য |
| অ্যানথ্রাসাইট | কার্বনের পরিমাণ সবচেয়ে বেশি |
| বিটুমিনাস | লিগানাইট কয়লার পরিবর্তিত রূপ |
| পিট কয়লা | ভিজা ও নরম। |
# বহুনির্বাচনী প্রশ্ন
আপেক্ষিকতাবাদ (Theory of Relativity)
১৯০৫ সালে জার্মান বিজ্ঞানী আলবার্ট আইনস্টাইন দেখান যে, পদার্থ এবং শক্তি প্রকৃতপক্ষে অভিন্ন। পদার্থকে শক্তিতে রূপান্তরিত করা যায়। m ভর বিশিষ্ট কোনো পদার্থকে সম্পূর্ণরূপে শক্তিতে রূপান্তরিত করলে প্রাপ্ত শক্তির পরিমাণ হবে E = mc2, এখানে হলো আলোর বেগ। একে আইনস্টাইনের পদার্থ ও শক্তির অভিন্নতা বিষয়ক সূত্র বলা হয়।'থি ওরি অব রিলেটিভিটি'র প্রণেতা আলবার্ট আইনস্টাইন। প্রখ্যাত বৈজ্ঞানিক আইনস্টাইনের নামের সাথে বাংলাদেশি বৈজ্ঞানিক ঢাকা বিশ্ববিদ্যালয়ের অধ্যাপক সত্যেন্দ্রনাথ বোস (Prof. M.N Bosh) এর নাম জড়িত।
বোস - আইনস্টাইন পরিসংখ্যান
সত্যন্দ্রনাথ বসু ছিলেন এক ভারতীয় বাঙালি পদার্থ বিজ্ঞানী। তিনি আলবার্ট আইনস্টাইনের সাথে যৌথভাবে বোস-আইনস্টাইন পরিসংখ্যান প্রদান করেন, যা পদার্থবিজ্ঞানের অন্যতম গুরুত্বপূর্ণ আবিষ্কার হিসেবে বিবেচিত হয়। সত্যেন্দ্রনাথ বসু বৃহত্তর বাংলার তিন শিক্ষায়তন ঢাকা, কলকাতা এবং বিশ্বভারতী বিশ্ববিদ্যালয়ের সাথে সম্পৃক্ত ছিলেন।
# বহুনির্বাচনী প্রশ্ন
হিগস-বোসন (Higgs Boson)
মহাবিশ্বে দুই ধরণের মৌলিক কণিকা আছে। যথা- বোসন ও ফার্মিয়ন। মহাবিশ্বে চার ধরনের বল রয়েছে। যথা- মহাকর্ষ, তাড়িৎচৌম্বকীয়, দুর্বল নিউক্লিয়ার বল এবং শক্তিশালী নিউক্লিয়ার বল। এ বল বা মিথষ্ক্রিয়াগুলো কার্যকর হয় বলবাহক কণাগুলোর আদান-প্রদানের মধ্য দিয়ে। বলবাহক এ কণাগুলো হচ্ছে গ্রাভিট্রন, ফোটন, ডব্লিউজেড ও গ্লুয়ন। কণাগুলোর সাধারণ নাম বোসন কণা। বোসনের একটি সাধারণ ধর্ম হচ্ছে স্পিন বা ঘূর্ণনবেগ পূর্ণ সংখ্যার। এই বোসন কণাগুলো বোস-আইনাস্টাইন পরিসংখ্যান মেনে চলে। ভারতীয় বাঙালি পদার্থবিজ্ঞানী সত্যেন্দ্রনাথ বসু (Prof. M.N Bosh) আলবার্ট আইনস্টাইনের সাথে যৌথভাবে বোস-আইনস্টাইন পরিসংখ্যান প্রদান করেন। অধ্যাপক সত্যেন্দ্রনাথ বসু বৃহত্তর বাংলার তিন শিক্ষায়তন ঢাকা, কলকাতা এবং বিশ্বভারতী বিশ্ববিদ্যৗালয়ের সাথে সম্পৃত্ত ছিলেন। ব্রিটিশ পদার্থবিজ্ঞানী পিটার হিগস ১৯৬৪ সালে শক্তি হিসেবে এমন একটি কণার ধারণা দেন, যা বস্তুর ভর সৃষ্টি করে এবং এর ফলে মহাবিশ্ব সৃষ্টি সম্ভব হয়েছে। এই কণাটি হল হিগের কণা। হিগস কণাকে বিজ্ঞানে হিগস বোসন বলেই উল্লেখ করা হয়। কারণ হিগস কণা একটি বোসন কণা। এ কণিকাকে অনেকে মজা করে ঈশ্বরের কণিকাও বলে খ থাকেন। হিগস বোসন কোয়ান্টাম তত্ত্বের একটি বিষয়। মহাবিশ্বে আরেক ধরণের কণা হচ্ছে ইলেকট্রন, প্রোটন এবং নিউট্রন। এগুলোকে বলা হয় ফার্মিয়ন। ফার্মিয়নের স্পিন ভগ্নাংশ সংখ্যার। এ কণাগুলো ফার্মি-ডিরাক-ডিরাক পরিসংখ্যান মেনে চলে।
# বহুনির্বাচনী প্রশ্ন
নিউক্লিয় শক্তি (Nuclear Energy)
নিউক্লিয়াস ভেঙ্গে বা বিভাজন করে অথবা দুটি হাল্কা নিউক্লিয়াসকে একত্রিত করে যে শক্তি পাওয়া যায়, এই শক্তিকে বলা হয় নিউক্লিয় শক্তি (Nuclear energy)। একে পারমাণবিক শক্তি (Atomic energy) নামেও অভিহিত করা হয়। পরমাণু হতে দুটি পদ্ধতিতে নিউক্লিয় শক্তি উৎপন্ন করা যায়-
ক) নিউক্লিয় ফিউশান (Nuclear Fusion)
খ) নিউক্লিয় ফিশান (Nuclear Fission)
যে নিউক্লিয় বিক্রিয়ায় দুটি ক্ষুদ্র নিউক্লিয়াস একত্রিত হয়ে অপেক্ষাকৃত বড় নিউক্লিয়াসযুক্ত ভিন্ন মৌল তৈরি করে তাকে নিউক্লিয় ফিউশান বা নিউক্লিয় সংযোজন বিক্রিয়া বলে। সূর্য ও অন্যান্য নক্ষত্রে শক্তির উৎস হচ্ছে নিউক্লিয় ফিউশান বিক্রিয়া। নিউক্লিয় ফিউশান নীতির উপর ভিত্তি করে হাইড্রোজেনের আইসোটোপ- ডিউটেরিয়াম, ট্রাইটিয়াম ব্যবহার করে হাইড্রোজেন বোমা তৈরী করা হয়।
পারমাণবিক চুল্লি (Nuclear Reactor)
যে যান্ত্রিক ব্যবস্থার সাহায্যে নিউক্লিয়াসের নিয়ন্ত্রিত বিভাজন দ্বারা বিপুল পরিমাণ পারমাণবিক শক্তি অর্জন করা যায় তাকে পারমাণবিক চুল্লি বলে। পারমাণবিক চুল্লিতে ইউরেনিয়াম ব্যবহার করা হয়, ইউরেনিয়াম পরমাণু স্বতঃস্ফূর্তভাবে ভেঙ্গে নিম্নতর ভর বিশিষ্ট পরমাণু সৃষ্টি হয়ে প্রচুর শক্তি উৎপন্ন হয় এবং উচ্চ গতি সম্পন্ন নিউট্রন নির্গত হয়। এই অতিরিক্ত নিউট্রনকে শোষণ করার জন্য চুল্লীতে ক্যাডমিয়াম ও বোরন দণ্ড ব্যবহার করা হয়, যা অতিরিক্ত নিউট্রনকে শোষণ করে নেয়। পারমাণবিক চুল্লিতে তাপ পরিবাহক হিসাবে সোডিয়াম ব্যবহৃত হয়।
জেনে রাখা ভালো
১. PCR-এর পরিপূর্ণ অর্থ পলিমার চেইন রিঅ্যাকশন।
২. ফিশন আবিষ্কার করেন জার্মান বিজ্ঞানী অটোহ্যান; ১৯৩৯ সালে।
৩. মানবকল্যাণে পারমাণবিক শক্তির ব্যবহার প্রথম শুরু হয়- ১৯৫৪ সালে। ঐ সময় তৎকালীন সোভিয়েত ইউনিয়নে প্রথম নিউক্লিয় তড়িৎ কেন্দ্রে তড়িৎ উৎপাদন শুরু করে।
# বহুনির্বাচনী প্রশ্ন
Read more






